Clear Sky Science · zh
MGMT 上调介导由 USP5 依赖性带来的替莫唑胺耐药性
为何某些脑肿瘤对关键药物失去反应
对于患有侵袭性脑癌胶质母细胞瘤的患者,医生依赖的主要药物之一是替莫唑胺。起初,这种化疗能够抑制疾病进展,但肿瘤常常学会如何摆脱其作用。本研究提出了一个关系生死的实用问题:究竟是什么让这些癌细胞逃避药物?我们能否找到新的薄弱环节来攻击,从而让治疗重新发挥效用?
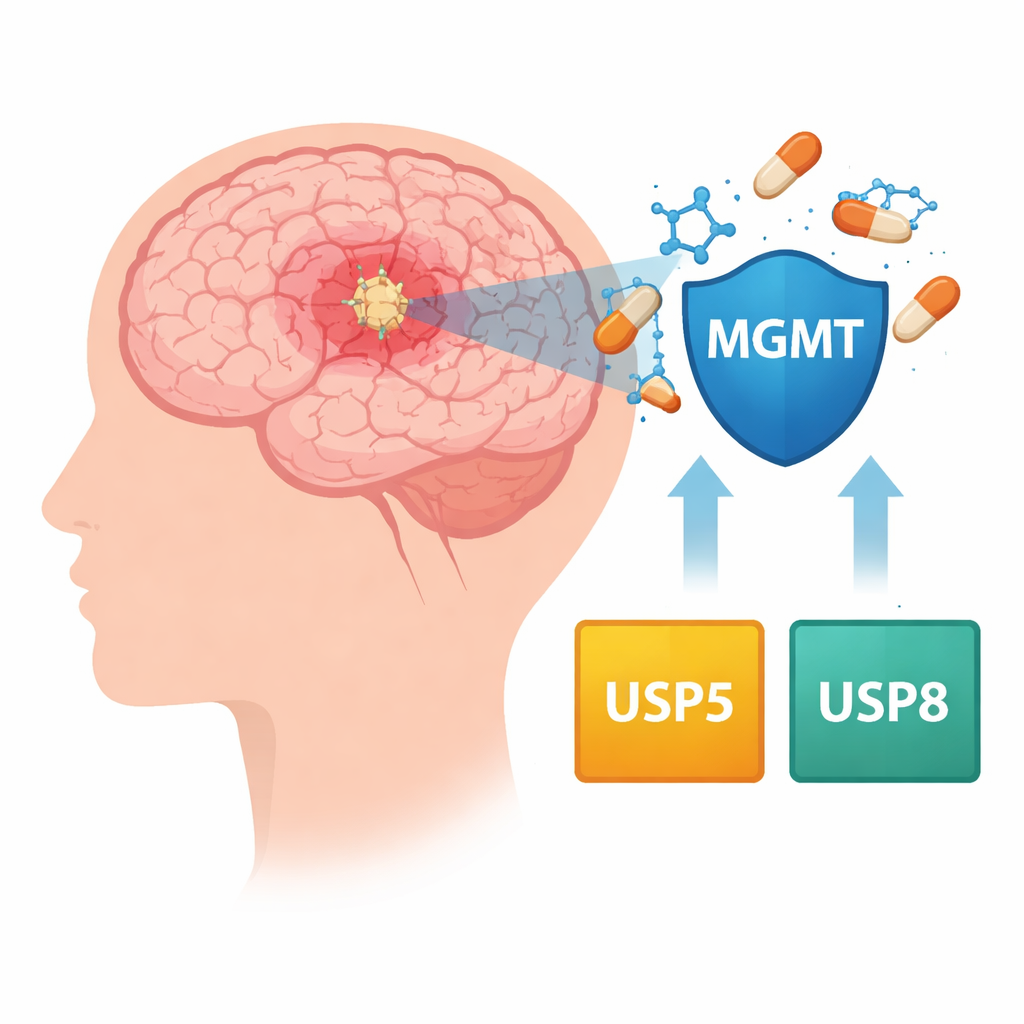
一种起效后逐渐失效的药物
替莫唑胺通过损伤迅速分裂的肿瘤细胞的 DNA 来发挥作用,迫使它们走向死亡。然而,许多胶质母细胞瘤会产生一种称为 MGMT 的修复蛋白,能够逆转这种损伤。那些肿瘤开启 MGMT 的患者预后通常更差,因为药物的效应被抵消。医生可以通过检测 MGMT 基因是否被化学性关闭(甲基化)或开启(未甲基化)来部分预测疗效,但这并不能完全解释耐药如何发生,也不能解释 MGMT 水平如何在肿瘤细胞内长期保持偏高。
保护修复蛋白的隐秘帮手
作者们考察了另一层调控:决定哪些蛋白被降解、哪些被保留的分子“清理队”。细胞通常会标记需报废的蛋白以便降解,而一类称为去泛素化酶(DUBs)的酶可以将蛋白从这种命运中救回。通过挖掘大型公共癌症数据库并检查在实验室中培养的耐药胶质母细胞瘤细胞系,研究团队锁定了两种此类酶:USP5 和 USP8。在数百名患者的肿瘤样本中,较高的 USP5 水平往往与较高的 MGMT 水平并存,且两者同时高表达的患者通常死亡更早。
在实验室构建耐药性
为了模拟患者体内的情形,研究人员将两种常见的胶质母细胞瘤细胞系缓慢暴露于递增剂量的替莫唑胺,直到细胞变得耐药。在这些被“锻造”的细胞中,多种 DUB 上调,但 USP5、USP8、USP10 以及修复蛋白 MGMT 尤其显著。当团队用小 RNA 分子沉默 USP5 或 USP8 时,耐药细胞突然变得脆弱:它们启动自我毁灭程序,包括细胞凋亡和一种由压力驱动的自噬形式。与此同时,MGMT 水平急剧下降,另一个与耐药相关的蛋白 USP10 也被降低,提示这些酶位于细胞生存网络的上游位置。
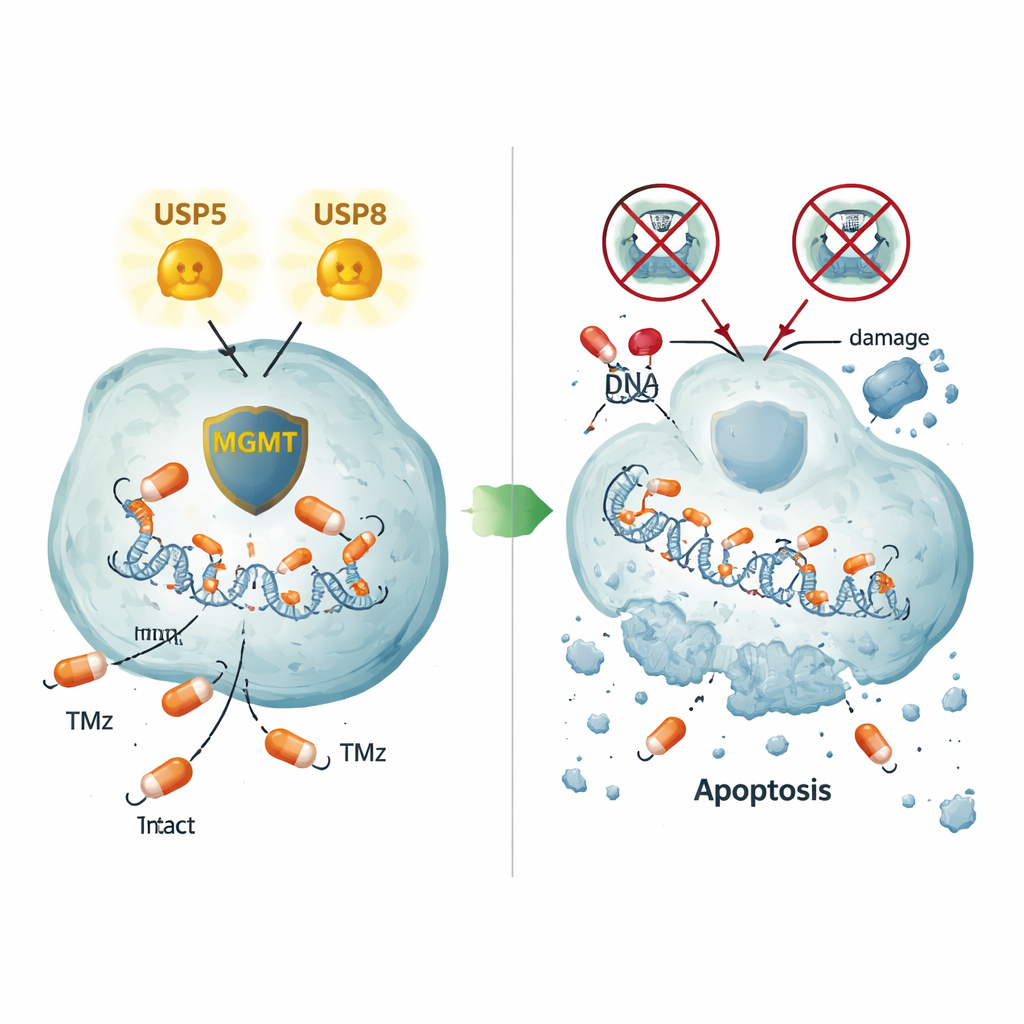
保持 MGMT 存活的两条不同途径
对肿瘤细胞和人类肿瘤组织的精细成像显示,USP5 与 MGMT 经常在细胞的相同区域共定位,尤其是在细胞质中。抑制 USP5 不仅降低了 MGMT,还导致 MGMT 被细胞的蛋白降解机器分解,这一过程可被阻断蛋白酶体的小分子抑制剂硼替佐米逆转。在本来不表达 MGMT 的细胞中过量表达 USP5 就足以提升 MGMT 蛋白水平,甚至在非脑细胞系中也成立,证明了其直接的稳定作用。USP8 的作用则不同:敲低 USP8 也会降低 MGMT,但不会改变 USP5 本身,显示出一条第二条、与 USP5 无关的维持 MGMT 的途径。即便在某些不产生 MGMT 的耐药细胞系中,关闭 USP5 或 USP8 仍能引发大量细胞死亡,表明这些酶还控制着其他促耐药通路。
与免疫系统的联系及新的治疗思路
除了药物耐受性外,这项研究还将 USP5 与胶质母细胞瘤如何与免疫系统相互作用联系起来。基因组数据分析表明,USP5 水平和基因拷贝数的变化会改变肿瘤周围多种免疫细胞的平衡,包括杀伤性 T 细胞和调节性 T 细胞。先前的研究也表明 USP5 能稳定 PD‑L1,这是一种肿瘤用来抑制攻击性 T 细胞的蛋白。综合来看,这些发现提示 USP5 可能既帮助肿瘤耐受化疗,又帮助其逃避免疫攻击,使其成为一个尤其有吸引力的药物靶点。
对未来脑癌治疗的意义
简而言之,这项工作确认了 USP5 和 USP8 是保护 MGMT 修复蛋白并帮助胶质母细胞瘤细胞抵抗替莫唑胺的关键“保镖”。通过拆除这些“保镖”,作者在实验室中能够杀死耐药细胞并降低 MGMT 水平,即便在某些 MGMT‑驱动的耐药并非唯一问题的情况下亦然。这带来了希望:未来以 USP5 或 USP8 为靶点的药物,可能与现有的化疗和免疫疗法联合使用,使顽固的脑肿瘤重新恢复对治疗的敏感性,从而延长患者的生存时间。
引用: Bhardwaj, S., Sanjay, Sharma, D. et al. MGMT upregulation mediates Temozolomide resistance conferred USP5 dependency. Sci Rep 16, 6118 (2026). https://doi.org/10.1038/s41598-026-36379-4
关键词: 胶质母细胞瘤, 替莫唑胺耐药, MGMT, USP5, 去泛素化酶