Clear Sky Science · zh
解密COPD发病机制:一种多组学方法以识别代谢物和遗传关联
为何肺病与体内化学过程有关联
慢性阻塞性肺病(COPD)通常被认为是吸烟者的肺病,但这项研究表明,血液化学中发生的变化可能与我们吸入的物质一样重要。通过整合大型遗传数据集、血中小分子(代谢物)的精确测量以及对人体气道细胞的实验室研究,研究人员揭示了体内受损的脂肪处理如何可能推动COPD进展——以及一种常见吸入器药物沙丁胺醇可能以一种令人意外的方式发挥作用。
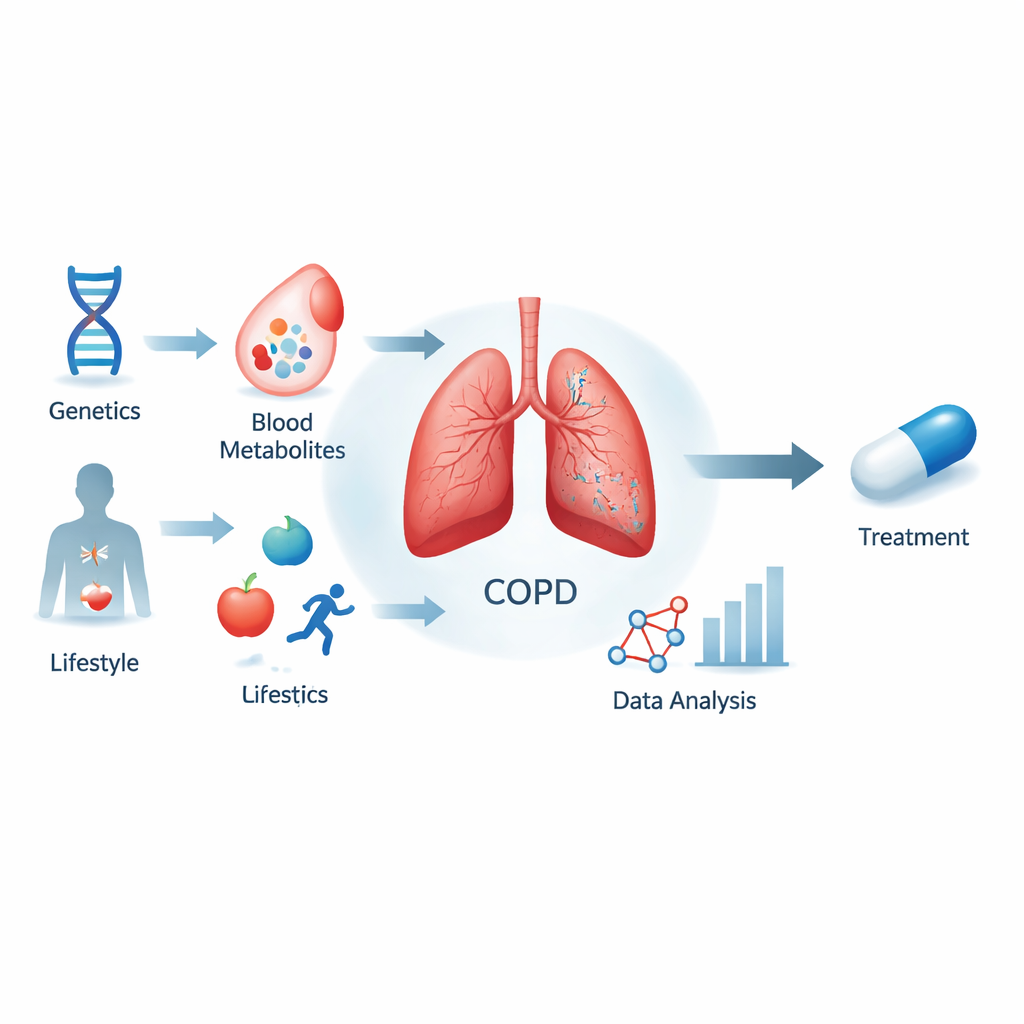
超越吸烟:深入观察COPD
COPD影响全球数亿人,预计将成为第三大死因。尽管吸烟和空气污染是主要原因,但它们并不能完全解释谁会患病或病情进展的速度。本研究团队质问:血液中的特定分子—称为代谢物—是否不仅仅是损伤的标志,而是疾病的活跃参与者。他们关注了在大型欧洲研究中测量的超过1,400种代谢物,并利用人群之间的遗传差异作为一种天然实验,将这些代谢物与COPD风险联系起来。
用基因检验因果关系
为了超越简单的相关性,研究人员使用了一种称为孟德尔随机化的技术。简单来说,他们追踪那些天生携带使某些代谢物升高或降低的基因变体的人,是否也更有可能患上COPD。这种方法有助于将真正的因果关系与诸如喝咖啡或吸烟等可能混淆结果的生活习惯区分开来。在1,400多种代谢物中,最初有六种与COPD风险相关。然而,第二轮更严格的遗传检验显示,只有两种——十四碳肉碱(Carnitine C14)和3-羟基油酰肉碱(3-hydroxyoleoylcarnitine)——与COPD拥有相同的潜在遗传信号。两者都与机体处理长链脂肪酸的方式有关,这提示脂肪代谢,而不仅仅是炎症和气流受限,可能是COPD的核心因素。
从分子追溯到关键调控开关
一旦确认了这两种可靠的代谢物,研究人员将它们追溯到所经过的代谢“道路”。这些道路汇聚到脂肪酸代谢,并突出了一组像交通信号灯一样的酶,控制着脂肪的合成与分解——尤其是酶ACACA和ACACB。通过挖掘现有的药物和蛋白相互作用数据库,团队发现这些酶位于与ADRB2相同的网络中,ADRB2是沙丁胺醇这一常用COPD救援吸入器的蛋白靶点。患者肺组织的分析显示,ACACA和ACACB表达上调,而ADRB2表达下调,这与病变肺中脂肪酸过载的状态一致。
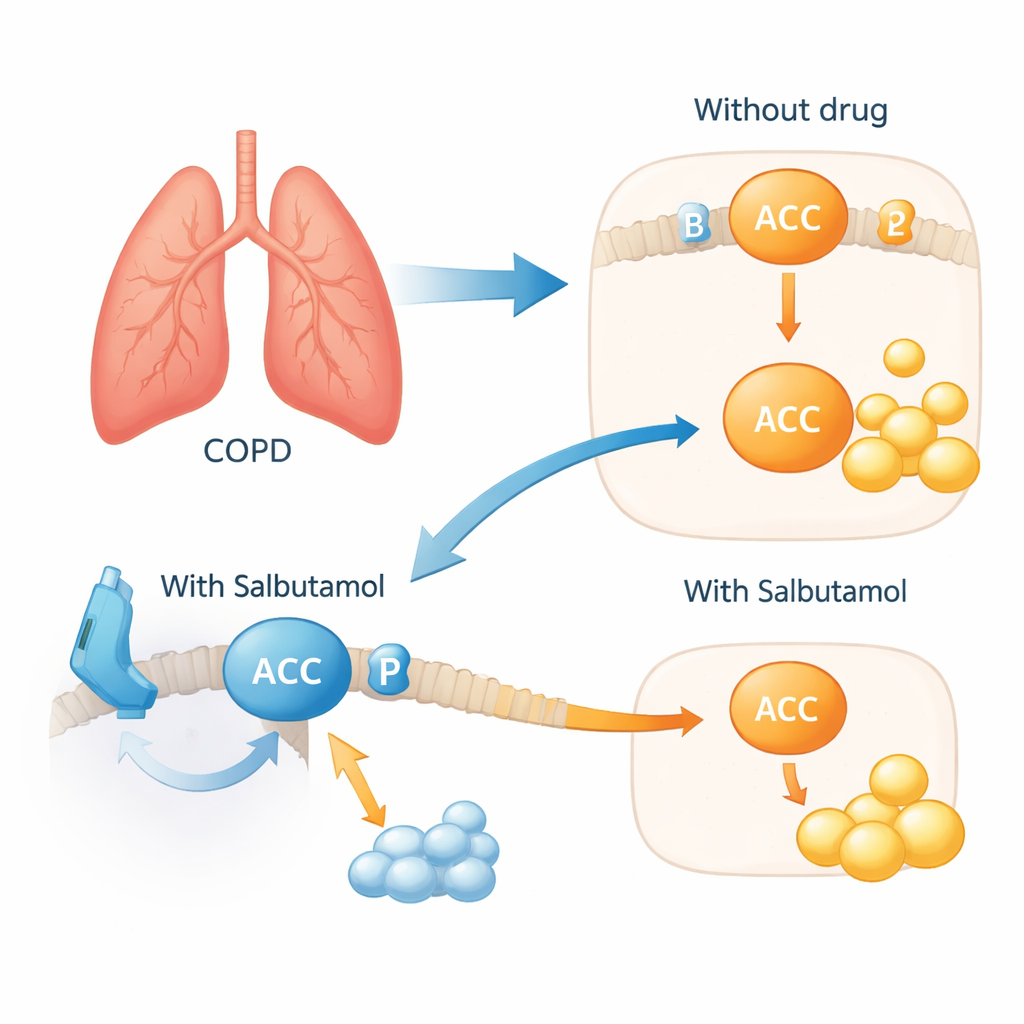
一种也能平抑失控脂肪代谢的吸入器
为了检验该网络在活细胞中是否重要,科学家们用香烟烟雾提取物刺激人支气管细胞以模拟COPD样应激。细胞的反应是上调ACACA和ACACB,并减少ACACA上的一种保护性化学标记,该标记通常用于抑制脂肪合成。当加入沙丁胺醇后,这种有害模式被逆转:ACACA上的保护性标记恢复,过度脂肪合成的迹象减少。简言之,该药物似乎通过位于细胞表面的ADRB2“开关”重新给细胞内的脂肪合成机制刹车。基于生活方式的遗传分析进一步支持这两个关键代谢物与基础生物学有关,而不仅仅是像咖啡摄入这样的习惯,这解释掉了若干其他候选分子的关联。
对病人和未来疗法的意义
对非专业读者而言,核心信息是:COPD部分由肺细胞处理脂肪的代谢拥堵驱动,而一种广泛使用的支气管舒张剂也可能在悄然帮助疏通这种拥堵。十四碳肉碱和3-羟基油酰肉碱作为强有力的血液标志物出现,将来可能有助于标识高风险人群或跟踪病情进展。位于脂肪代谢关键节点并与沙丁胺醇靶点ADRB2相关联的酶ACACA和ACACB,为药物开发者提供了新的干预靶点。尽管还需要在更多不同人群中以及更深入的代谢学研究,但这种多组学方法为COPD的治疗开辟了一条新路径——这些治疗或许不仅能打开气道,还能恢复肺内更健康的能量利用方式。
引用: Zeng, M., Liu, J., Cao, X. et al. Unraveling COPD pathogenesis: a multi-omics approach to identify metabolites and genetic links. Sci Rep 16, 6013 (2026). https://doi.org/10.1038/s41598-026-36368-7
关键词: COPD, 脂肪酸代谢, 沙丁胺醇, 肉碱生物标志物, 多组学