Clear Sky Science · zh
MNX1介导的组蛋白修饰与PBX基因家族在MNX1诱导的白血病发生中的作用
为什么一个微小的基因错误对生病的儿童至关重要
大多数儿童白血病现在可以治疗,但一种称为婴儿急性髓性白血病(AML)的罕见类型仍然尤其致命。许多患儿共有同样的遗传事故:两条染色体互换片段,使一个在发育中通常沉默的基因MNX1变得过度活跃。本研究提出了一个简单但关键的问题:一旦MNX1被激活,它在幼年造血细胞内究竟做了什么推动它们走向癌变——这一过程能否被阻断?
从正常胎儿血细胞到失控生长
白血病发生于未成熟的血细胞停止分化并开始失控增殖。在携带t(7;12)染色体易位的婴儿中,MNX1在胎肝和骨髓中非常早期的造血细胞里异常活跃。研究者建立了一个模拟这种情况的小鼠模型:他们在胎儿造血干细胞中开启人源MNX1,将其移植到小鼠体内,并观察动物从白血病前期状态发展为全面白血病。通过将不同时期的细胞与健康对照比较,他们追踪了MNX1如何随时间重塑细胞的内部控制系统。
MNX1如何重写细胞的指令手册
MNX1是一种转录因子,附着于DNA并控制哪些基因被开启或关闭。团队结合了多种强有力的方法——质谱、RNA测序和染色质谱系分析——以识别MNX1的合作伙伴及其调控的基因。他们发现MNX1与为组蛋白添加化学标记的酶协同工作。特别地,MNX1增强了一种“开启”标记H3K4me3,并在基因组的特定位点降低了一种“关闭”标记H3K27me3。这些改变松散了局部的DNA结构,使关键的增殖相关基因更容易被激活。
对关键控制基因的“打击即跑”推动
在众多受影响的基因中,有一个尤为突出:Pbx1,它属于长期与白血病相关的PBX家族DNA结合蛋白。研究显示MNX1直接结合于Pbx1基因的调控区,在该处增加“开启”标记并去除“关闭”标记。这在细胞仍处于白血病前期时就启动了Pbx1的表达。令人意外的是,后来——一旦白血病建立,MNX1自身在该位点的结合并不强烈,但Pbx1基因仍保持开启状态,其组蛋白标记也保持有利于生长的构型。这提示了一种“打击即跑”机制:MNX1短暂作用于关键染色质区域,留下持久的表观遗传标记,然后离开,而被改变的状态仍然继续推动疾病。
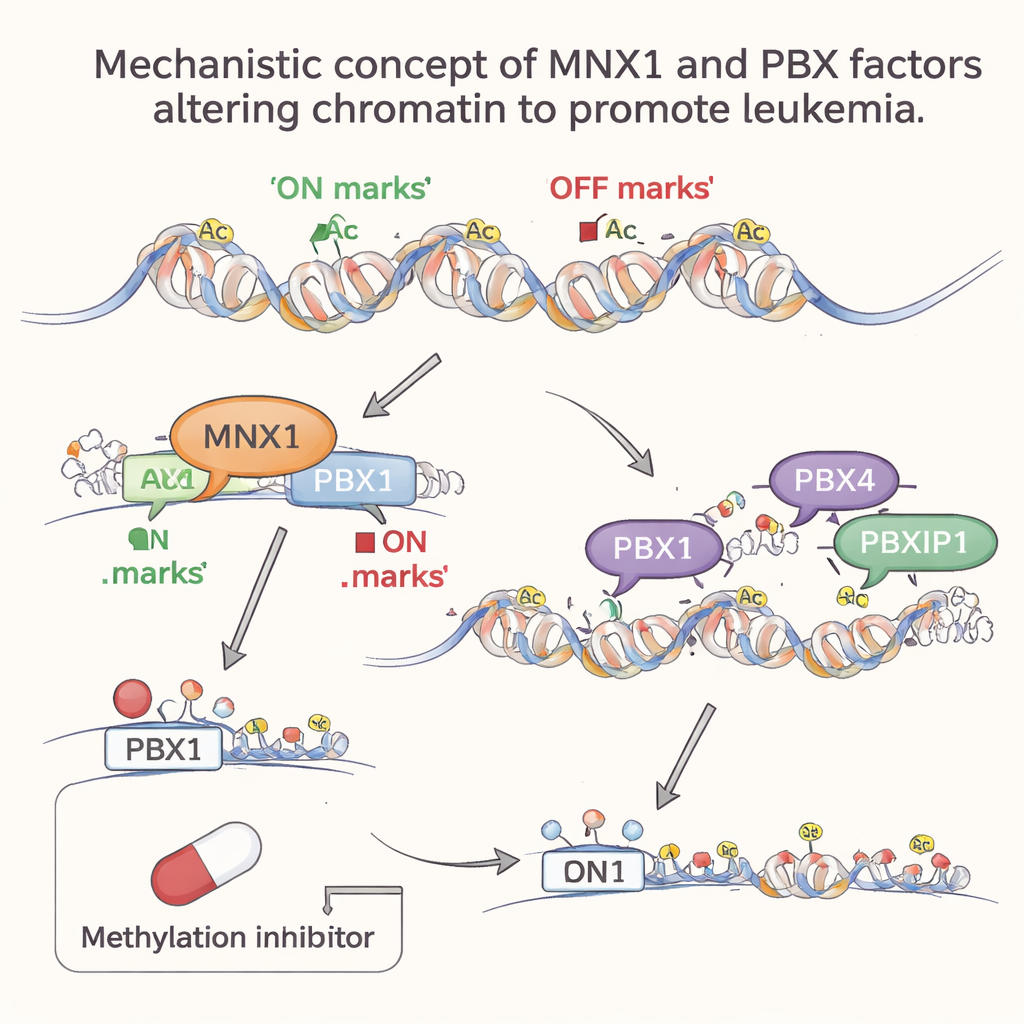
后期帮手加入以锁定癌变状态
随着白血病进展,其他PBX家族成员PBX4和PBXIP1的活性在后期变得更高,但仅限于这一阶段。全基因组分析显示,它们偏好的DNA基序在那些已被MNX1重塑、变为开放活跃的染色质区域中显著富集。换言之,MNX1先改造染色质景观并激活Pbx1;随后PBX4和PBXIP1进入这些新暴露的区域,强化异常基因程序,促进细胞分裂、阻断正常血液发生并削弱DNA修复。阶梯式的参与暗示了分工:PBX1作为依赖MNX1的早期开关发挥作用,而PBX4和PBXIP1则帮助维持白血病程序。
阻断推动白血病的化学标记
由于MNX1通过向组蛋白添加甲基基团的酶发挥作用,研究组测试了一种广谱甲基转移酶抑制剂Sinefungin是否能打断这一连锁反应。在表达MNX1的白血病前期胎儿造血细胞中,Sinefungin显著降低了Pbx1水平,与阻断MNX1依赖的启动子特异性甲基化相符。相比之下,PBX4和PBXIP1的水平几乎没有变化,这与它们在疾病进展中后期的间接激活相一致。综合这些结果强有力地表明,携带t(7;12)的婴儿AML并非仅由一个损坏的基因驱动,而是由MNX1引发的一连串持久表观遗传改变所推动。
这对未来治疗意味着什么
对非专业读者而言,核心信息是本研究描绘了一条连锁反应:过度活跃的MNX1基因重塑包裹DNA的蛋白上的化学标记、早期激活PBX1,并为PBX4和PBXIP1协助将细胞锁定在白血病状态铺平道路。由于这些步骤依赖特定的组蛋白甲基化模式,它们为干扰这些标记的药物提供了明确且可检验的靶点。长期来看,针对MNX1–PBX轴或放置这些表观遗传标签的酶的疗法,可能有助于关闭驱动婴儿这种侵袭性白血病的错误指令,改善实现持久治愈的机会。
引用: Malmhäll-Bah, E., Östlund, A., Nilsson, T. et al. Role of MNX1-mediated histone modifications and PBX gene family in MNX1-induced leukemogenesis. Sci Rep 16, 2593 (2026). https://doi.org/10.1038/s41598-026-36367-8
关键词: 婴儿急性髓性白血病, MNX1, PBX1 PBX4 PBXIP1, 表观遗传组蛋白甲基化, t(7;12) 染色体易位