Clear Sky Science · zh
CDC25C下调通过线粒体应激诱导自噬和凋亡抑制HCC生长
这项肝癌研究为何重要
肝癌是全球最致命的癌症之一,许多患者在被诊断时已错过手术或标准治疗的最佳时机。本研究考察了一个细胞内的“开关”蛋白CDC25C——它似乎推动肝癌增长,但对健康肝细胞的重要性较低。研究者通过下调该开关,发现可以通过细胞自身的清理和自毁系统(自噬与凋亡)对癌细胞施加应激并最终将其消灭,提示这可能是一种有前景且更具选择性的治疗策略。
肝瘤内的生长开关
每个细胞都必须决定何时分裂、何时停止。CDC25C是推动细胞进入分裂周期的关键蛋白之一。在肝癌中,这个开关常常处于“开启”状态,助长肿瘤的生长和扩散。研究团队使用小鼠肝癌细胞和正常小鼠肝细胞,以及带瘤小鼠,通过人工方法降低CDC25C水平。通过常规的基因和蛋白检测,他们确认实验组中CDC25C明显降低,与对照组相比形成了稳固的模型,用以研究当这一生长开关被关闭时会发生什么。
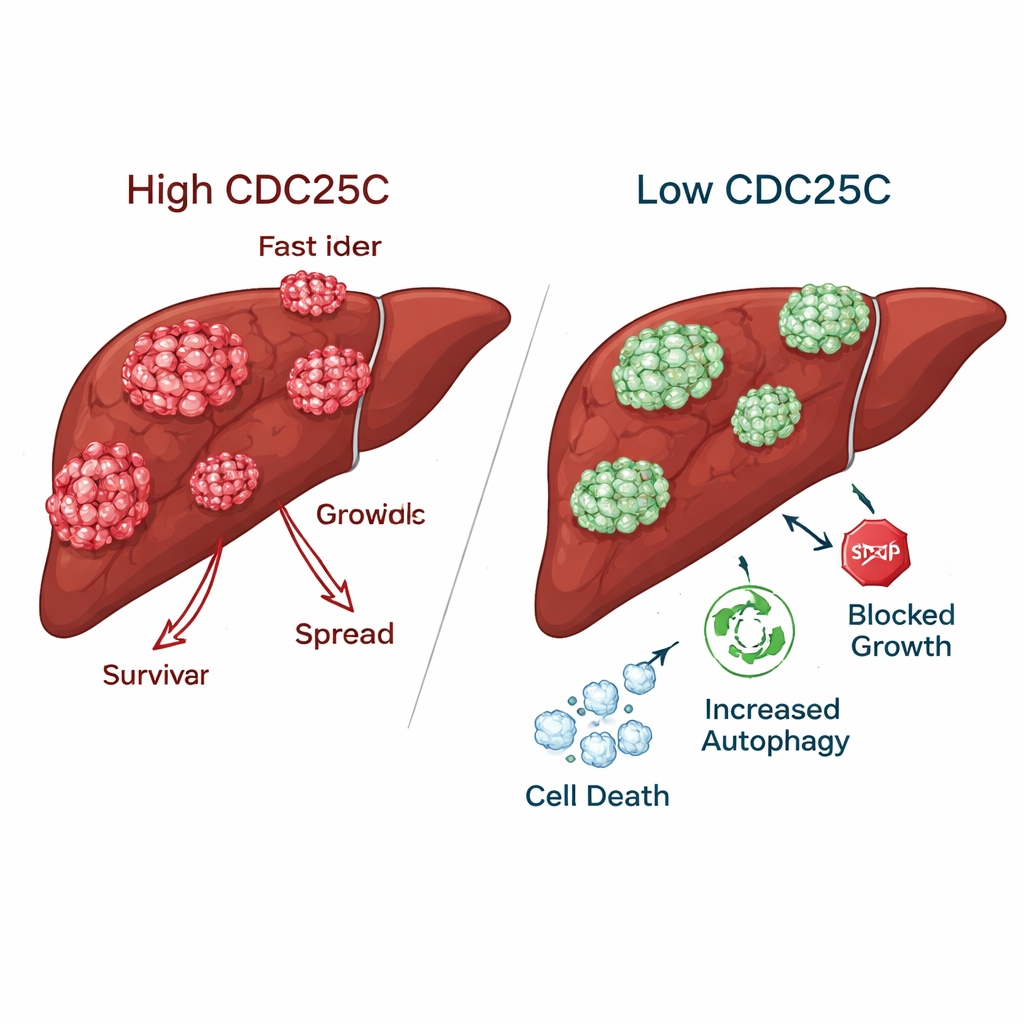
抑制癌细胞同时保护健康肝细胞
在肝癌细胞中下调CDC25C后,肿瘤表现出的许多侵袭性特征减弱。癌细胞形成的克隆显著减少,在人工“划痕”迁移实验中移动变慢,并且在体外侵袭穿透实验中能力下降。相反,正常肝细胞在CDC25C降低时反而表现出更好的生长和迁移能力,提示健康组织可能能耐受甚至从CDC25C抑制中受益。在小鼠体内,工程化下调CDC25C的肿瘤在基因和蛋白水平上均显示该蛋白降低,证实活体中也发生了相同效应。
能量工厂受损与细胞清理机制
借助电子显微镜观察细胞内结构,研究者发现低CDC25C的癌细胞含有肿胀、受损的线粒体——细胞内的小型能量工厂——以及表明细胞内回收系统(自噬)被激活的自噬体泡状结构。随后他们测量了线粒体应激的关键指标:钙离子水平和活性氧(ROS),在CDC25C下调后癌细胞中这两者均升高。线粒体应激反应的标志物也增加,包括伴侣蛋白HSP60和两种线粒体“质量控制”酶,另外与应激相关并将线粒体问题与更广泛细胞反应连接的因子CHOP也上调。值得注意的是,这些应激信号在正常肝细胞中呈相反趋势,进一步支持癌细胞与健康细胞对CDC25C缺失反应迥异的观点。
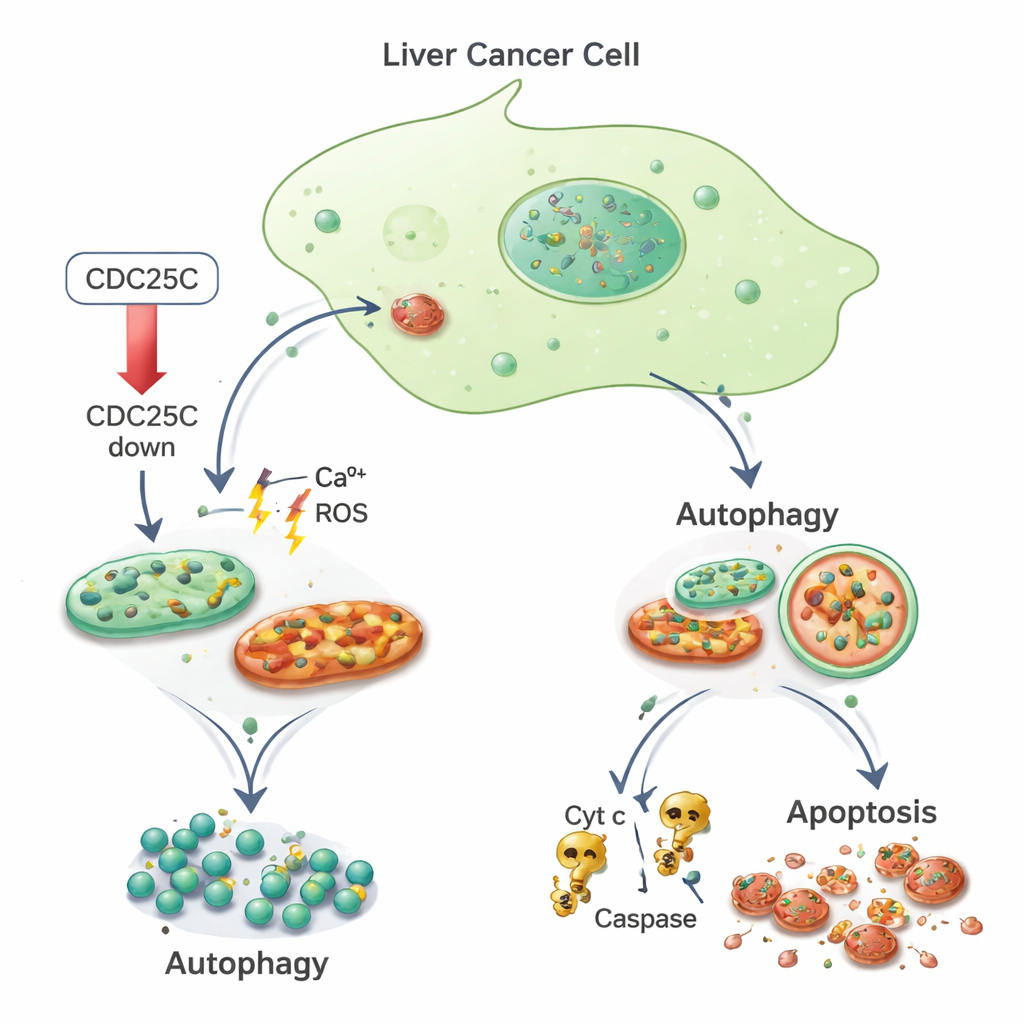
从应激到自我消化与细胞死亡
研究团队接着询问这些承受应激的癌细胞如何应对。他们发现当CDC25C被下调时,自噬的标志在癌细胞和正常肝细胞中均有所增强。反映自噬体形成和活性的蛋白,如LC3和p62,水平均升高,表明细胞正在加强其清理机制。与此同时,仅在癌细胞中,线粒体损伤似乎使细胞无法修复并进入程序性死亡。使用荧光染色和流式细胞术,研究者观察到更多癌细胞出现核碎裂和强烈染色的核,这是凋亡的典型标志,并伴随线粒体膜电位下降。他们还检测到细胞色素c以及Caspase-3和Caspase-9等酶的水平升高,这些是线粒体驱动的死亡通路的经典成分。相比之下,在相同的CDC25C降低条件下,正常肝细胞的凋亡减少。
这对未来治疗意味着什么
对普通读者来说,关键信息是:下调CDC25C似乎攻击了肝癌细胞的薄弱环节,使其线粒体承受过大负荷、推动其回收系统过度运转并最终触发干净的自我毁灭——而对正常肝细胞影响较小。作者总结认为,CDC25C不仅是一个简单的生长开关;它还影响细胞如何处理应激、清理和死亡。由于癌细胞高度依赖CDC25C,并在其缺失时以致命的线粒体应激和凋亡作出反应,靶向该蛋白或其下游应激通路的药物未来可能提供一种更具选择性的肝癌治疗方式,减少对健康肝组织的伤害。
引用: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
关键词: 肝细胞癌, CDC25C, 线粒体应激, 自噬, 凋亡