Clear Sky Science · zh
诱导性耐受紫外线应激驱动同源大肠杆菌群体的存活异质性
为什么阳光对微生物可能致命
来自太阳和消毒灯的紫外线(UV)是杀灭微生物的强有力手段,包括常见的肠道细菌大肠杆菌(Escherichia coli)。然而即便在基因完全相同的一组细菌中,也有一些细胞能在消灭邻居的紫外线轰击中幸存。该研究提出了一个看似简单但对消毒与感染控制有重大影响的问题:这些顽强幸存者是天生不同,还是在受损开始后迅速切换到一种受保护的状态?
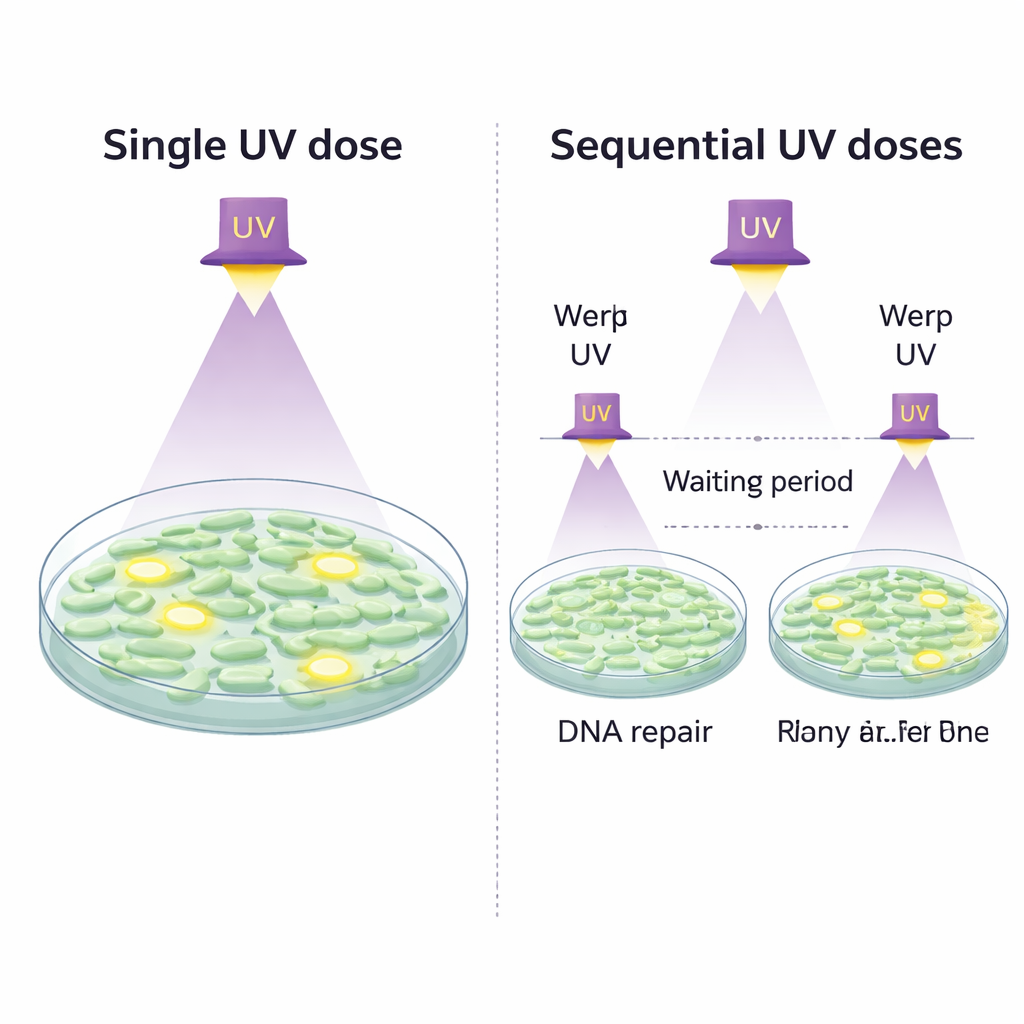
天生强韧,还是经受磨练变强?
多年来,生物学家们已知道少数细菌亚群可以暂时耐受抗生素,而不需要抗药性突变。一种观点认为,少数“预备”细胞在药物到来之前已处于特殊状态,而其余细胞则易感。另一种可能是大多数细胞仅在受击后才做出反应,开启应急系统修复损伤并维持存活。作者希望弄清在大肠杆菌遭受破坏其 DNA 的紫外线攻击时,哪一种情况成立。
一种巧妙的方法来检验隐性差异
为将先天强韧与即时反应区分开,研究者采用了对经典实验(Luria–Delbrück 波动性检验)的现代改良。他们并行培养了许多微小的大肠杆菌培养物。其中一些每个培养物都始于一个单细胞并演化为克隆;另一些作为噪声对照,每个培养物起始于数千个细胞的随机混合。所有培养物随后暴露于由 262 纳米发光二极管发出的可控紫外线剂量,并统计幸存细胞数。如果确有极少数预先处于“预备”状态的细胞存在,那么某些由单细胞起始的克隆在偶然情况下应含有更多预备细胞,从而显示出显著更高的存活率。
紫外线幸存者是被造就的,而非生来如此
在不同紫外线剂量下,大肠杆菌的存活率确实存在变异,但这种变异并不像由预先存在的预备细胞主导时所预期的那样。无论是中等还是极强的紫外线照射,单细胞克隆中幸存者的分布与混合对照培养物非常相似。不存在一组显著高存活的培养物亚群,来指示预先武装的细胞。研究团队还用一种以不同方式损害 DNA 的交联化疗药物丝裂霉素 C(mitomycin C)重复了这一方法,亦未发现广泛耐受 DNA 损伤的稳定预备群体的证据。
两次小击胜过一次重击
当研究者把紫外线剂量分成两次给出时,情况发生了变化。他们先施加一次适度的“第一次击”,在黑暗中等待 30 分钟以便修复系统响应,然后再给出第二次紫外线照射。如果存活纯粹是偶然的,那么通过两次击打存活下来的细胞比例应等于两次单次剂量存活率的乘积。相反,连续低剂量后的实际存活率比这一简单预测高出数倍,并且高于一次性给出等量总能量的单次强照射。这表明第一次击打触发了 DNA 修复途径(如著名的 SOS 反应和核苷酸切除修复),暂时增强了细胞应对后续损伤的能力。
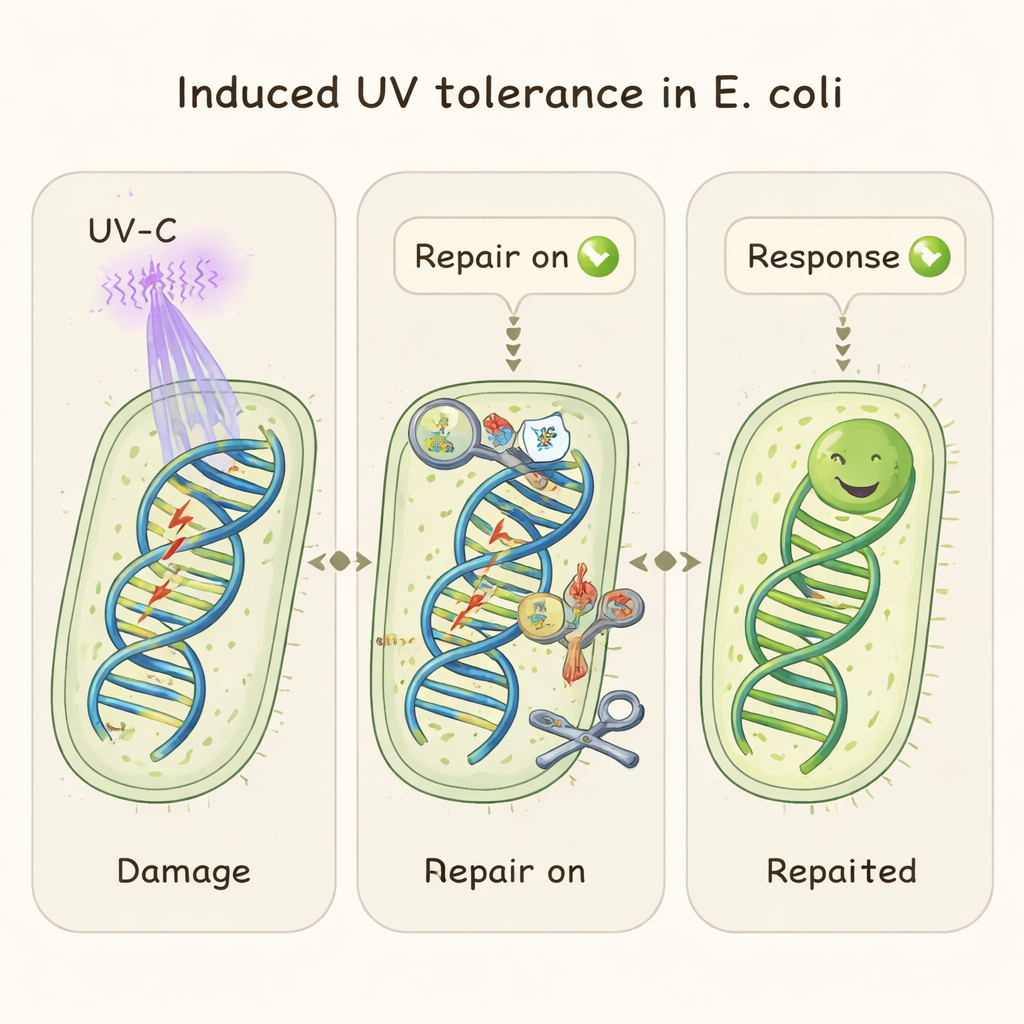
对消毒与存活的含义
用日常语言来说,这项工作表明,基因相同的大肠杆菌细胞并不是因为有些“生来”就被保护而免受紫外线;相反,大多数幸存者在首次暴露后迅速通过开启应急 DNA 修复而变得更强韧。这种被诱导的、短暂的耐受性帮助它们比预期更好地挺过后续的紫外线应激。对于依赖紫外线消毒水、表面或医疗器械的技术而言,这意味着剂量模式和时间安排很重要,而不仅仅是传递的总能量。理解细菌在重复应激下如何动态修复 DNA,可能有助于制定更可靠的灭菌策略,并深化我们对简单生物体在不改变基因的情况下适应恶劣环境的认识。
引用: Ichikawa, S., Tanoue, M., Takeuchi, J. et al. Induced tolerance to UV stress drives survival heterogeneity in isogenic E. coli cell populations. Sci Rep 16, 5931 (2026). https://doi.org/10.1038/s41598-026-36328-1
关键词: 紫外线应激耐受, 大肠杆菌, DNA 修复, 细菌持久体, SOS 反应