Clear Sky Science · zh
D-甘露糖通过微生物—肠—脑轴缓解轮虫酮诱导的帕金森小鼠模型
甜分子,大希望
帕金森病以引起震颤和运动迟缓闻名,但许多患者在确诊前多年就已饱受顽固便秘和其他肠道问题之苦。本研究探讨了一个引人注目的设想:一种名为D-甘露糖的简单糖(已作为膳食补充剂出售)能否通过抑制肠道和大脑的炎症并恢复更健康的肠道微生物群,从而缓解小鼠模型中的帕金森样症状?
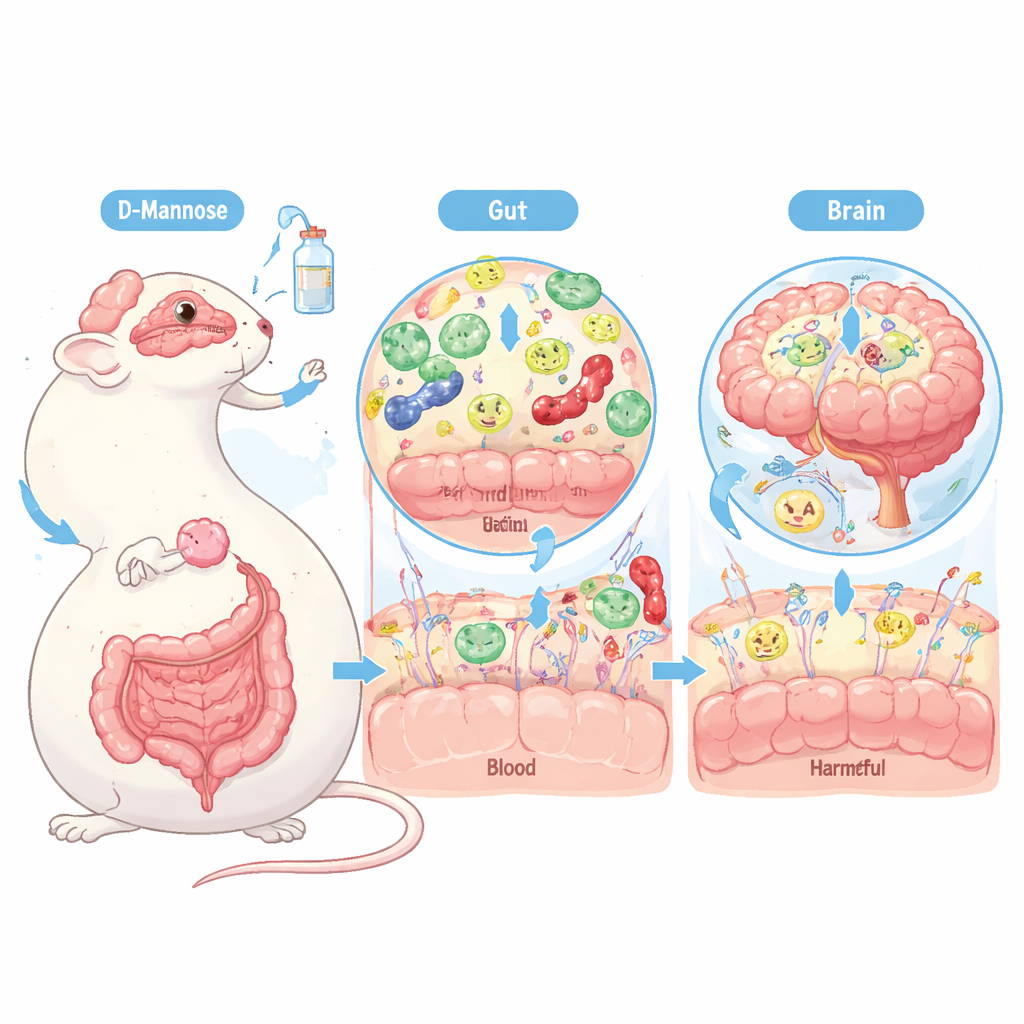
帕金森起于大脑之外
帕金森病影响数百万老年人,目前尚无治愈方法。常规药物可以改善运动症状,但对阻止多巴胺生成神经元持续丧失帮助有限。与此同时,许多帕金森患者伴有慢性便秘和其他消化问题,这提示该疾病不仅仅局限于大脑。越来越多的证据指向一种双向的“肠—脑”对话:肠道细菌的改变和肠道长期存在的炎症可能随着时间推动大脑损伤。
温和的糖接受检验
D-甘露糖是一种天然存在于水果和植物中的糖,已用于预防尿路感染。它被认为安全、耐受性良好,并且不会强烈扰动正常代谢,使其成为长期使用的有吸引力候选物。在这项研究中,研究者给小鼠喂食农药轮虫酮,这是一种已建立的诱导帕金森样运动障碍和肠道功能紊乱的方法。在四周轮虫酮处理后,部分小鼠在随后的两周饮水中加入D-甘露糖。随后研究团队评估了运动、肠道功能、肠道细菌、炎症及脑健康标志物。
运动改善,肠道更平静
轮虫酮处理的小鼠出现了典型的帕金森样问题:运动变慢、抓握力和平衡测试表现变差,并伴有肠道蠕动迟缓与结肠变短。当这些小鼠饮用D-甘露糖后,体重下降有所缓解,运动和抓握力得到改善,在测量协调性和灵活性的任务中表现更好。它们的肠道功能也恢复——结肠变长,食物通过肠道的速度加快,排便更为正常。显微镜下可见结肠黏膜损伤与瘢痕减少,化学检测显示炎性分子和细菌毒素水平降低,表明D-甘露糖有助于修复肠道的保护屏障。
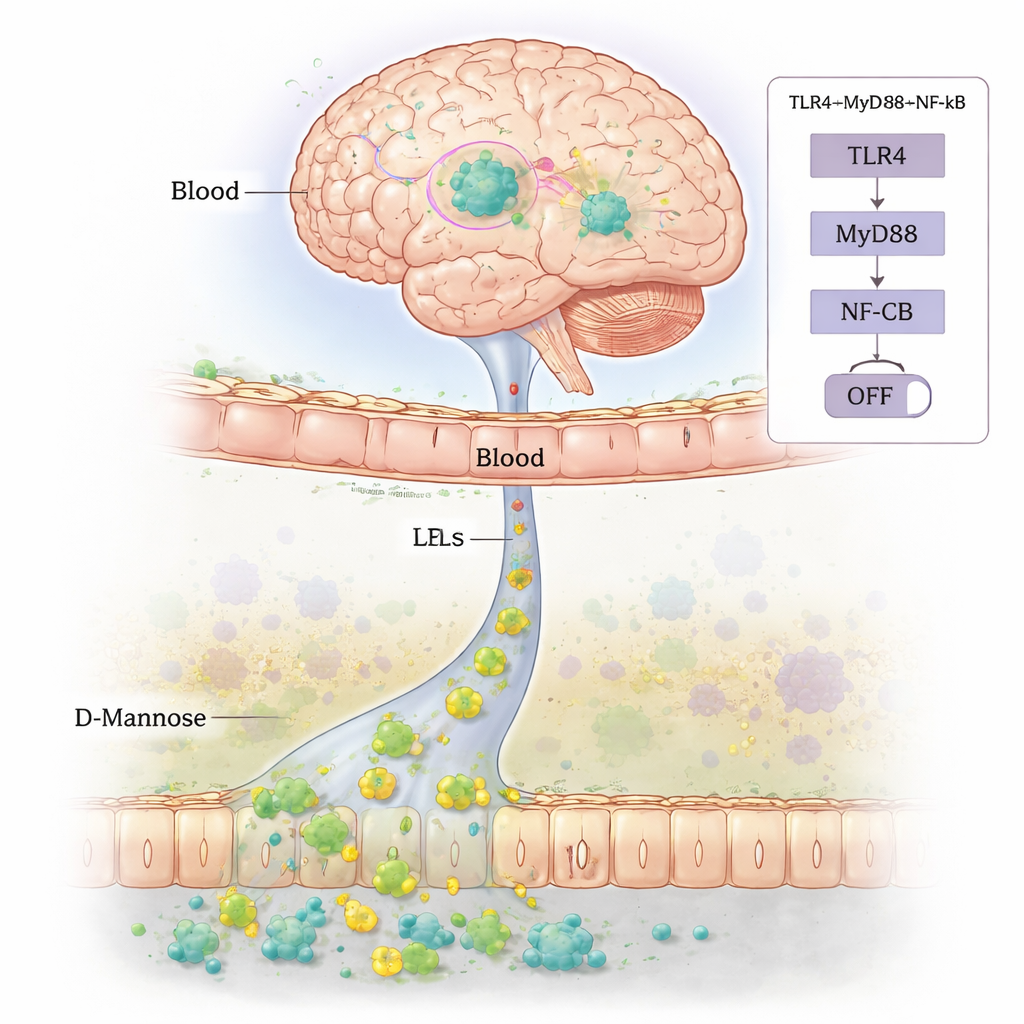
微生物更健康,脑细胞受保护
研究者接着检查了小鼠肠道中的微生物群落。轮虫酮破坏了正常的细菌组成,降低了总体多样性并偏向与炎症相关的菌群。D-甘露糖在一定程度上逆转了这些变化,将微生物群落朝更健康的平衡方向推回。同时,关键运动相关脑区——黑质中的炎症迹象减少。接受D-甘露糖的小鼠有更多存活的多巴胺生成神经元,激活的支持细胞(小胶质细胞和星形胶质细胞)更少,这些细胞通常在脑部炎症时大量出现。血液和大脑中炎性介质及一种名为LPS的细菌毒素水平下降,维持血脑屏障的蛋白质也更好地保存。
平息一种炎性警报通路
为理解这些变化如何关联,研究团队关注免疫细胞内的一个分子警报系统。该系统以TLR4、MyD88和NF-κB等蛋白为核心,当检测到像LPS这样的细菌产物时会被激活,进而驱动强烈的炎性反应。在轮虫酮处理的小鼠中,这一路径在大脑中高度活跃。D-甘露糖抑制了该信号:TLR4、MyD88和活化的NF-κB水平均下降,与炎症和细胞损伤的减少相一致。这些发现表明,通过重塑肠道微生物群、强化肠道与大脑屏障并减少细菌毒素进入血流,D-甘露糖有助于关闭这一炎性警报。
对人类可能意味着什么
小鼠研究并不能证明D-甘露糖能治疗人类的帕金森病,但它指出了一个引人关注的新方向。与其单纯聚焦大脑,研究支持这样一种观点:保护肠道健康并平息肠—脑对话或许有助于保护脆弱的神经细胞。鉴于D-甘露糖已被广泛作为补充剂使用且显现安全,若未来临床研究证实小鼠中观察到的益处可转化到人体,它有望成为管理帕金森病症状的更广泛策略的一部分。
引用: Hong, Y., Ge, C., Jin, J. et al. D-mannose alleviates rotenone-induced PD mouse model through microbiota-gut-brain axis. Sci Rep 16, 5680 (2026). https://doi.org/10.1038/s41598-026-36272-0
关键词: 帕金森病, 肠—脑轴, D-甘露糖, 肠道微生物群, 神经炎症