Clear Sky Science · zh
通过聚合物纳米凝胶重新定位达格列净用于结直肠癌治疗
为什么一种糖尿病药可能有助于对抗结肠癌
结直肠癌是全球癌症相关死亡的主要原因之一,尽管接受手术和化疗,许多患者仍会复发。这项研究探索了一种意想不到的对抗该病的盟友:达格列净,这是一种常用于2型糖尿病的口服药。研究人员通过将该药装入遇胃酸会形成温和凝胶的微小柔软颗粒,旨在将更多药物递送至大肠——结肠肿瘤生长的部位——同时口服剂量与现有片剂相近。
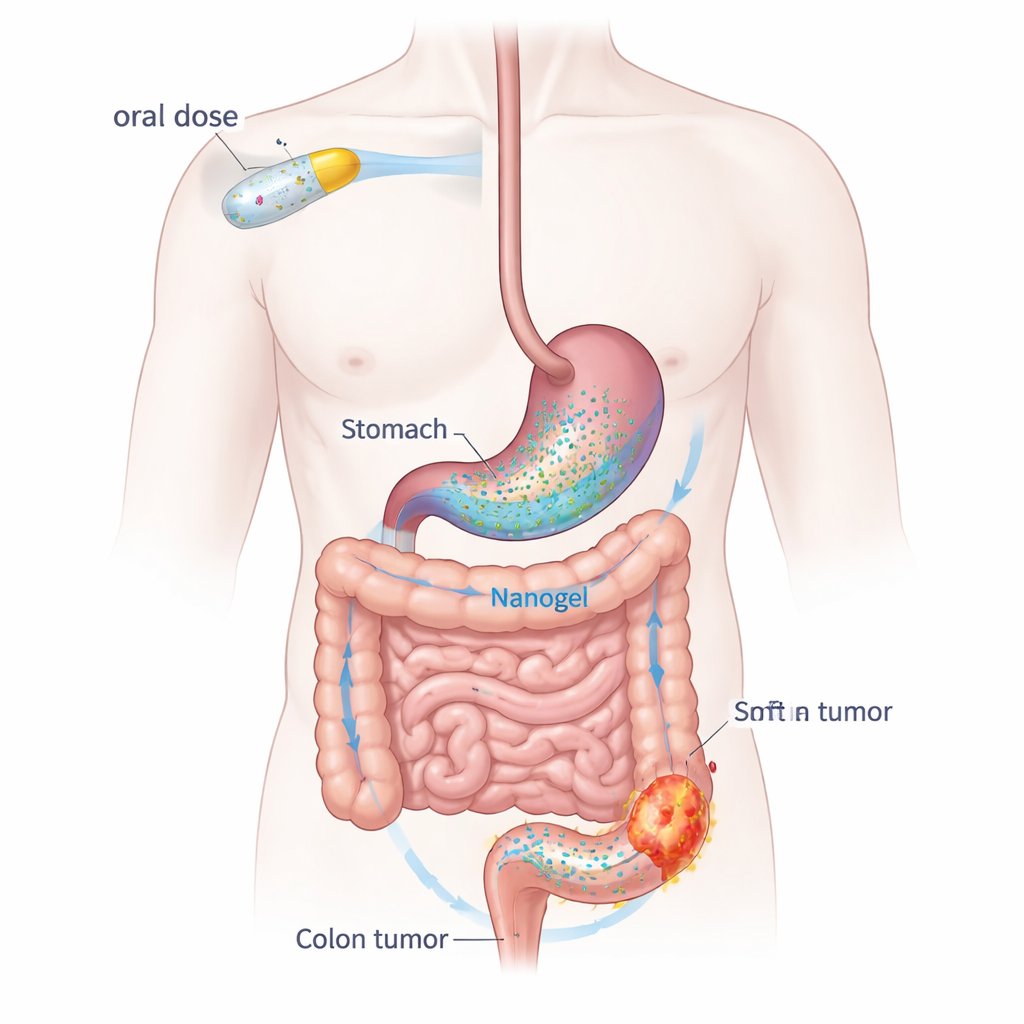
把日常药片变成靶向抗癌的载荷
达格列净通常在肾脏发挥降低血糖的作用,但它也具有抑制炎症和减缓细胞增殖的效果——这两种过程是癌症所依赖的。单独使用时,该药水溶性差且在体内清除较快。为克服这些问题,团队构建了一种“纳米凝胶”递送系统,使用两种类似食品的聚合物:从海藻中提取的海藻酸钠和广泛使用的生物相容性增稠剂聚乙烯醇。药物被困在直径约为千分之一毫米的纳米颗粒中。当这些颗粒遇到胃酸时,会沉降并相互结合成柔软的水凝胶团块,该凝胶停留并逐渐释放药物,随之向结肠移动。
提高药物溶解性并延缓洗脱
科学家首先优化了颗粒的制备方法,微调两种聚合物的比例,使纳米颗粒保持小尺寸、均一并在液体中稳定。他们确认药物被良好地嵌入聚合物网络中,并部分从晶体形态转为更无定形的形态,这通常有利于溶解。在模拟胃液和肠液的试验溶液中,纳米凝胶配方使达格列净的表观溶解度较原药提高约1.7–1.8倍。当监测药物释放速度时,纳米凝胶显示出数小时的温和“控释”曲线,而非原药的快速释放。一个称为F2的配方在酸性条件下能形成致密、耐久的凝胶,至少两小时内保持完整并稳定释放药物。
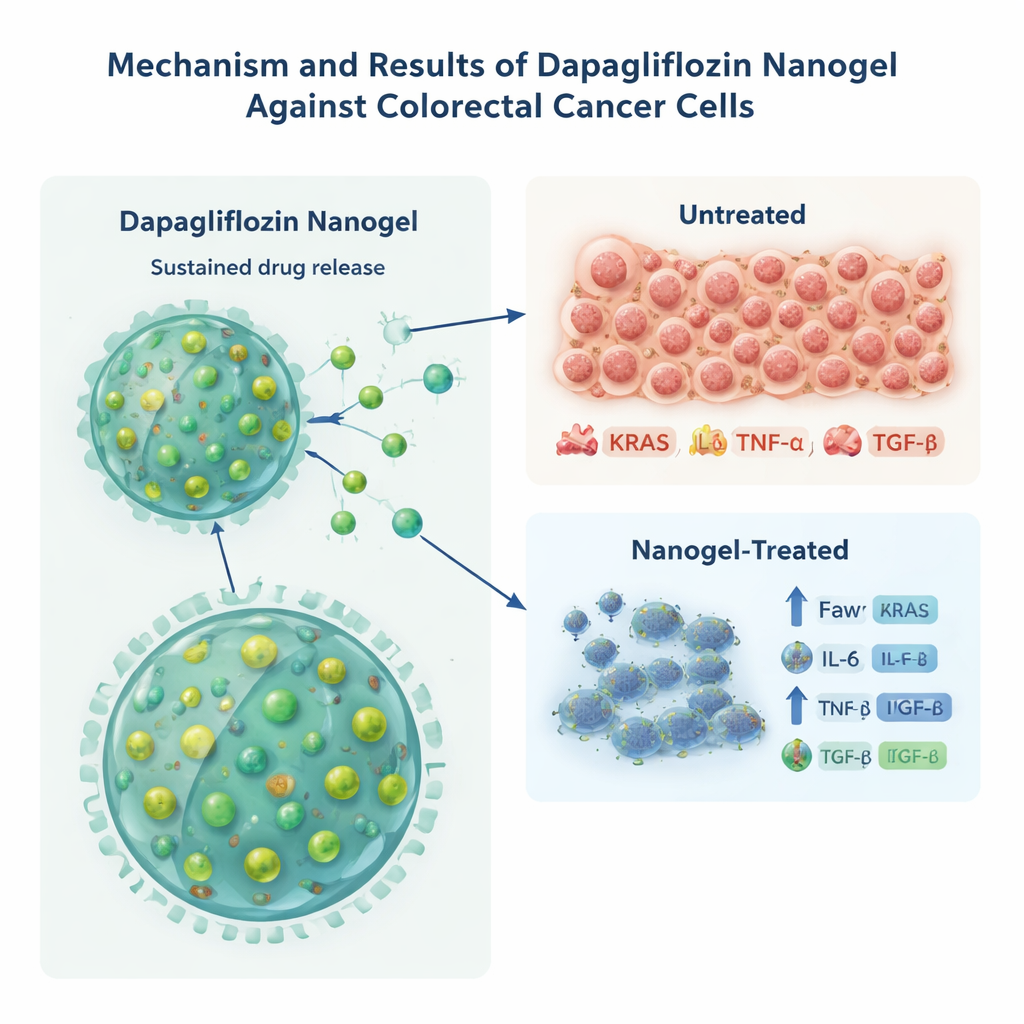
在体外使癌细胞承受压力
为评估这种新型达格列净是否能真正损害癌细胞,团队在培养皿中用HCT-116结直肠癌细胞进行了测试。与相同剂量的游离药物相比,纳米凝胶形式在较低浓度下即可杀死更多癌细胞,使抑制细胞增殖至一半所需剂量约降低三分之一。研究人员随后检测了与肿瘤侵袭性和慢性炎症相关的分子,包括驱动癌症的重要蛋白KRAS以及信号蛋白IL-6、TNF-α和TGF-β。用负载药物的纳米凝胶处理的细胞,这些标志物的水平明显低于用游离药物或空载颗粒处理的细胞,表明由纳米颗粒提供的持续暴露更有效地抑制了与癌症和炎症相关的信号。由于该细胞系已携带固定的KRAS突变,作者提醒这类KRAS蛋白下降可能反映的是应激反应而非直接的基因修复,但这仍支持了强烈的生物学效应。
改变机体对药物的处理方式
团队随后转入动物研究,给大鼠口服相同剂量的达格列净粉末悬浮液或优化后的纳米凝胶。在纳米凝胶组,血液中的峰值药物浓度出现得更晚且更低,但药物在循环中维持的时间更长。总体暴露量(以曲线下面积计)小幅增加约7%,表观半衰期大约翻倍。这些变化意味着机体看到的是更平缓、更持久的药物暴露,而不是剧烈的峰值后快速下降。这种行为与研究人员设计凝胶的初衷一致:在肠道中滞留药物、缓慢释放,并可能在下消化道和结肠(肿瘤发生处)维持较高的局部药物浓度。
这对未来癌症治疗可能意味着什么
通俗来说,这项研究将一种众所周知的糖尿病药物装备以新的“递送护甲”,使其更好地到达并滞留在结肠肿瘤附近。纳米凝胶使药物更易溶解、减缓其从肠道流失,并似乎提高了对结直肠癌细胞的毒性,同时下调了关键的炎症与生长信号。在大鼠中,它温和地延长了药物在血液中的存在时间,而并未大幅增加总体剂量。该工作仍处于早期阶段——仅限于一条癌细胞系和短期动物实验,尚未在活体动物或人中显示直接的肿瘤缩小效果。尽管如此,它为将达格列净重新定位为未来结直肠癌治疗的一部分奠定了详细基础,表明通过智能口服纳米凝胶可以把熟悉的药片转化为更具靶向性的抗癌工具。
引用: Abdullah, S., Thiab, S., Altamimi, A.A. et al. A repurposing Dapagliflozin via polymeric nanogels for colorectal cancer therapy. Sci Rep 16, 5625 (2026). https://doi.org/10.1038/s41598-026-36232-8
关键词: 结直肠癌, 药物重新定位, 纳米颗粒, 口服给药, 达格列净