Clear Sky Science · zh
泰国(2020–2024)全国范围内对耐碳青霉烯类和耐粘菌素的肺炎克雷伯菌血流分离株的基因组监测
致命的血液感染在增加
全球多家医院正面临一个令人不安的趋势:曾被我们最强效抗生素压制的常见细菌正变得几乎无法治疗。本研究聚焦于肺炎克雷伯菌,这种微生物可入侵血流并引发危及生命的感染,追踪其在泰国各地如何演化以抵御即便是最后一线药物。了解这些超级细菌的传播区域以及它们如何规避药物,对于保护患者、指导临床用药以及制定公共卫生政策至关重要。
追踪一种医院超级病原在全国的扩散
研究者分析了2020年至2024年间从泰国各地医院患者血液中分离出的227株肺炎克雷伯菌样本。这些样本来自一个常规收集耐药感染数据的全国监测网络。实验室检测显示,超过93%的血流分离株对碳青霉烯类——一种在其他药物失效时常被使用的强效抗生素——具有耐药性。更令人担忧的是,近三分之一的耐碳青霉烯株同时对粘菌素也表现出耐药性,而粘菌素常被视为医生在别无他法时的最后选择。通过将标准药敏检测与全基因组测序相结合,团队不仅能看到哪些药物失效,还能识别细菌为了生存而采用的遗传“伎俩”。
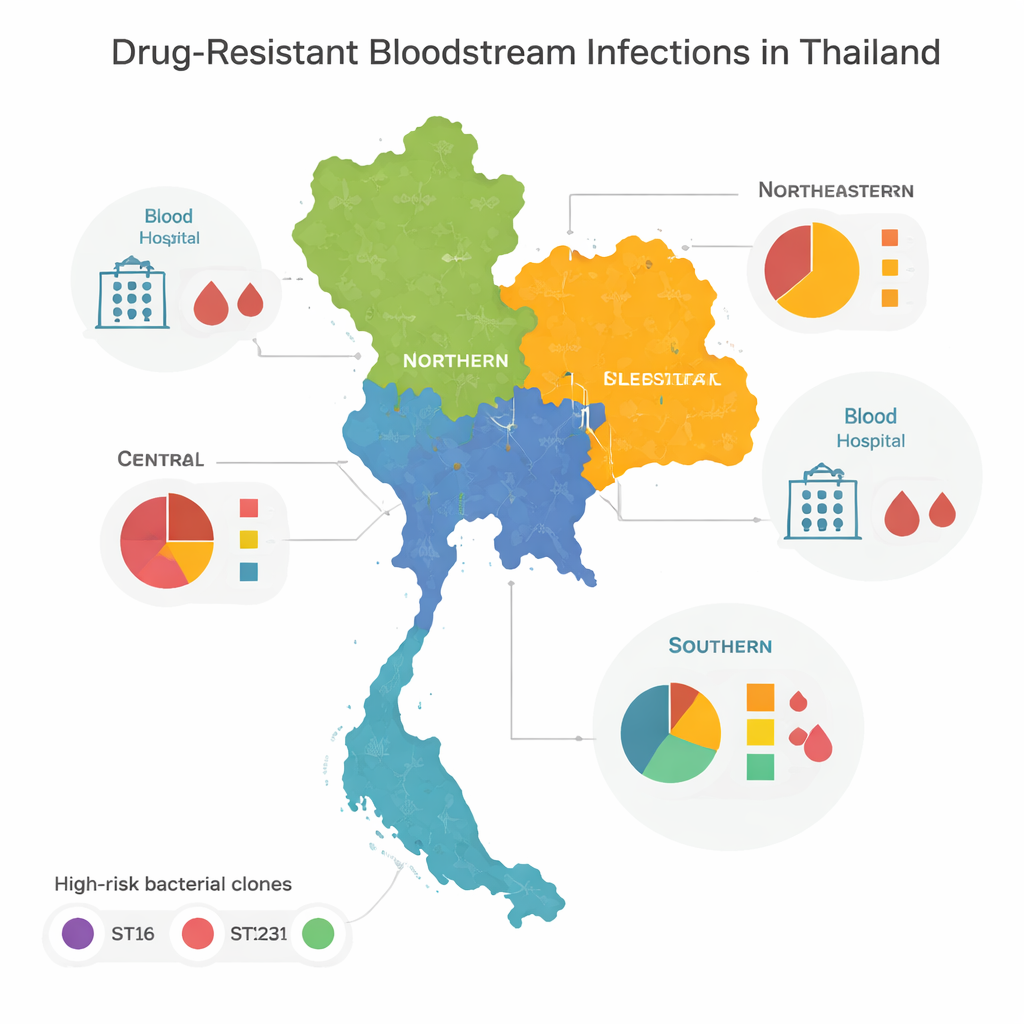
高危克隆与区域分布模式
当团队比较基因组时发现,大多数耐药细菌属于少数几个被全球公认为会在医院引发爆发的“高危”家族或克隆。尤其有三个——称为ST16、ST147和ST231——在泰国中部、北部和东北部占主导地位。这些克隆在各区域广泛传播,表明患者、医务人员或细菌在医院间频繁流动。南部情况则不同:那里并非由少数类型主导,而是存在多样化的细菌谱系,许多仅出现一次。这种多样性暗示出更复杂的局部爆发、环境来源和跨境流动的混合情形,而非一两株失控的克隆造成的单一扩散。
细菌如何智胜抗生素
研究揭示了这些细菌如何叠加多种耐药机制。许多ST16和ST231菌株携带称为blaNDM和blaOXA的基因,这些基因能产生酶,在碳青霉烯类抗生素发挥作用前将其分解。一些菌株还在外膜上发生改变,减少药物进入,二者结合导致非常高水平的耐药性。ST231菌株常携带另一个基因rmtF1,该基因能阻断一类重要药物——氨基糖苷类,从而进一步缩减治疗选项。ST147以其遗传灵活性著称:它能混合匹配不同的耐药基因和质粒(小而可移动的DNA环),使其成为将耐药特性传播给其他细菌的潜在枢纽。
最后防线的失守与隐匿的危险
最令人震惊的发现涉及对粘菌素的耐药性——这是一种医生在绝望情况下才会使用的药物。少数罕见的细菌家族携带可在物种间传播的mcr基因,这些基因位于质粒上并能直接导致对粘菌素的耐药性。其他菌株,尤其是ST16中的一些,即使缺乏任何已知的耐药基因或突变,也表现出对粘菌素的耐药性。这表明科学家尚未完全绘制出细菌中所有能中和这一最后用药的途径。团队还鉴定出高毒力菌株——即特别善于引发严重疾病的细菌——其中一个谱系同时兼具高度毒力和对所有检测碳青霉烯的耐药性,是一种尤其危险的组合。
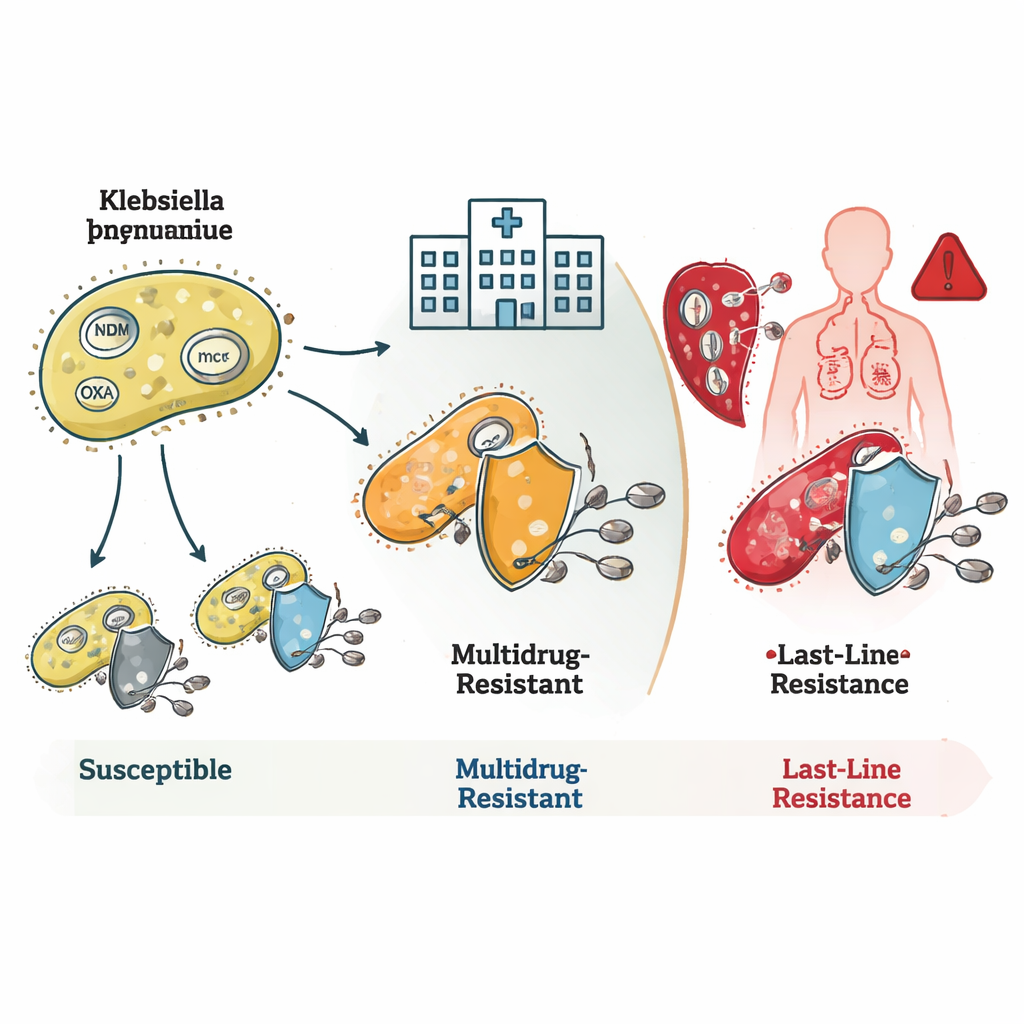
基因组监测为何重要
为了理解遗传变化如何转化为现实中的药物失效,研究者使用统计模型将特定耐药基因与实际实验室测试结果联系起来。诸如blaNDM-1及其近缘基因与碳青霉烯耐药性表现出极强的相关性,证实了它们在导致治疗失败方面的核心作用。然而对于粘菌素来说,大多数耐药细菌并未带有公认的耐药标记,这指出仍有待发现的隐匿机制。作者认为,在医院监测中常规使用全基因组测序可以像一种早期预警雷达,识别新兴的高危克隆、追踪它们在地区与国界间的移动,并指导快速的感染控制应对。
这对患者与政策意味着什么
对普通读者而言,信息既严峻又明确:泰国的一些血流感染现在由几乎能抵抗医生现有几乎所有药物的细菌引起,而某些危险菌群正在广泛传播。与此同时,研究表明,凭借合适的工具——全国性抽样、基因分析与快速数据共享——卫生系统可以预见这些威胁并做出调整。扩大基因组监测、开发快速分子检测并加强感染控制,有助于减缓这些超级细菌的扩散,为新疗法和疫苗的研发争取时间。
引用: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
关键词: 抗微生物耐药性, 肺炎克雷伯菌, 血流感染, 基因组监测, 泰国医疗保健