Clear Sky Science · zh
在脂肪源间充质干细胞分化为髓核样细胞过程中异常表达的长非编码RNA
为何背痛与隐匿的RNA重要
下腰痛是导致人们请病假或就医的主要原因之一,而其重要成因是脊椎骨之间缓冲软垫——椎间盘的渐进性退化。每个椎间盘内部都有一个凝胶状核心,称为髓核,它依赖一群健康的特化细胞来保持弹性和含水量。当这些细胞丧失或衰老时,椎间盘会脱水、塌陷,进而引发慢性疼痛。科学家正在探索是否可以引导干细胞——一种能分化为多种组织的多能细胞——来替代这些损耗的髓核细胞。本研究提出了一个出人意料但基础的问题:当干细胞被诱导成为新的椎间盘细胞时,哪些“沉默”的遗传信号会被激活?如何利用这些信号来改善未来的治疗?
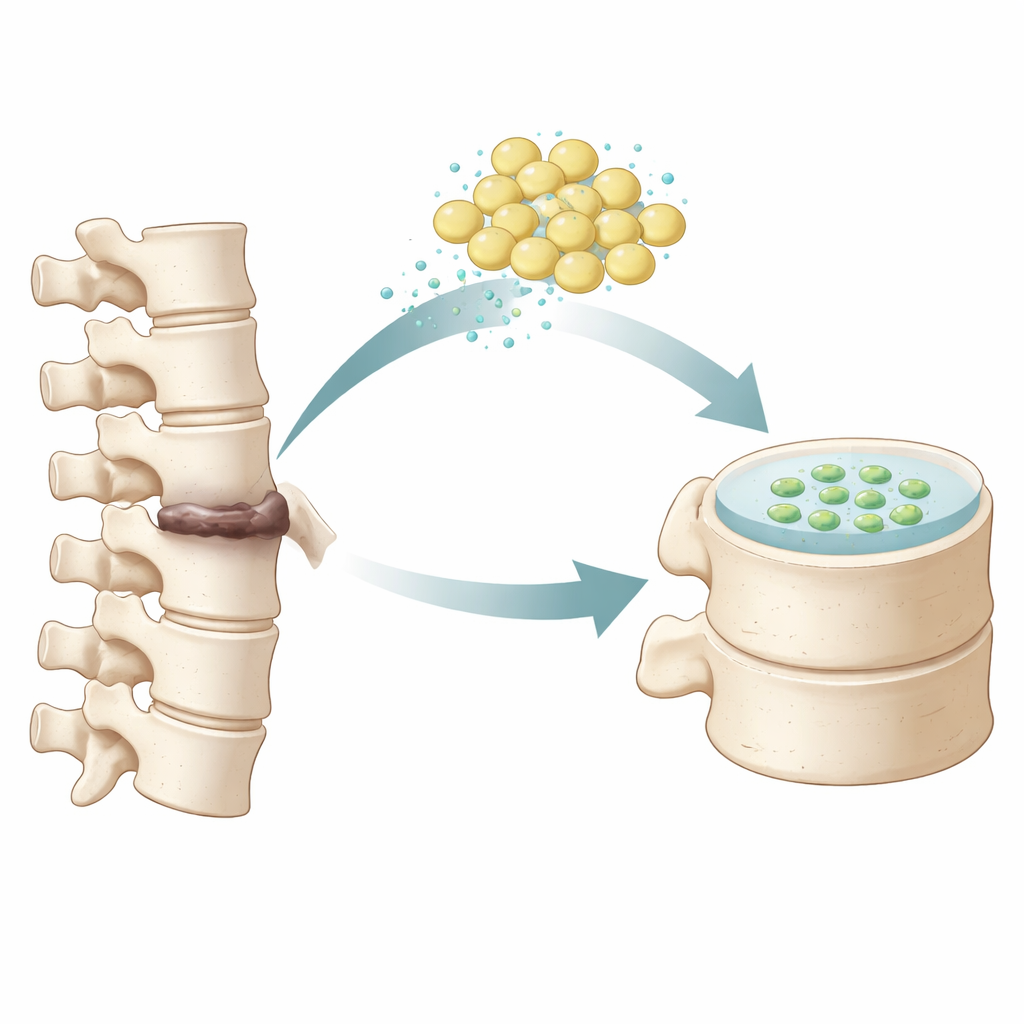
从脂肪组织到椎间盘修复
研究人员聚焦于来自人体脂肪的间充质干细胞,这类细胞较易获得。在体外,他们将这些细胞培养成小的三维颗粒,并用先前研究发现能促使细胞朝髓核样表型转变的一组生长因子进行处理。数周内,团队用常规显微染色和荧光标记对颗粒进行监测。经处理的细胞开始在形态和功能上更接近健康椎间盘的凝胶核心细胞,产生诸如胶原和聚聚蛋白(aggrecan)等椎间盘组织的标志性成分,并激活与髓核身份相关的关键基因。
倾听细胞的“背景喧嚣”
除了常见的蛋白编码基因外,细胞还产生长非编码RNA——不编码蛋白但能微妙调控基因开关的RNA片段。这些分子正逐渐被认作细胞分化过程中的重要指挥者。研究团队利用高通量RNA测序同时测量了在向椎间盘样方向分化的干细胞中以及未分化对照细胞中的信使RNA和长非编码RNA。他们发现基因活动图谱发生了广泛重塑:约有500条长非编码RNA和601条信使RNA的表达发生变化,其中一些上调,另一些下调,随着细胞向髓核样状态转变而改变。
关键通路与主控调节因子
为理解这份冗长的变化清单,科学家们使用生物信息学工具将基因按其细胞功能进行分组。许多改变的基因与细胞外基质的构建与组织有关——即由胶原、糖类及其他分子组成,使椎间盘具备缓冲性能的网状结构。通路分析突出显示了PI3K–Akt信号通路和控制细胞骨架的系统在分化过程中尤其活跃,提示这些回路可能推动脂肪源干细胞向椎间盘样细胞的转变。通过构建相互作用网络,团队识别出一组位于调控RNA、信使RNA与微小RNA之间通信中心的长非编码RNA,包括MALAT1、MEG3、GAS5、ZNF331及与JARID2关联的RNA。这些中心节点可能作为主开关,控制干细胞承诺为椎间盘样命运的效率。
为更好的干细胞疗法提供线索
椎间盘退变产生的环境尤为不利——酸性、低氧并富含炎性分子——这会挫伤移植的干细胞。通过绘制在体外成功将脂肪源干细胞转化为髓核样细胞过程中发生变化的RNA与通路,本研究提供了一份分子靶点目录,可能用于调节以提升治疗性细胞在真实患者体内的存活与功能。尽管该研究在体外并且样本量有限,但它为未来实验奠定了基础,例如通过调整特定长非编码RNA或信号通路来增强椎间盘再生。
这对背痛患者意味着什么
对长期受下腰痛困扰的人来说,这些发现不会在明天改变临床治疗,但它们补齐了一个关键的缺失环节:干细胞如何学习成为用于修复的精确类型的椎间盘细胞。研究表明,这一转变不仅由已知基因引导,还受一张复杂的长非编码RNA与信号通路网络的塑造。解码这一隐蔽的调控层将使科学家更接近设计出更智能的干细胞疗法,使其更能抵御受损椎间盘的恶劣环境并更可靠地重建其缓冲核心,未来有望为患者带来更持久的缓解。
引用: Zhu, J., Jin, L., Jin, K. et al. Aberrantly expressed long noncoding RNAs in adipose-derived mesenchymal stem cells differentiation to nucleus pulposus-like cells. Sci Rep 16, 8029 (2026). https://doi.org/10.1038/s41598-026-36219-5
关键词: 椎间盘退变, 干细胞治疗, 髓核细胞, 长非编码RNA, RNA测序