Clear Sky Science · zh
用于线粒体靶向光动力治疗的吡啶鎓和溴取代二苯乙烯-BODIPY 染料
从内部点亮癌细胞
光动力疗法是一种利用光激活药物选择性杀死肿瘤细胞且在很大程度上保留健康组织的癌症治疗方法。本研究探讨了一类新型荧光染料,旨在定位到细胞的能量工厂——线粒体,并在用深红光照射时产生有毒的活性氧物种以摧毁癌细胞。该工作展示了在分子层面设计这种染料所带来的潜力与挑战。
为什么要靶向细胞的能量站?
线粒体在能量产生中至关重要,并参与决定细胞生存或死亡。癌细胞的线粒体膜通常比正常细胞带有更高的膜电位,这使它们对带正电的分子的累积更为敏感。研究者利用这一点,将带正电的吡啶鎓基团连接到一种知名的荧光染料骨架 BODIPY 上。这一设计有助于将染料引导进入线粒体,在那里光触发的化学反应可以对癌细胞造成最大损伤,同时限制对其他部位的危害。
设计更智能的光激活染料
团队合成了三种彼此紧密相关的染料,命名为 PyBHI、PyBMI 和 PyBBrI,主要区别在于所携带溴原子的数量(无、一个或两个)。它们都具有很长的共轭结构,使它们的光吸收和发射移至近红外区——这是光可以更深穿透组织的有用波段。理论上,这些染料可以通过两种不同的内在途径到达产生反应性单线态氧的“三重态”激发态:一种由重原子(溴)驱动,另一种由分子内临时的电荷转移驱动。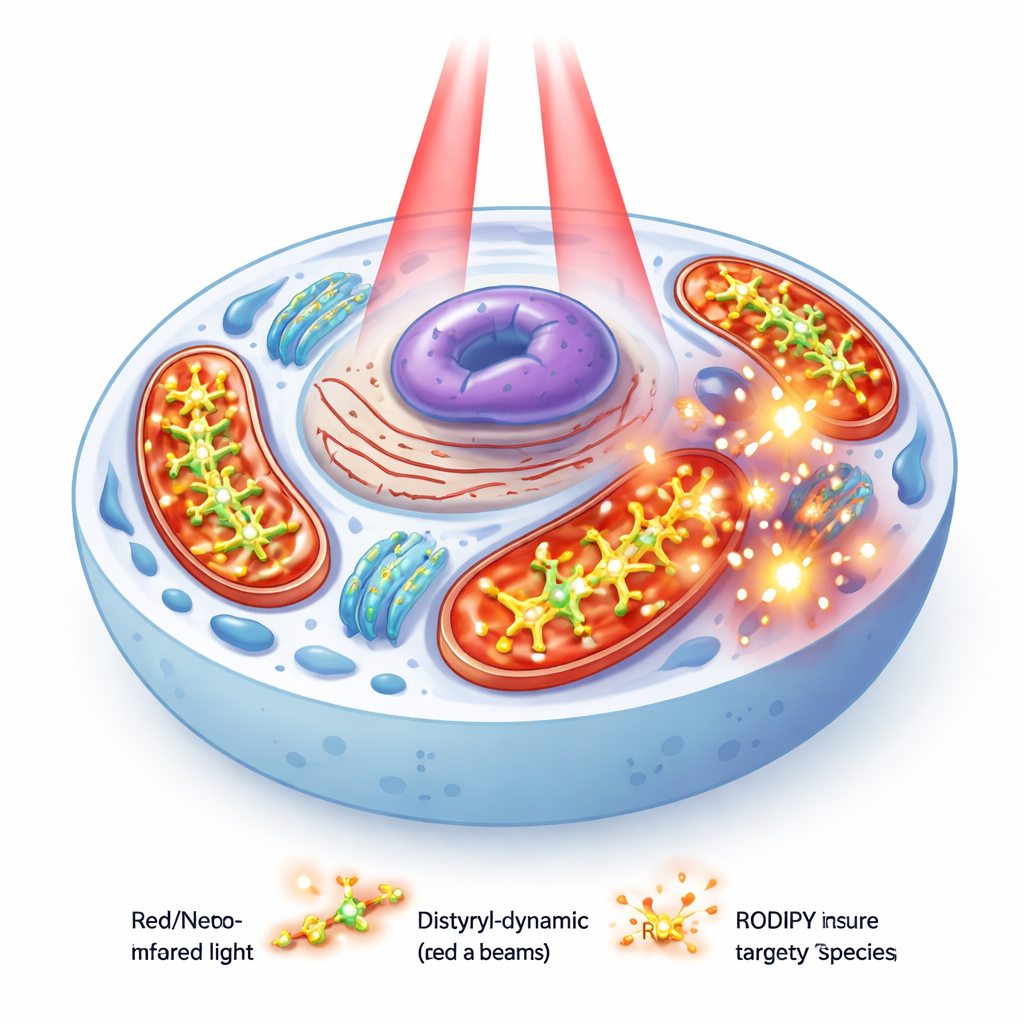
理论与实验现实的碰撞
尽管理论设计优雅,细致的测试表明这些染料产生单线态氧的效率并未达到预期。研究者使用会在与单线态氧反应时失去颜色的化学探针,测得三种染料的产氧量都非常低,随着溴原子增多仅有温和的改善。飞秒激光实验揭示了原因:在吸光后,染料迅速进入电荷转移态,这些态大多以热能无害地弛豫,而不是转化为期望的三重态。在溴化版本中,重原子确实为通往三重态打开了一条通路,但这一路径比竞争性的能量损失慢得多,从而限制了总体效率。
在活细胞中靶向肿瘤线粒体
在生物环境中情况发生了变化。在培养的人乳腺癌(MCF-7)和宫颈癌(HeLa)细胞中,共聚焦显微镜显示三种染料都强烈积累于线粒体,并与标准线粒体染色共定位。暗态毒性测试表明,在无光照条件下这些染料基本无害。然而在红光照射下,二溴化染料 PyBBrI 导致了大量癌细胞死亡,低纳摩尔剂量即可将细胞活力降至一半。其他两种染料则效果较差。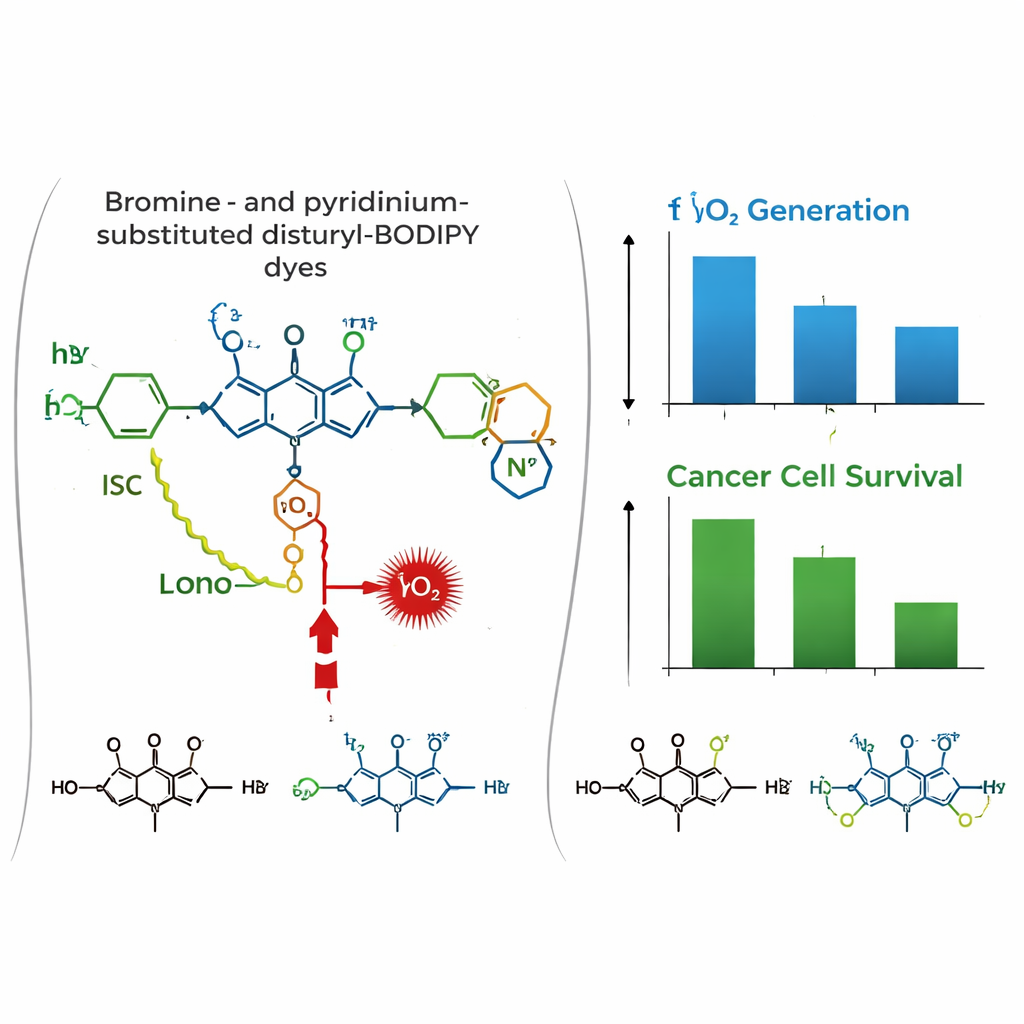
这对未来癌症治疗意味着什么
对非专业读者来说,关键结论是:微小的化学修饰可以极大地改变光激活抗癌药物的行为,并且它们在真实细胞中的表现可能优于或劣于由基础测量所预测的结果。在本例中,改造最严重的染料 PyBBrI 在试管中仅显示出有限的活性氧产生,但一旦到达线粒体便对癌细胞表现出高度效力。这项工作强调了将药物定向递送到癌细胞内部易受攻击结构的重要性,同时也凸显了预测光动力效率的复杂性。它为下一代线粒体靶向疗法指明了方向,这类疗法利用近红外光在恰当的位置选择性“开启”杀伤细胞的化学反应。
引用: Kim, C., Badon, I.W., Jo, J. et al. Pyridinium- and bromine-substituted distyryl-BODIPY dyes for mitochondria-targeted photodynamic therapy. Sci Rep 16, 6789 (2026). https://doi.org/10.1038/s41598-026-36213-x
关键词: 光动力疗法, 线粒体靶向染料, BODIPY, 单线态氧, 癌细胞