Clear Sky Science · zh
γ辐射在猪脑中诱发与肌萎缩侧索硬化症和额颞叶痴呆相关标志物的区域性亚细胞改变
为什么微量辐射和猪脑很重要
大多数人把辐射视为纯粹有害,尤其对大脑而言。然而,我们周围充满了来自医学扫描、航空旅行和环境的低剂量辐射。与此同时,科学家仍在探索导致肌萎缩侧索硬化症(ALS,致使棒球明星卢·盖里格瘫痪的致命疾病)及其近亲额颞叶痴呆(FTD,侵袭行为与个性)的原因。本研究提出了一个出人意料但充满希望的问题:一次适度的γ射线低剂量照射,是否会以并非纯粹损伤的方式,微妙地重塑大脑化学,并可能在分子层面上对抗与ALS和FTD相关的改变?
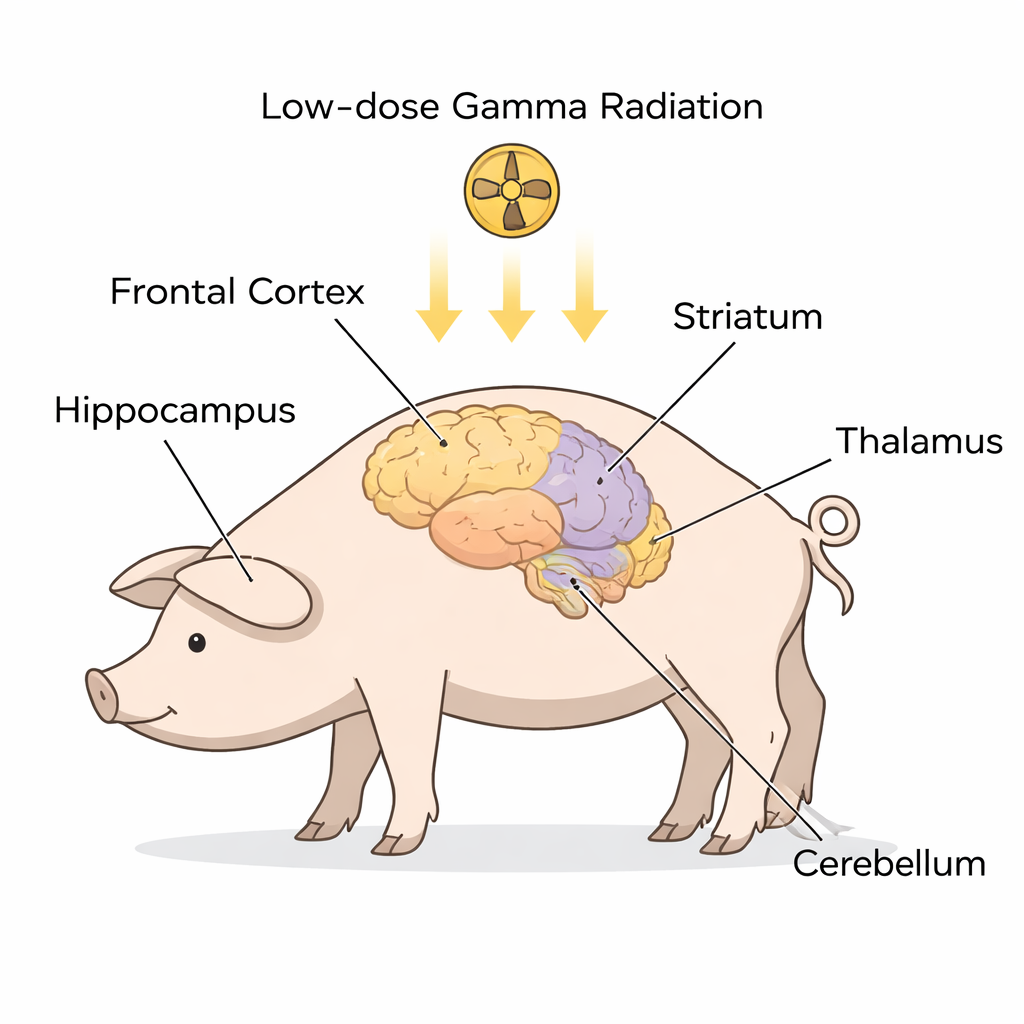
更近距离地观察大脑中ALS的警示信号
研究者没有检查已患ALS的患者,而是使用了解剖结构与人类相似的哥廷根小型猪。九只动物接受了一次性全身低剂量γ辐射暴露,另有六只在麻醉状态下未照射,作为对照。约一个月后,科学家解剖了五个在ALS和FTD中常涉及的关键脑区——额叶皮层、海马、纹状体、丘脑/下丘脑和小脑。在每个区域,他们将细胞内容物分为两个主要隔室:细胞质(细胞的流体内腔)和细胞核(包含DNA的隔室)。通过西方印迹(Western blot)技术,他们测量了与ALS及ALS‑FTD密切相关的若干蛋白水平,包括SOD1、FUS、C9orf72、STMN2、泛素、TDP‑43及其磷酸化形式。
辐射令一些标志维持不变——另一些则发生转移
一个令人宽慰的发现是,总量SOD1(某些遗传性ALS由其突变引起)在任何脑区均未因辐射而改变。同样,TDP‑43的主要形式——这一蛋白最常见于ALS相关的大脑斑块中——在所有区域的细胞核和细胞质中均保持稳定。但并非一切都静止不变。研究组观察到若干其他蛋白在特定区域和特定隔室中发生了变化。例如,FUS(一种通常位于细胞核、在ALS中可发生功能异常并聚集的蛋白)在丘脑/下丘脑的细胞质中减少,而在额叶皮层的核内水平升高,在海马的核内水平则下降。与ALS相关的C9orf72在细胞质中未见变化,但在海马细胞核内出现下降。维持神经纤维的重要蛋白STMN2也在海马核内下降,提示在这一与记忆相关的区域,这两种分子可能存在协同反应。
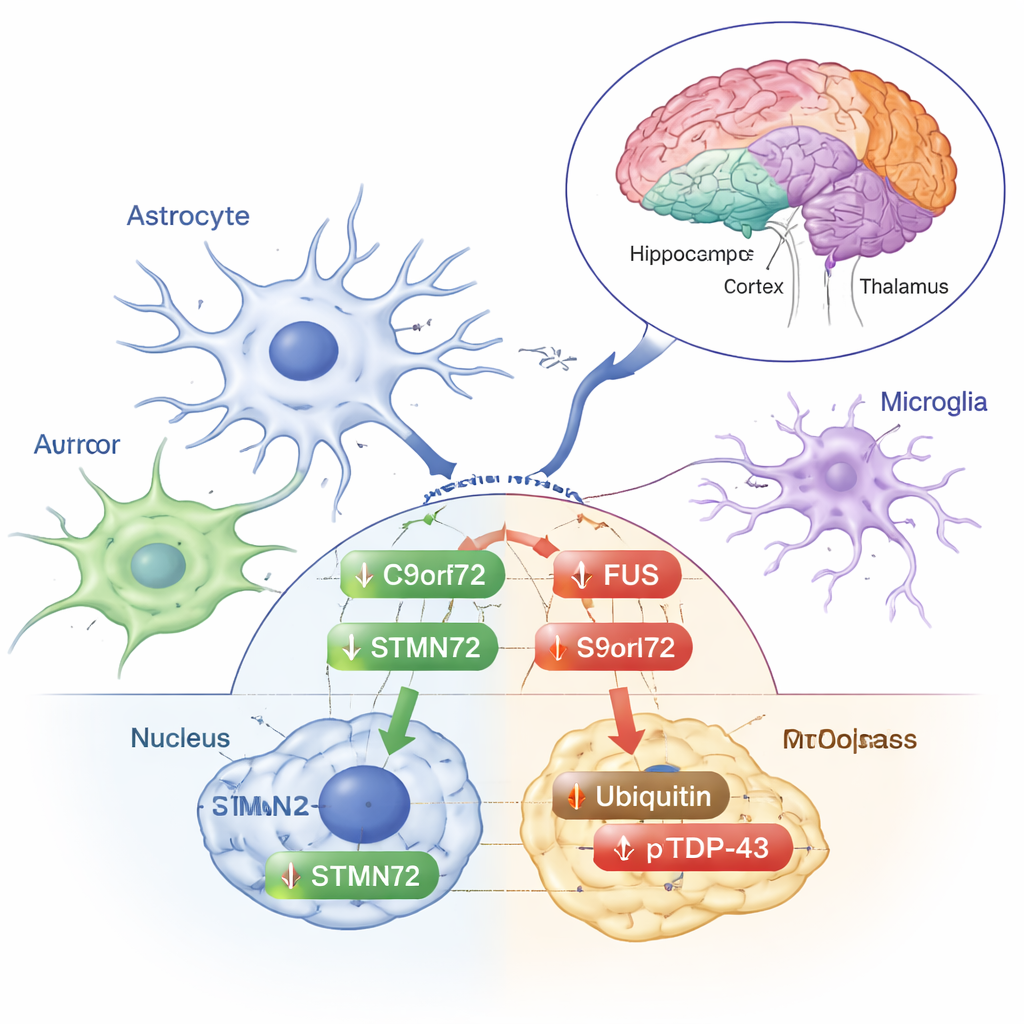
应激信号还是早期保护?
其他变化更像是经典的应激反应。泛素——细胞用来标记受损蛋白以便清理的小标签——在额叶皮层的细胞质分馏中增加。TDP‑43的磷酸化形式(常见于ALS和FTD中异常沉积物)在额叶皮层、纹状体和丘脑/下丘脑的细胞质中升高,即便总量TDP‑43并未变化。这些变化表明,低剂量辐射在不触发定义疾病的全面错误折叠和聚集模式的情况下,轻微推动了大脑的蛋白质处理机制。作者强调,这些反应随脑区和蛋白是否位于细胞核内外而异,凸显了大脑对应激反应的精细调节性。
这对ALS风险——以及可能的益处——意味着什么
这是否意味着低剂量辐射会导致ALS?数据并不支持简单的肯定。研究者未见到主要ALS蛋白的典型错误定位或堆积,许多变化更指向调控的改变而非明确的损伤。有趣的是,这些结果与同一研究组和其他团队早期的工作相符,即少量辐射有时可触发“调节性激励”(hormesis)——即轻度应激激活修复通路并在动物模型中降低与阿尔茨海默或帕金森病相关的有害蛋白。本研究提示,至少在短期内,一次低剂量γ辐射能以可能为适应性而非破坏性的方式重塑与ALS相关的标志物。
重大问题与谨慎的希望
对非专业读者而言,关键结论是辐射与大脑健康之间的关系比“所有辐射都是有害的”更为复杂。在这一大型动物模型中,低剂量γ照射在不复制患者大脑中损伤性模式的情况下,产生了与ALS和FTD相关蛋白的细微、区域特异性变化。这些变化可能反映大脑应对并修复应激的尝试,在某些情况下甚至可能有益。然而,该研究仅在单次暴露后一个月内观察,且仅限于大脑(未包括ALS最严重受累的脊髓)。在考虑将此类发现转译到人类之前,还需要长期和重复剂量的研究。尽管如此,这项工作为日常水平的辐射如何与导致毁灭性神经退行性疾病的分子相互作用打开了一扇新窗——并提出了一个可能性:在严格控制的条件下,小剂量或许有朝一日能被用于激发大脑自身的防御机制。
引用: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
关键词: 肌萎缩侧索硬化症, 额颞叶痴呆, 低剂量辐射, 脑蛋白, 小型猪模型