Clear Sky Science · zh
FcIgG-GE11-蜂毒素作为一种新型针对EGFR的肽体,对癌细胞具有强效细胞毒活性
蜂毒与精准癌症疗法相遇
许多有前景的抗癌药物对机体其他部分来说过于毒性强,难以安全使用。一个鲜明的例子是蜜蜂毒液中的主要毒素——蜜蜂毒素(melittin):它能撕裂癌细胞,但也会损伤红细胞和健康组织。本研究探索了一种巧妙的变通方法——构建一种“制导导弹”,将蜜蜂毒素直接运送到在表面表达特定标志的肿瘤细胞,同时在很大程度上保护正常细胞。
为何靶向一种常见的癌症开关
许多肿瘤的重要参与者是一种称为表皮生长因子受体(EGFR)的分子。该受体位于细胞表面,帮助调控生长和存活。在包括肺癌、结直肠癌、前列腺癌以及部分头颈癌和肾癌等多种癌症中,EGFR的过度表达会驱动失控的细胞分裂。因此,能结合EGFR的药物已成为一类重要的靶向疗法。然而,现有的EGFR药物主要是阻断信号传导;它们并不主动破坏癌细胞。研究者提出,是否可以利用蜜蜂毒素强大的细胞溶解能力,并将其选择性地递送到富含EGFR的肿瘤细胞。
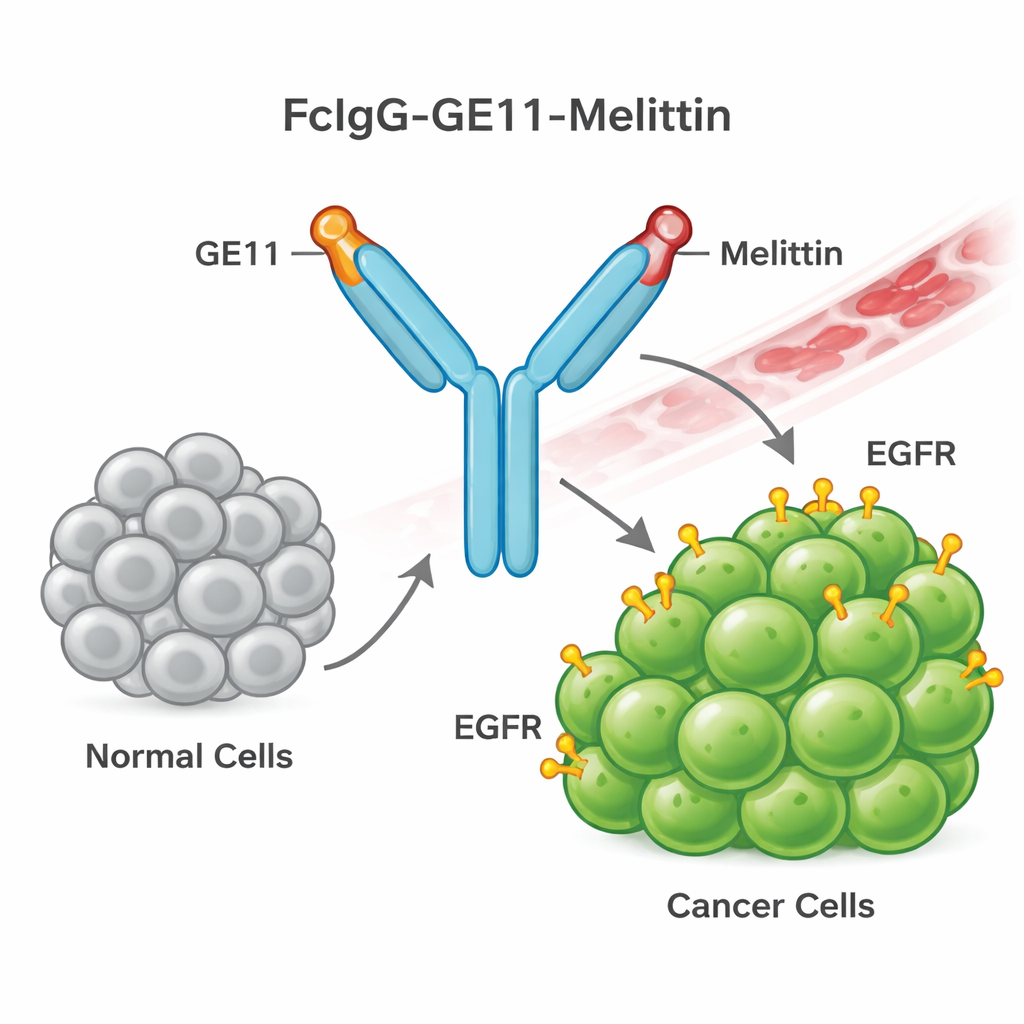
构建一种制导蜂毒武器
为此,研究团队设计了一种称为FcIgG-GE11-Melittin的新型融合蛋白。它由三部分组成:一段抗体“尾部”(人IgG的Fc区),可提高血液中稳定性并便于纯化;一段识别并结合癌细胞EGFR的短制导肽GE11;以及能破坏细胞膜的蜂毒肽melittin。研究者通过工程化细菌大量表达该融合蛋白,并对蛋白进行复性和纯化。体外检测证实该蛋白形成预期的二聚体结构并带有人类抗体标签,表明构建正确。
锁定肿瘤细胞,而非任意细胞
接下来的问题是这种设计分子是否真的能识别并黏附在富含EGFR的癌细胞表面。研究者使用流式细胞术在已知高表达EGFR的A549肺癌细胞上检测结合情况。经FcIgG-GE11-Melittin处理的细胞显示出荧光显著增加,说明大量融合分子附着在细胞表面。作为阴性对照的无关肽体Romiplostim几乎没有结合。新型构建体的结合谱与知名的EGFR抗体Cetuximab非常接近,这支持GE11成分正确地将融合蛋白引导至其靶标的观点。
杀死癌细胞同时保护血细胞
团队随后测试了该融合蛋白在培养条件下对不同癌细胞系的杀伤效果。游离的melittin本身极具效力但缺乏选择性,在低剂量下即可显著降低肺(A549)、前列腺(DU145)和结直肠(SW480)癌细胞的存活率。相比之下,FcIgG-GE11-Melittin呈剂量依赖性杀伤作用,在EGFR阳性细胞中最为明显,而EGFR表达较低的乳腺癌细胞系(MDA-MB-453)则相对耐受。这一模式表明融合构建体的攻击依赖于EGFR靶向,而非随机的膜破坏。更重要的是,在与人红细胞的实验中,游离melittin在适中剂量即可引起几乎完全的溶血,而融合蛋白即使在非常高浓度下也仅导致不到5%的溶血。换言之,将melittin连接到寻EGFR的载体上,大幅降低了其裂解红细胞的倾向。
这对未来癌症治疗意味着什么
总体来看,这项工作表明,将像melittin这样强效的膜破坏毒素与精确的靶向系统耦合,可以把它从一种广谱毒性物质转变为更具肿瘤选择性的武器。FcIgG-GE11-Melittin能强烈结合EGFR过表达的癌细胞,以可控的、剂量依赖的方式杀灭它们,并在体外对红细胞造成的损伤甚微。尽管在临床应用前仍需进一步的动物研究和安全性检测,这一策略展示了如何通过重新工程化天然毒素为制导疗法,开辟治疗EGFR阳性肿瘤的新途径,且有望减少副作用。
引用: Hallaji, M., Fayaz, S., Allahyari, M. et al. FcIgG-GE11-Melittin as a novel EGFR targeted peptibody with potent cytotoxic activity against cancer cells. Sci Rep 16, 7047 (2026). https://doi.org/10.1038/s41598-026-36167-0
关键词: 靶向癌症治疗, EGFR, 蜂毒素蜜蜂毒素(melittin), 肽体, 肿瘤选择性毒素