Clear Sky Science · zh
推定的长程苔藓纤维再生与海马区域细胞色素c氧化酶改变在内侧颞叶癫痫患者中的表现
当癫痫重塑大脑的记忆中心
内侧颞叶癫痫(MTLE)是最顽固的癫痫类型之一,常对药物抵抗,并在患者最具生产力的年龄剥夺记忆与独立性。本研究深入观察大脑的记忆枢纽——海马,探查癫痫发作活动如何在结构上重连其回路并改变脑细胞的能量利用方式,进而揭示癫痫持续的原因,并为外科医生与未来疗法提供更精准的靶向线索。
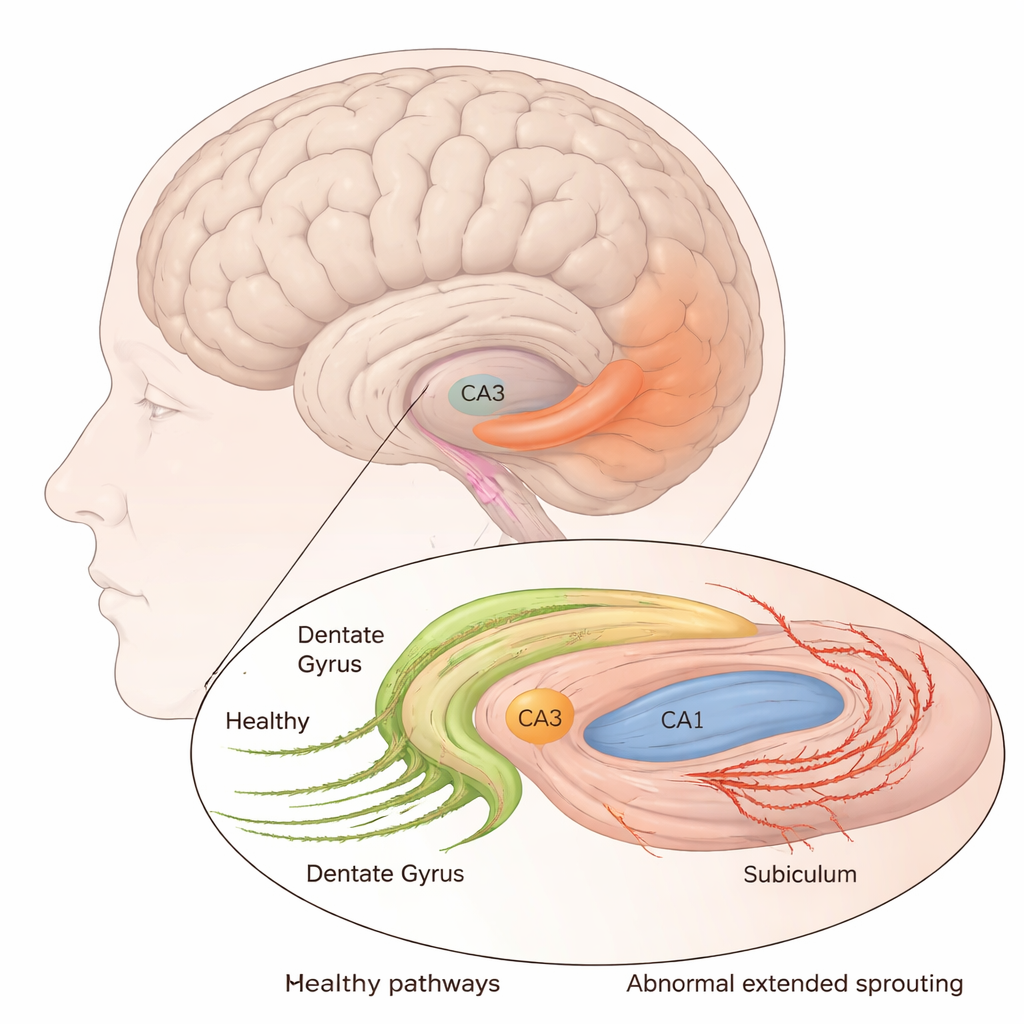
问题核心的大脑区域
在MTLE中,癫痫发作通常源自海马——一个呈马首状、对形成新记忆至关重要的结构。许多患者出现“海马硬化”,即关键神经元群体死亡并由胶质组织瘢痕化。作者检查了20例因药物难治性MTLE而外科切除的海马样本,并与20例非癫痫捐献的大脑进行比较。他们聚焦于齿状回(海马的入口)、称为CA3、CA2、CA1的区域,以及一个邻近的输出区——下丘(subiculum)。通过一组分子染色,他们能够计数存活神经元、追踪称为苔藓纤维的特定神经纤维束,并测量细胞能量工厂(线粒体)中一种主要能量生成酶的活性。
丧失的神经元与混乱的细胞层
首先,团队证实了MTLE中经典的损伤模式。在外科样本中,齿状丛(dentate hilus)以及CA3和CA1区的许多神经元缺失,部分损失延伸到CA2和下丘。齿状回中原本整齐的细胞排列被打乱:颗粒细胞扩散并甚至形成岛状簇,这一现象称为颗粒细胞弥散。两种独立的神经元标记显示了相同的情况——海马回路中关键中继站严重变薄,而像CA2和部分下丘等一些区域相对幸存,但结构上仍显紊乱。
延伸超出预期的再生纤维
最显著的变化涉及苔藓纤维——齿状颗粒细胞的轴突,正常情况下它们在海马内形成短程连接。使用三种不同标记,研究者发现这些纤维不仅向邻近层(内分子层)再生,这是癫痫的已知特征,而且似乎延伸得比通常更远。在MTLE组织中,内分子层变宽并呈强烈染色,而原始苔藓纤维所在的齿状丛和CA3区信号大量丧失,表明这些部位轴突减少。与此同时,一条被标记的纤维纤维带从CA2区穿过收缩的CA1并延伸到下丘。该模式在多种标记下均可观察到,提示幸存的苔藓纤维可能发生长程投射,潜在地创建连接海马“入口”与其主要输出区的新型异常通路。
过度活跃网络中的能量热点
癫痫发作是强烈电活动的爆发,需要大量能量。为评估MTLE中局部代谢如何改变,作者对线粒体能量生成的核心酶——细胞色素c氧化酶进行了染色。与对照脑相比,MTLE海马在已受损的CA1区显示出酶标记减少,但在内分子层与下丘显示出标记增加。换言之,接收再生苔藓纤维的那些区域也似乎处于“高温”运行,具有更高的代谢能力。这种结构重连与能量使用升高的并存,支持了这些区域可能形成维持或传播癫痫的过度活跃枢纽的观点,即便原有大部分回路已退化。
对难治性癫痫患者的意义
对非专业读者而言,信息是:MTLE不仅仅是海马中组织坏死的问题;它也是幸存神经细胞发出新的、可能误导的连接以及某些区域成为代谢热点的故事。研究表明,苔藓纤维可能从齿状回形成比正常更长的通路,通向CA1和下丘,这些重排的通路可能助长药物难治患者中持续的癫痫发作。通过绘制新的连线图与能量分布图,该工作提示了未来策略——从更精细的手术靶点到针对这些过度活跃通路的新型干预——有朝一日或可在尽量保留健康记忆回路的同时控制癫痫发作。
引用: Tu, T., Wan, L., Zhang, QL. et al. Putative long range mossy fiber sprouting and regional cytochrome c oxidase alteration in the hippocampus of patients with mesial temporal lobe epilepsy. Sci Rep 16, 5232 (2026). https://doi.org/10.1038/s41598-026-36148-3
关键词: 颞叶癫痫, 海马, 苔藓纤维再生, 神经元丧失, 大脑代谢