Clear Sky Science · zh
氟喹诺酮骨架上R5和R7位点驱动F-肌动蛋白丝的破坏
把抗生素变成大脑助手
许多常见的脑部疾病,从阿尔茨海默病到帕金森病,都有一个隐蔽的元凶:神经细胞内部的微小结构棒状体随时间变得卡滞和僵硬。这些棒状体由一种名为肌动蛋白的蛋白质构成,肌动蛋白通常是细胞内部支架的灵活组成部分。本研究探索了一个出人意料的可能性——一种广为人知的抗生素类别氟喹诺酮,经过重新设计后,可能温和地拆散这些有害的肌动蛋白束,从而潜在地保护大脑。
当细胞支架出问题时
健康的脑细胞不断重塑其内部骨架以形成和改造连接。肌动蛋白丝在此过程中起关键作用,按需形成和解体。然而在应激下,肌动蛋白可能锁定为顽固的棒状聚集体,堵塞细胞、扰乱重要货物的运输,并促进与疾病相关蛋白(如淀粉样蛋白和tau)的堆积。多年累积后,这些棒状体可成熟为称为Hirano体的致密结构,常见于多种神经退行性疾病患者的大脑中。由于现有针对肌动蛋白的药物往往毒性极高,研究者迫切希望找到更安全的小分子,能在不损伤细胞的情况下松散这些聚集体。
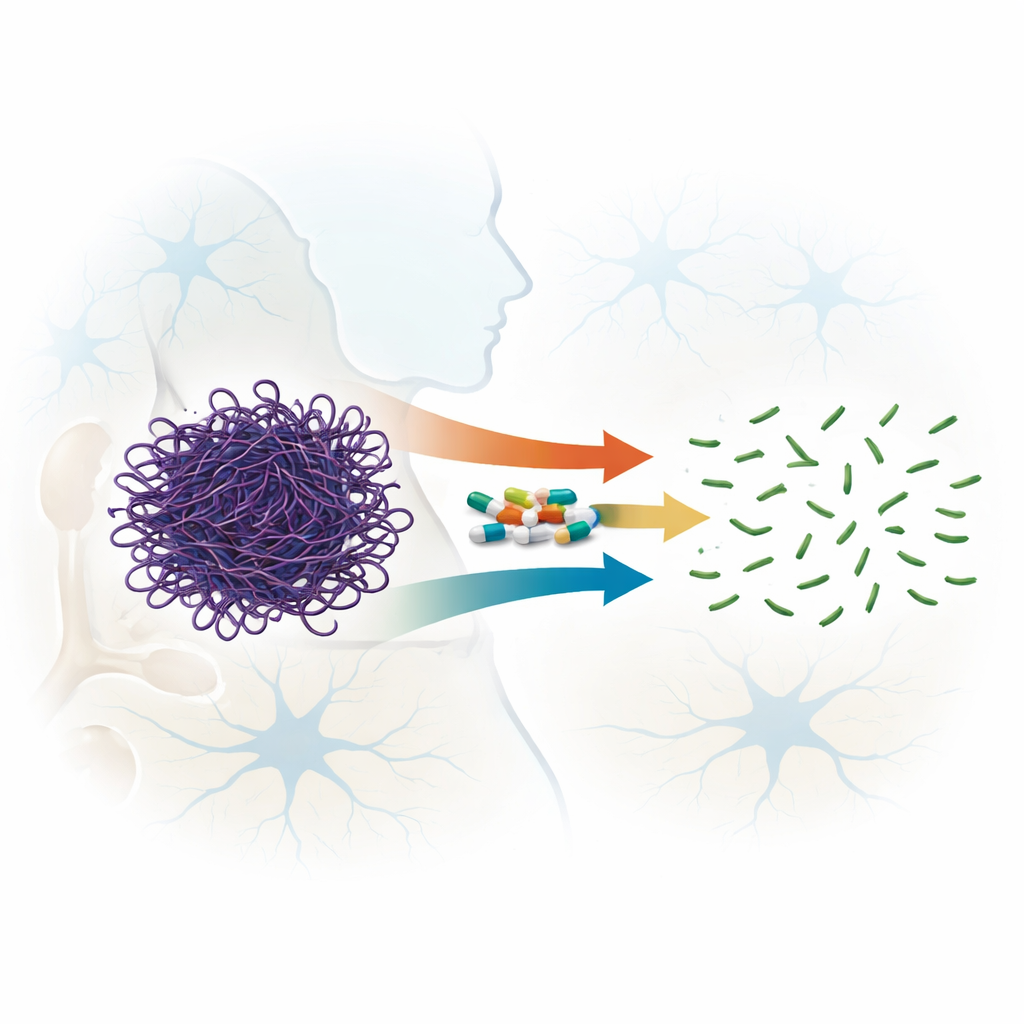
熟悉药物的意外特长
氟喹诺酮是用于治疗感染的广谱抗生素,该类一些较新的成员能穿过血脑屏障。早期线索显示某些氟喹诺酮可以使肌动蛋白丝不稳定。在这项工作中,作者系统比较了七种相关化合物,覆盖该药物家族的四代成员,以评估它们在破坏预先形成的肌动蛋白丝(而不仅仅是阻止其形成)方面的能力。通过光散射测量、电子显微镜和凝胶过滤,他们表明所有被测试药物都能干扰肌动蛋白丝,但强度差异很大。两种药物——斯帕氟沙星(第三代)和莫西氟沙星(第四代)——表现突出:即使在相对较低的药物与蛋白质比例下,也能快速且不可逆地将长丝切割成更小的片段。
看见丝状结构瓦解
高分辨成像和生物物理测试揭示了药物处理下丝状体的变化。电子显微镜显示,未经处理的肌动蛋白形成长而连续的链,而有效的氟喹诺酮将其转化为短而分散的碎片。效力较低的成员产生弯曲和折角的丝,但并未完全断裂。基于热学的蛋白稳定性测定证实了这种物理性破坏:处理后,肌动蛋白的行为更像其游离、未组装的形式,熔点降低,但其基本构建单元结构几乎未改变。这表明药物并未使肌动蛋白本身错误折叠或受损——它们主要是撬开构成丝状体时单元之间的粘结。
放大到分子抓握位点
为理解为何某些氟喹诺酮比其他的更有效,团队结合了先进的核磁共振实验与药物–蛋白相互作用的计算模拟。他们发现所有化合物都依赖共同的环状“核心”与肌动蛋白接触,尤其是在该核心上有两个位点反复接触丝体。然而,在特定位点上附加的额外化学基团——称为R5和R7——强烈影响每个分子结合的牢固度和位置。在最有效的破坏剂中,这些位点带有氨基和大的环状体系,能够伸入相邻肌动蛋白链之间的一个小口袋,在那里它们干扰关键的稳定接触,包括通常有助于保持丝状体结合的一个重要盐桥。
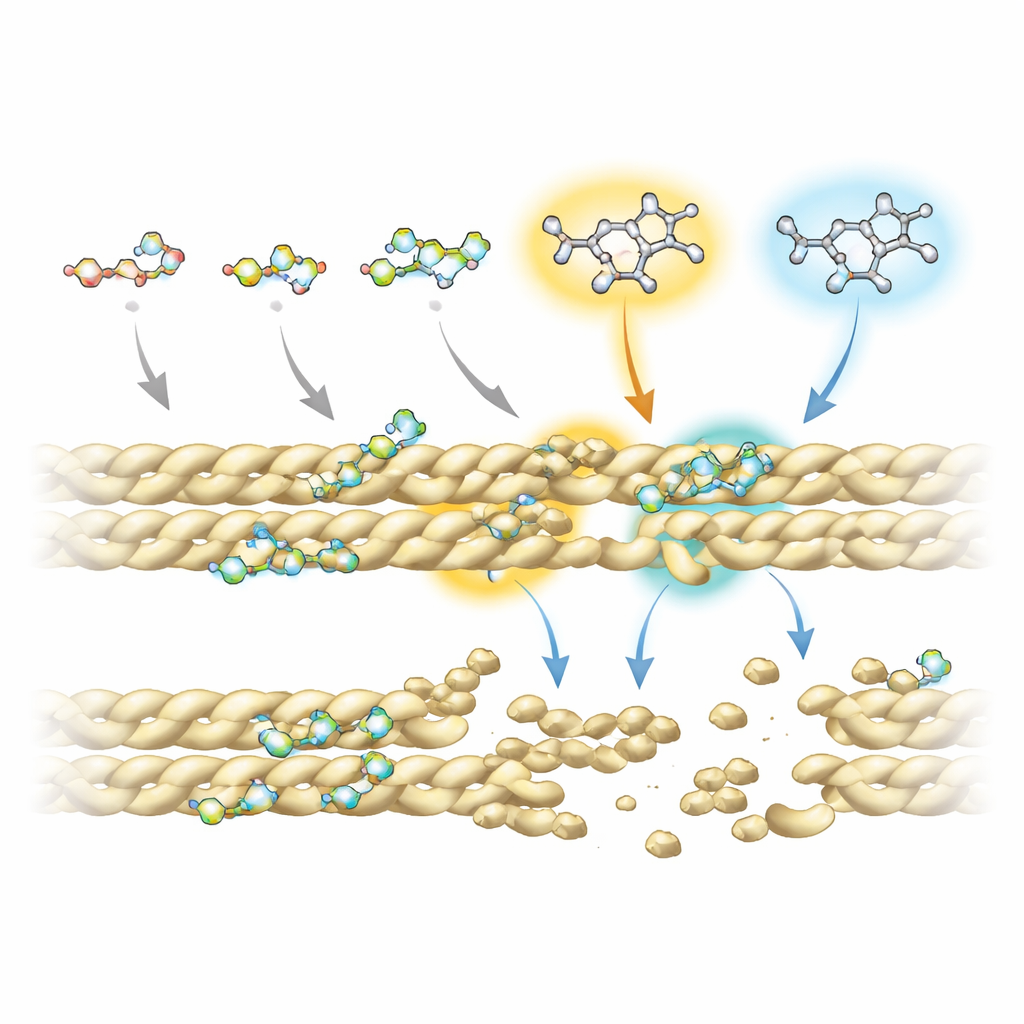
从酵母细胞到未来疗法
研究者还在一种自然积累肌动蛋白束的酵母菌株中测试了这些药物,以模拟病变细胞的某些方面。在显微镜下,未经处理的酵母显示出大而明亮的肌动蛋白团块,而暴露于氟喹诺酮的细胞——尤其是斯帕氟沙星、莫西氟沙星以及较高剂量下的萘啶酸——显示出更为弥散、点状的分布模式,表明这些束已被分解。重要的是,这些药物的作用显得相对温和:它们削弱了丝的堆积而没有严重扭曲肌动蛋白的基础形态,且其结合强度低于经典的肌动蛋白毒素,可能降低严重副作用的风险。
设计更智能的肌动蛋白靶向药物
总体而言,这项研究表明,对已知抗生素进行细微改造即可显著改变它们与细胞内部骨架的相互作用。通过将R5和R7位点标定为影响肌动蛋白破坏和大脑渗透性的关键“调节旋钮”,作者提出了一条基于氟喹诺酮的分子改造蓝图,旨在选择性拆散有害的肌动蛋白聚集体。尽管这些发现仍处于早期实验室验证阶段,但它们提出了一个可能性:未来从熟悉抗生素衍生的药物或许可以帮助清除神经细胞中的有毒支架,从而减缓或预防某些形式的神经退行性疾病。
引用: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
关键词: 肌动蛋白聚集体, 氟喹诺酮类抗生素, 神经退行性疾病, 药物再利用, 细胞骨架