Clear Sky Science · zh
与缺血‑再灌注损伤相关的细胞衰老基因的作用及其生物标志物的鉴定
为什么血液回流会加重心脏损伤
当有人心脏病发作或接受心脏手术时,医生争分夺秒恢复供血以挽救缺血的心肌。矛盾的是,这一步关键的救治行为本身有时会带来额外损害——这就是所谓的缺血‑再灌注损伤。该研究探讨了为何部分心脏细胞在血液回流时反应极差,聚焦于细胞衰老的生物学,并识别出一小组基因,可能帮助临床更准确地检测并最终治疗这种隐性损伤。
救援何以变成新的伤害
缺血‑再灌注损伤呈现为两个阶段。首先,冠状动脉被堵塞,心肌缺氧(缺血);随后当梗阻被清除、血液再次涌入(再灌注)时,活性分子和炎症的爆发会损害已然脆弱的细胞。现有工具——如心电图、影像扫描以及检测肌钙蛋白等血液标志物——往往漏检早期或微妙的损伤,且难以预测谁会出现长期问题。正是这种空白促使研究者深入探究心脏细胞内部的分子事件。
细胞衰老:一个被忽视的驱动因素
作者将重点放在细胞衰老上,这是一种细胞永久停止分裂并转向“报警”行为的状态。衰老的心肌细胞会分泌一系列炎性分子和酶,统称为衰老相关分泌表型(SASP)。这种化学“云团”会加剧瘢痕形成、吸引免疫细胞并干扰组织修复,从而形成损伤和慢性功能障碍的恶性循环。研究团队通过挖掘公开的小鼠心脏缺血‑再灌注基因表达数据,并与数百个与细胞衰老相关的基因交叉比对,将候选基因缩减到在损伤后显著变化的26个基因。
构成诊断指纹的六个基因
为了在这26个基因中找到最具信息量的信号,研究者使用了多种机器学习方法。那些算法搜索能够最好地区分受损心脏与健康心脏的基因组合。经过逻辑回归、LASSO和支持向量机分析后,六个基因脱颖而出,组成了一个强有力的诊断面板:CDKN2B、ID1、STAT3、TERF2、TP53和ZNF277。在合并的数据集中,这些基因的表达模式能够以非常高的准确率识别缺血‑再灌注损伤,在内部测试中优于许多传统血液标志物。基因‑通路分析将这些标志物关联到应激反应回路,涉及氧化损伤、细胞死亡程序以及如MAPK和PI3K‑AKT等已知信号通路,这些通路共同决定了细胞是恢复还是进入永久衰老。
免疫系统如何加入这一过程
由血流恢复引起的损伤不是孤立发生的;免疫细胞会迅速涌入心脏。通过从相同的基因表达数据估算免疫细胞活性,研究发现受损心脏中存在明显的免疫参与信号,包括多类T细胞、B细胞、巨噬细胞和肥大细胞。其中一个衰老相关基因CDKN2B与“中枢记忆”CD4 T细胞高度相关,而TP53则与活化的肥大细胞相关。这些关联表明,心肌细胞的衰老通路与免疫系统的变化彼此强化:“年长”细胞招来免疫响应,免疫反应反过来又可加剧损伤和瘢痕形成。
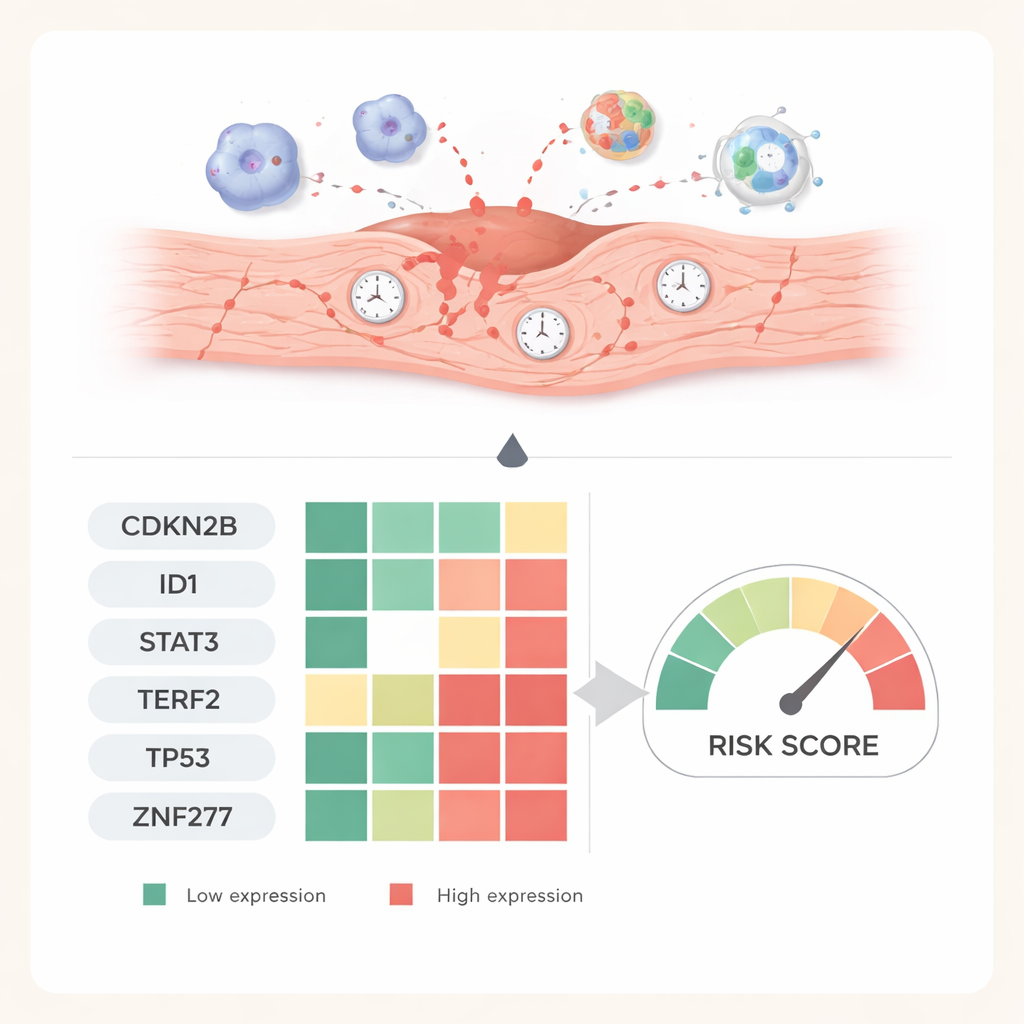
从计算预测到活体心脏的验证
为了检验这六个基因在计算结果之外是否具有实际意义,研究者建立了小鼠缺血‑再灌注损伤模型。他们在血流恢复后不同时间点测量基因活性,并通过组织染色在心脏切片中可视化相应蛋白。一个基因CDKN2B在一周内持续上升,提示其有助于将受损细胞锁定为长期衰老状态。其他基因如ID1、STAT3、TP53、TERF2和ZNF277在早期显著下降,随后逐步恢复,反映了急性应激、活跃损伤与随后修复之间的转变。这些时序性模式支持了每个基因捕捉心脏反应不同阶段的观点。
这对患者可能意味着什么
对普通读者来说,核心信息是该研究将心梗相关损伤与细胞衰老生物学联系起来,并在实验模型中识别出一个六基因“指纹”来标记这种损伤。尽管这项工作仍处于临床前阶段,主要基于小鼠数据和公开数据库,但它为开发新的血液或组织检测方法提供了路线图,可能比现有工具更早、更特异地检测缺血‑再灌注损伤。长期来看,理解这些与衰老相关基因如何调控炎症、瘢痕形成与修复,或可为在重新通畅血管的同时,帮助受损心脏更完全愈合的治疗策略开辟新途径。
引用: Sun, L., Liu, H., Jia, T. et al. The role of cellular senescence-related genes in ischemia–reperfusion injury and the identification of their biomarkers. Sci Rep 16, 5211 (2026). https://doi.org/10.1038/s41598-026-36076-2
关键词: 缺血 再灌注 损伤, 细胞衰老, 心脏病发作, 生物标志物, 免疫 炎症