Clear Sky Science · zh
结肠上皮细胞的ACE2表达与病毒感染、免疫和能量代谢相关
为何呼吸道病毒也关乎肠道
当我们想到COVID-19时,通常会联想到肺部积液和患者呼吸困难。然而,许多感染SARS-CoV-2的人也会出现腹痛、腹泻以及长期的肠道问题。本研究探讨了为何肠道——尤其是结肠——可能是病毒的重要靶点。通过对儿童结肠的单细胞进行放大观察,研究人员显示一个关键的病毒“门径”ACE2蛋白在特定肠道细胞中高度活跃,并且不仅与病毒感染有关,还与我们的免疫防御以及细胞如何管理能量相关联。
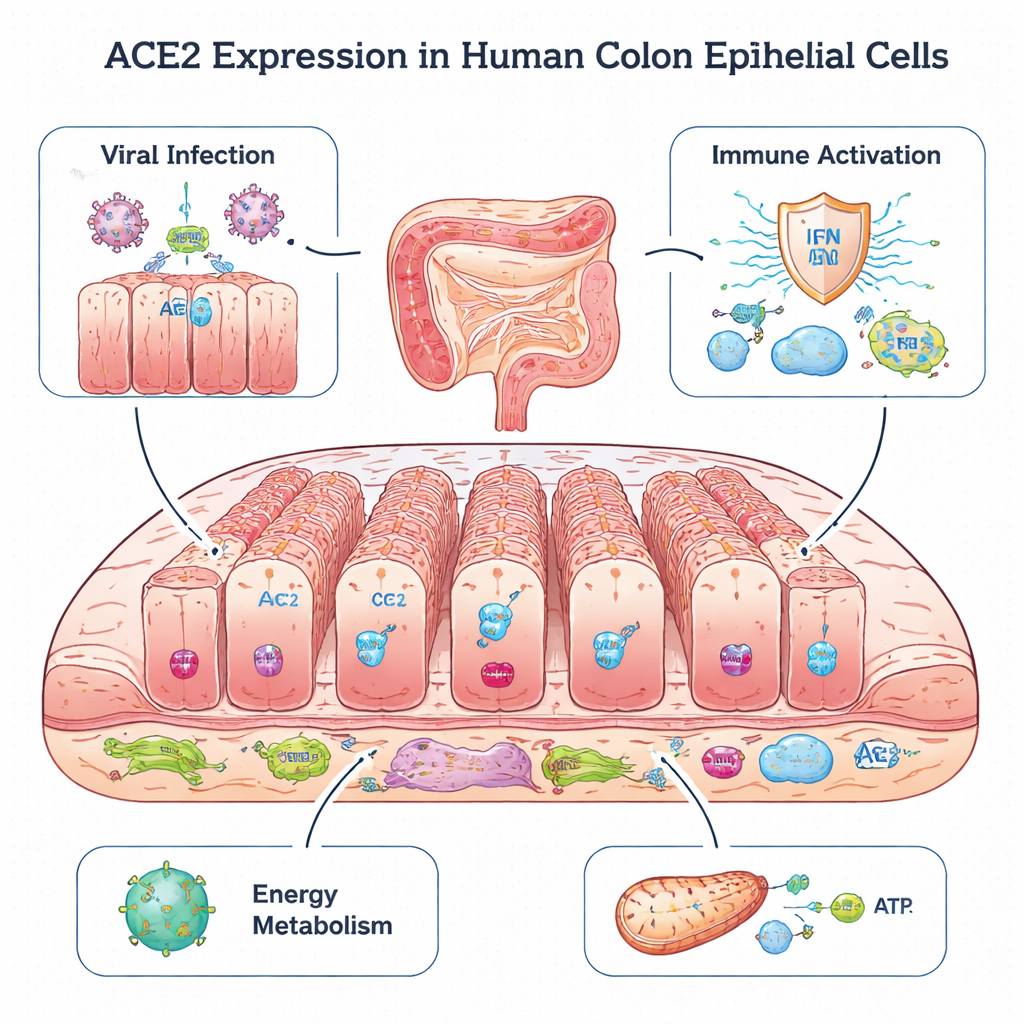
结肠中的细胞门径
ACE2最为人所知的是它是原始SARS病毒和SARS-CoV-2进入肺细胞的主要通路。具有讽刺意味的是,动物研究表明ACE2也能通过维持控制血压的激素系统平衡来保护组织免受损伤。在肠道中,已知ACE2有助于维持健康的微生物群并防止炎症。在这项工作中,科学家们重新分析了来自17名儿童结肠活检的单细胞RNA测序数据:其中一些儿童肠道健康,另一些患有结肠炎或炎性肠病,包括溃疡性结肠炎和克罗恩病。该技术使他们能够查看成千上万个单个细胞中哪些基因处于活跃状态,并精确定位ACE2在何处被启动。
结肠细胞:主要靶标与先遣反应者
分析显示,ACE2几乎集中表达在结肠细胞(colonocytes)中,这是一种主要的上皮细胞,衬在结肠内腔并面向肠道内容物。与其他上皮细胞相比,结肠细胞还表现出更高的基因活性,这些基因有助于病毒进入细胞、出芽和释放。与此同时,这些细胞表达了许多参与感知病毒遗传物质并触发I型和III型干扰素反应的基因——这是免疫防御的重要早期报警系统。它们还产生炎性信号和将病毒片段呈递给T细胞的分子,表明结肠细胞既可能成为病毒靶标,也是在早期警报中向免疫系统发出信号的重要前沿哨兵。
免疫与能量利用的关联网络
研究人员接着询问在结肠细胞中还有哪些基因的表达与ACE2同步上调或下调。他们发现有超过3400个基因随着ACE2水平上升而上调,而有超过2100个基因在ACE2增加时反而下降。与ACE2正相关的基因富集于与病毒进入和释放、先天免疫信号、自然杀伤细胞和T细胞的杀伤活性以及多条细胞内产能通路相关的过程,包括线粒体功能和脂肪与糖的代谢。相比之下,与ACE2呈负相关的基因——在ACE2低时表达高——与基于抗体的(体液)免疫、细胞的蛋白质合成机器、细胞吞噬等胞内摄取过程以及补体系统(另一条免疫防御途径)有关。这一模式表明ACE2标志着结肠细胞处于一种偏向快速抗病毒感应和能量产生的状态,同时其他较慢的免疫程序被下调。
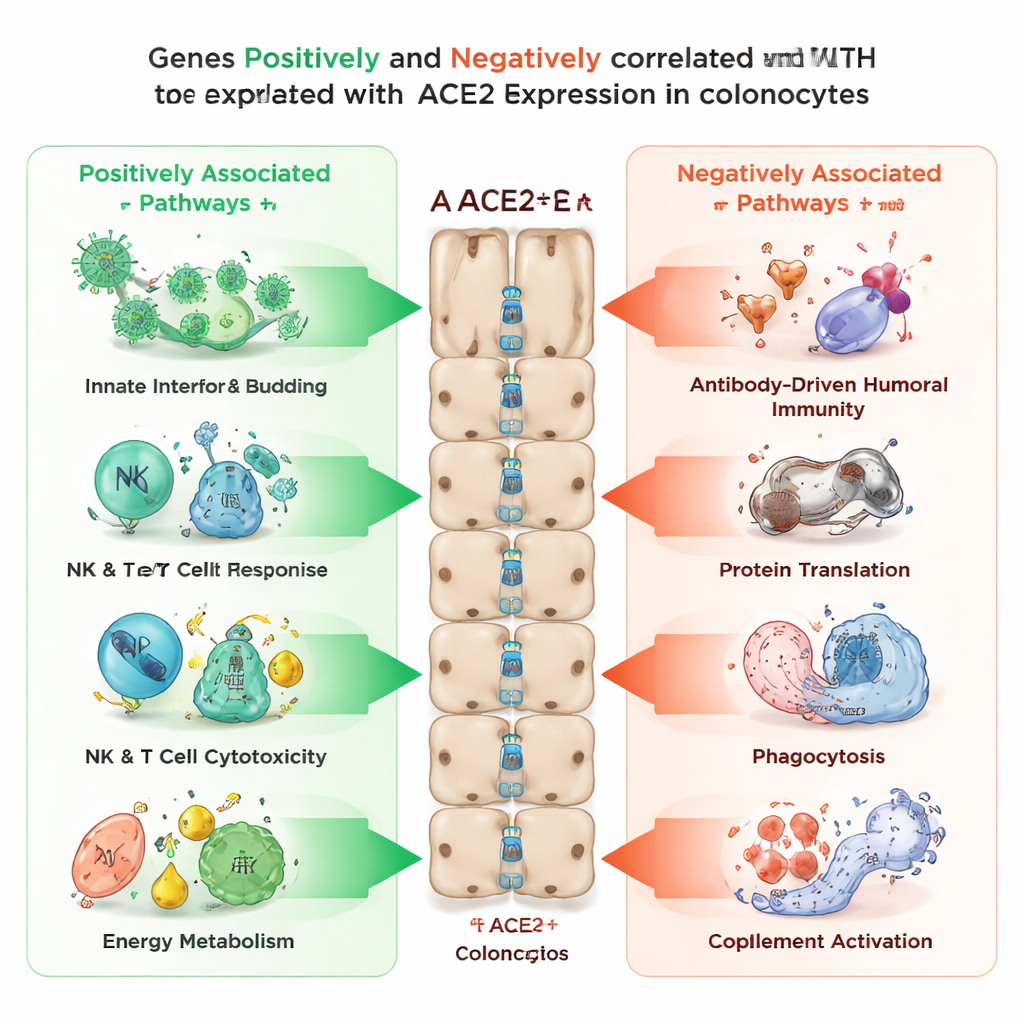
来自炎症性肠道的证据
为了验证这些模式在实际组织中是否存在,团队在来自溃疡性结肠炎、克罗恩病患儿及对照的结肠样本上使用了多重免疫荧光技术——该技术用不同颜色标记特定蛋白。他们证实ACE2蛋白主要位于用EPCAM标记的上皮细胞上。在炎性肠病患者中,ACE2阳性的细胞显示出更高水平的IFNA4和RSAD2,这两种蛋白与干扰素信号通路和抗病毒活性密切相关。这表明在发炎的肠道中,携带ACE2的结肠细胞不仅是潜在的病毒通道,还是抗病毒反应的热点。
对患者与未来治疗的意义
对于非专业读者而言,信息是:结肠在COVID-19中并非被动旁观者。让病毒进入细胞的同一蛋白也帮助协调肠道免疫和能量利用,特别是在有既存肠道炎症的儿童中。这种双重作用或有助于解释为何一些患者出现胃肠道症状,以及为何炎性肠病患者在COVID-19中的结局复杂但并非一概更差。该研究也为关于作用于凝血与血压通路的药物提供了更多讨论基础,其中部分药物可能减轻严重感染时的肺与血管损伤。尽管该研究基于相关性,无法证明因果关系,但它强调了富含ACE2的结肠细胞在病毒进入、免疫防御与代谢交汇处的重要作用——指出肠道是冠状病毒疾病中的一个关键且可能可被干预的领域。
引用: Qi, Y., Huang, Y., Chen, H. et al. ACE2 expression by colonic epithelial cells is associated with viral infection, immunity, and energy metabolism. Sci Rep 16, 5738 (2026). https://doi.org/10.1038/s41598-026-36052-w
关键词: ACE2, 结肠细胞, COVID-19 肠道, 炎性肠病, 抗病毒免疫