Clear Sky Science · zh
内皮祖细胞分泌组蛋白质组分析识别出Serpine 1作为强效成骨调节因子
在不取供体移植物的情况下愈合断骨
当骨骼严重断裂或有缺损时,外科医生常常难以同时恢复其强度和形状。现有选择——自体取骨或使用合成移植体——可能伴随疼痛、风险,并且并非总是成功。本研究探讨了另一种思路:能否不移植细胞,而只是递送恰当的天然蛋白质来激活机体自身的造骨机制?
为何某些骨损伤难以愈合
大多数骨折会自发愈合,但较大骨缺损——例如由外伤、肿瘤或严重牙槽骨萎缩造成的——常常不会。在这些情况下,局部血管细胞和成骨干细胞数量不足,无法重建缺失部分。组织工程研究者试图通过组合三要素来解决这一问题:能够形成新骨的活细胞、为其提供生长空间的支架,以及指导其行为的信号。细胞移植虽可奏效,但成本高、监管严格,并不总适合常规临床使用。这推动科学家寻找以智能生物材料和精心挑选蛋白为核心的“无细胞”解决方案。
来自血管形成细胞的秘密信号
内皮祖细胞是血液中罕见的细胞,参与新血管的形成。早期工作表明,当这些细胞移植到骨附近时,它们通过分泌可溶性信号促进愈合,而并非直接转化为骨细胞。在本项新研究中,作者收集了这些细胞培养生长所用的培养上清液,并利用先进的蛋白质分析技术对数百种分泌分子进行了目录化。他们聚焦于八种与血管生长和骨形成密切相关的蛋白,并在体外用人骨髓干细胞和人微血管内皮细胞系统测试,系统评估这些蛋白对细胞增殖、定向迁移以及诱导类骨矿化的效果。
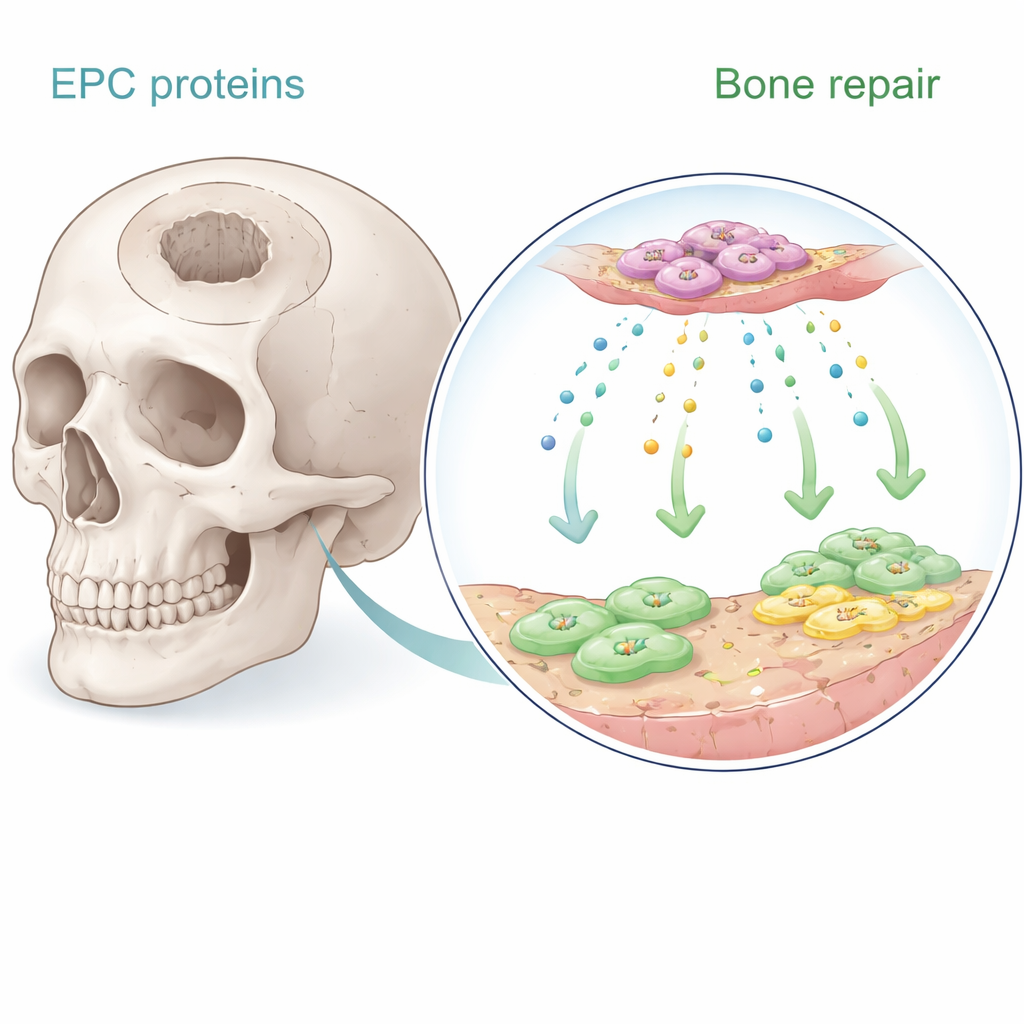
一款出人意料的蛋白占据主导
在候选蛋白中,有一种蛋白脱颖而出:Serpine-1,通常以其在血液凝固调节和伤口愈合中的作用而闻名。在培养皿中,Serpine-1以剂量依赖的方式显著增加了骨髓干细胞和内皮细胞的增殖,在这方面比BMP-2和SDF-1等知名生长因子表现更佳。它还促进了干细胞向成骨细胞的成熟,经典染色方法显示碱性磷酸酶活性和富含钙的矿化沉积增加。其它蛋白,如血小板衍生生长因子和BMP-2,在迁移实验中更能促使细胞爬入“伤口”区域,但Serpine-1罕见地同时增强了细胞数量和成骨行为的能力。
将蛋白转化为可用的植入物
发现有前景的蛋白只是挑战的一半;还必须以可控方式将其递送到损伤部位。研究团队将Serpine-1封装在由医用聚合物PLGA制成的微小可降解球体中,然后将这些微球混入软性胶原凝胶,形成能够缓慢释放蛋白的支架。他们在小鼠体内测试该系统:在颅骨上打了一个4毫米的圆形缺损——这一尺寸通常不会自愈。有些缺损仅填充胶原,有些填充胶原加空微球,有些则填充负载Serpine-1的支架。八周后,高分辨率微CT显示,Serpine-1组在缺损内部的骨体积、密度和厚度显著更高。值得注意的是,只有这些动物在缺口中心形成了新骨,而不仅仅是沿边缘生长。
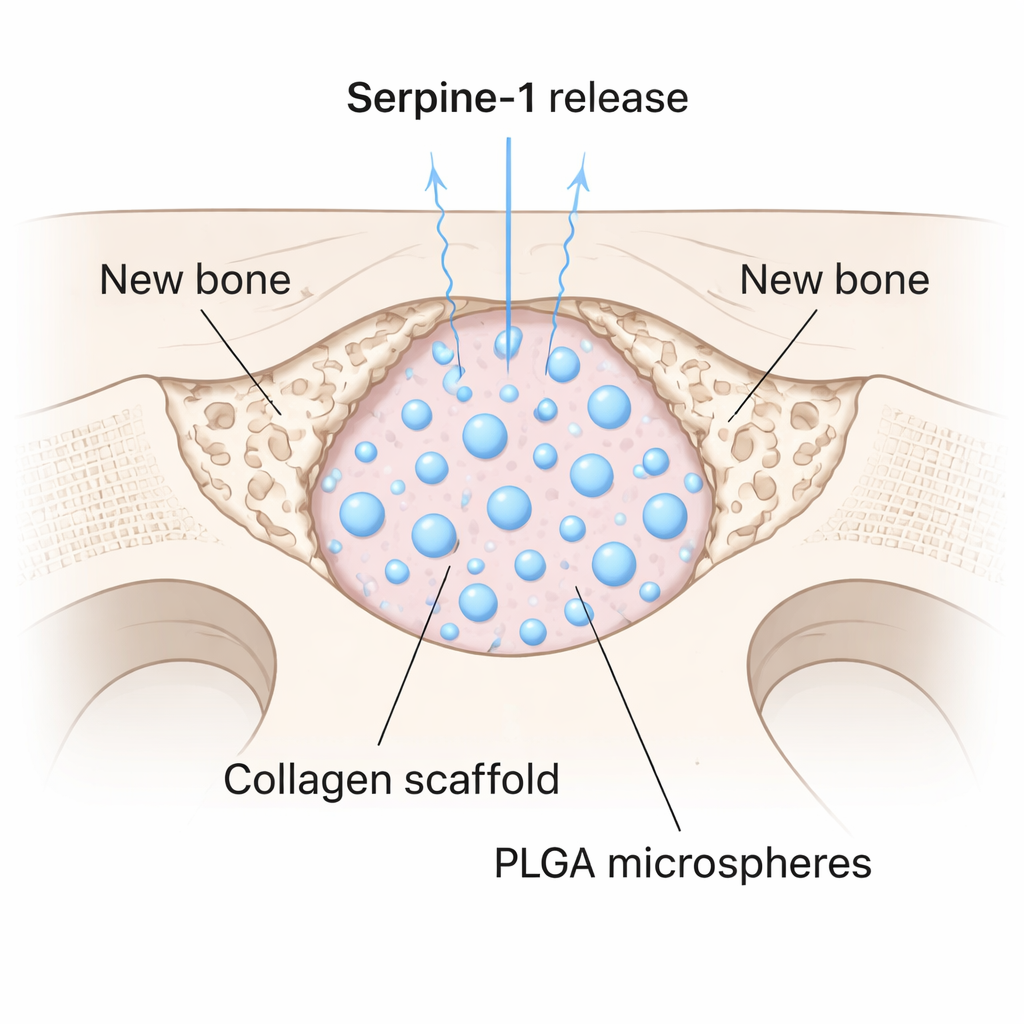
这对未来骨科护理意味着什么
该研究将Serpine-1引入视为一种强效且此前被低估的成骨信号。通过将这种蛋白与缓释支架配对,研究人员在本来不会愈合的缺损中实现了显著的骨再生。尽管Serpine-1在吸引细胞迁入缺损方面不如某些其他因子,但其促进现有细胞增殖和成熟的能力表明,可将其与促进迁移的蛋白联合使用以取得更好效果。对患者而言,这类无细胞、基于蛋白的材料未来可能减少自体取骨或依赖复杂细胞疗法的需求,为促使顽固骨损伤最终愈合提供一种更简便的途径。
引用: Asbi, T., Tamari, T., Doppelt-Flikshtain, O. et al. Proteomic analysis of endothelial progenitor cells secretome identifies Serpine 1 as a potent regulator of osteogenesis. Sci Rep 16, 5165 (2026). https://doi.org/10.1038/s41598-026-36048-6
关键词: 骨再生, Serpine-1, 组织工程, 内皮祖细胞, 胶原支架