Clear Sky Science · zh
分子拥挤对细菌蛋白质组中蛋白质稳定性的影响
为什么蛋白质的拥挤生活很重要
在每个活细胞内部,蛋白质在一个被其他分子挤得水泄不通的空间中执行它们的功能,几乎一半的体积可能被占据。然而,大多数实验室实验在稀释、几乎空旷的溶液中研究蛋白质。本文提出了一个简单但重要的问题:这种拥挤的现实如何改变蛋白质的稳定性和行为?这对分子尺度上的生命如何运作意味着什么?
窥探拥挤的细胞世界
为了解这一点,研究者使用了一种名为Cupriavidus necator的细菌,这种微生物在碳捕获和生物塑料生产等绿色技术中很有应用价值。他们温和地裂解细胞,使数百种不同蛋白质尽可能保持接近天然的状态。随后他们加入高浓度的大型亲水聚合物——常用来模拟细胞致密内部的“拥挤剂”,如PEG、右旋糖、和Ficoll。
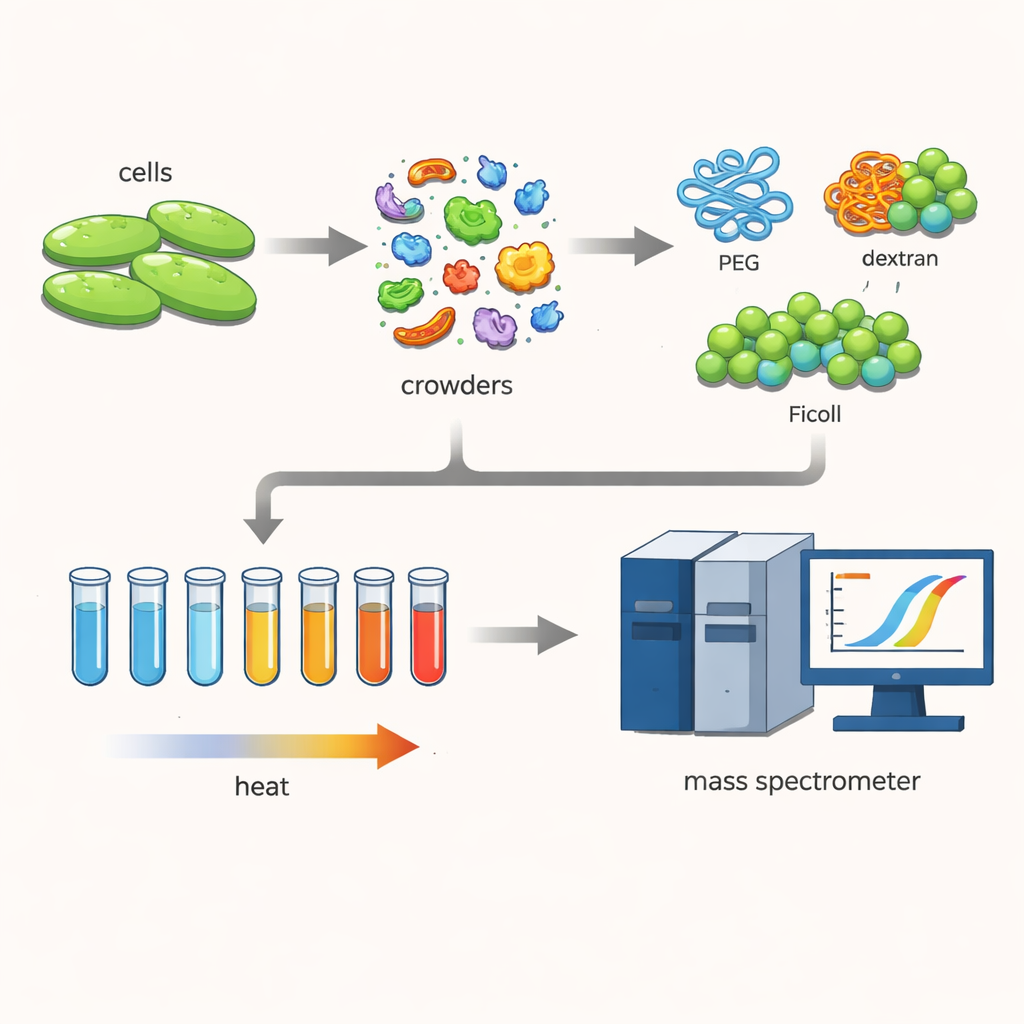
观察蛋白质的熔解
团队使用了一种称为热蛋白质组谱的技术。他们将蛋白质混合物的许多微小样本以阶梯方式从30摄氏度加热到70摄氏度。随着温度升高,较不稳定的蛋白质会展开并聚集,从而沉降出溶液。通过标记剩余的可溶性蛋白并用高灵敏度质谱测量,科学家们能够重建每种蛋白的熔解曲线并确定其熔点——即半数蛋白从可溶、可工作的状态中丧失的温度。比较有无拥挤剂时的这些温度,揭示了拥挤环境如何改变蛋白质的稳定性。
复杂的图景:有些蛋白更稳,有些更脆
总体而言,加入任一六种聚合物拥挤剂都会降低细菌蛋白质组的平均熔点,意味着存在轻微的总体去稳定效应。但这一全局趋势掩盖了更为细致的情况。对数十种个别蛋白质而言,拥挤剂要么明显提高稳定性,要么明显降低,有时变化达几度。大多数蛋白只对六种试剂中的一种有反应,但有少数对多种试剂都有响应,且几乎所有这些蛋白都表现出一致的被稳固或被去稳定的趋势,这提示它们与拥挤剂相互作用的底层特征可能相似。
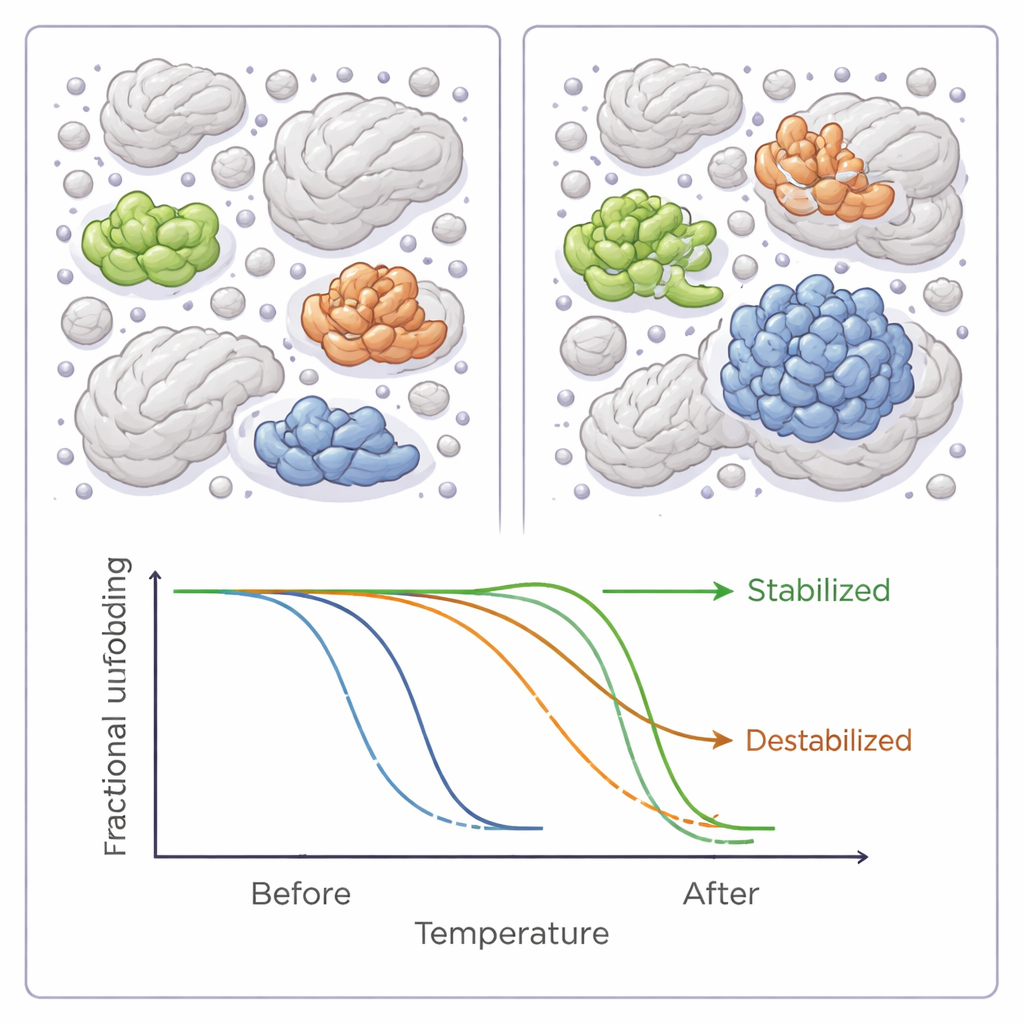
是什么让蛋白在拥挤中胜出或失利
当作者更仔细地查看这些敏感蛋白的性质时,出现了模式。那些在拥挤条件下变得更稳定的蛋白往往更疏水——即具有更多排斥水的表面——且更常见于具有明确活性位点的经典酶类。它们也更可能参与蛋白—蛋白相互作用或携带调节功能的化学修饰。相比之下,去稳定的蛋白平均更小,且较少带有此类修饰。这些发现与计算模型和其他实验结果相呼应:拥挤可以因蛋白的大小、形状以及它们通常如何与伙伴相互作用而有选择性地有利于某些蛋白,同时使其他蛋白更脆弱。
超越简单挤压:拥挤剂的真正作用方式
传统对分子拥挤的解释侧重于“排除体积”——大分子简单地占据空间,减少可用空间,从而推动蛋白保持折叠状态。如果这就是全部解释,人们会期望拥挤剂主要稳定蛋白,并且与拥挤剂的体积或粘稠度有强相关性。相反,作者只观察到与聚合物尺寸和黏度的弱关联。他们的数据更契合“优先排斥”模型:拥挤剂与蛋白在化学上相互回避,这间接偏向某些折叠态,但也可能扰动维持其他蛋白稳定性的微妙相互作用。简言之,不只是物理挤压,而是微妙的化学推拉共同塑造了蛋白的行为。
这对理解生命化学意味着什么
对非专业读者来说,关键的信息是:细胞内的蛋白质不能仅在孤立、清澈缓冲液中被完全理解。围绕它们的稠密分子“丛林”可以使某些蛋白更坚固,而使另一些更脆弱,从而改变整套反应网络的行为。通过一次性测量数百种蛋白的稳定性变化,这项研究表明拥挤效应是复杂且蛋白特异的,并且可能与直接相互作用一样受简单包装效应驱动。无论是设计药物、工业酶还是工程微生物,认识到这种拥挤现实对于预测蛋白在生物系统中真实表现至关重要。
引用: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
关键词: 分子拥挤, 蛋白质稳定性, 热蛋白质组谱, 细菌蛋白质组, 细胞环境