Clear Sky Science · zh
细颗粒物通过DNMT3A介导的GPX4 DNA甲基化调控加重儿童哮喘
脏空气为何对儿童肺部有害
城市烟雾不仅碍眼;它会把哮喘儿童送进急诊室。本研究提出了一个对居住在污染地区家庭至关重要的问题:称为PM2.5的微小空气颗粒究竟如何使哮喘发作加重?通过追踪从室外空气到儿童气道上皮细胞发生的变化,研究人员发现了肺细胞内一条隐藏的事件链,将污染与炎症和气道受损联系起来。
微粒虽小,麻烦很大
PM2.5指的是小到能深入肺部的悬浮颗粒。临床上早已观察到,PM2.5水平高的日子常伴随哮喘症状的加重——更多咳嗽、喘鸣和呼吸困难。然而将脏空气与这些发作之间连接起来的生物学步骤仍不清晰。本研究聚焦于儿童哮喘,利用动物模型和儿童样本,显示PM2.5不仅仅是表面刺激肺部;它似乎触发了一种特定的细胞损伤形式,从而加剧炎症。
气道内的一种特殊细胞损伤
团队将注意力集中在一种新近被认识到的细胞死亡类型——铁死亡(ferroptosis),这种死亡由铁和细胞膜脂质的失控氧化驱动。他们将小鼠和人支气管细胞暴露于蟑螂过敏原(一种常见的哮喘诱因)和PM2.5。在小鼠中,PM2.5暴露导致更多炎性细胞聚集在气道周围、黏液增厚以及肺组织中炎性分子IL-6和IL-8水平升高。当研究者给予阻断铁死亡的药物时,这些有害变化在很大程度上被抑制,提示这种特定的细胞损伤是污染加重哮喘的关键步骤。
机体的内在保护以及污染如何使其失效
细胞对抗这种破坏性氧化有自身防御机制,其中一个重要的保护者是名为GPX4的蛋白。在健康的气道细胞中,GPX4有助于中和有害的氧化副产物,防止它们破坏细胞膜。本研究中,PM2.5暴露使小鼠肺和人气道细胞中的GPX4水平下降。随着GPX4减少,细胞表现出更多活性氧、更多膜损伤以及线粒体功能丧失——这些都是铁死亡的标志。当科学家在细胞中人为提升GPX4时,大部分氧化应激、细胞损伤和IL-6/IL-8的释放被逆转,强调了GPX4作为关键保护屏障的作用。
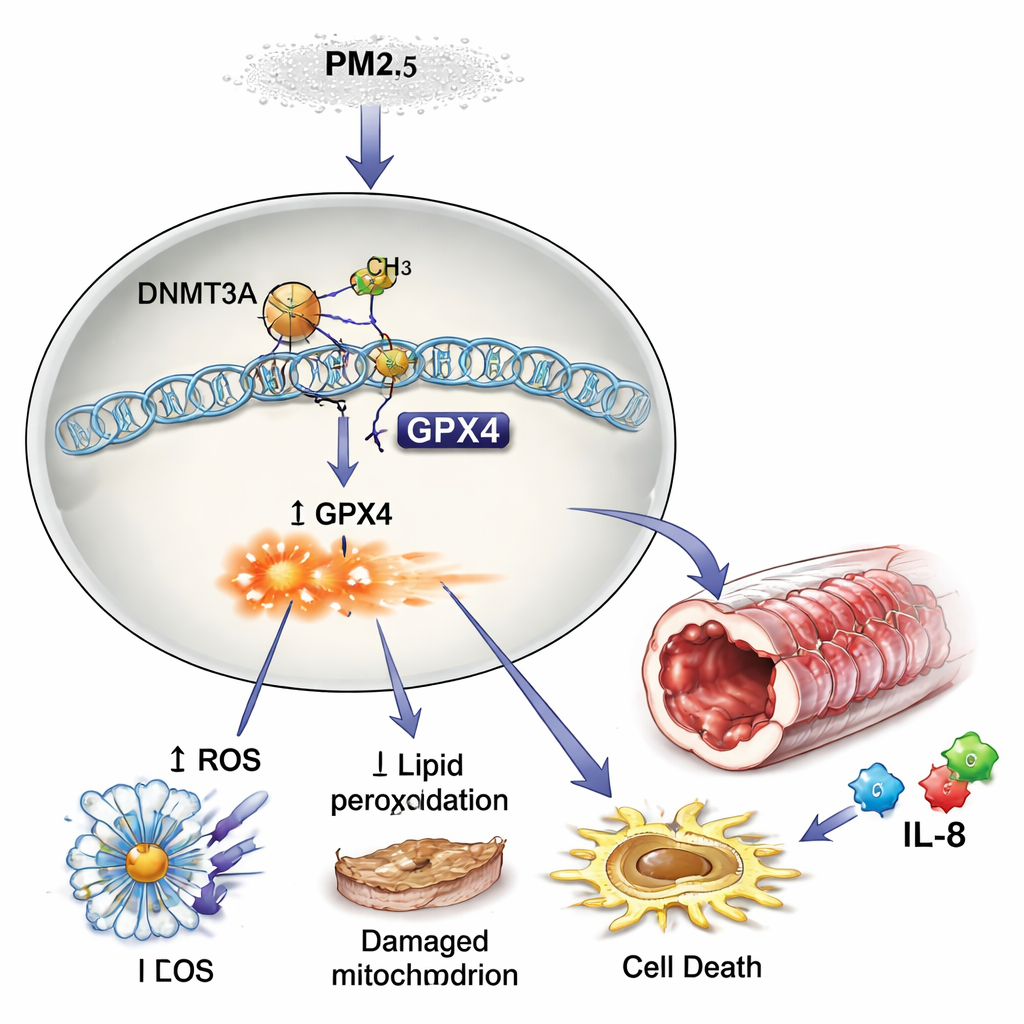
污染通过化学标签重写基因开关
为何PM2.5暴露后GPX4水平下降?答案在于表观遗传学——像是基因上的调光开关的化学标签。研究人员发现,PM2.5增加了一种名为DNMT3A的酶的活性,该酶会在DNA上添加甲基。这些甲基在GPX4基因的控制区积累,实际将该基因的活性调低。阻断DNMT3A可以防止这种额外的甲基化并恢复GPX4的表达,表明PM2.5通过加紧这个基因调光开关来“重编程”气道细胞。在哮喘儿童的血细胞中,病情更严重者具有更高的GPX4甲基化、更低的GPX4蛋白水平及更高的IL-6/IL-8水平,这一结果与实验室发现相呼应。
对保护儿童意味着什么
对非专业读者而言,信息是:微小的污染颗粒不仅仅刺激肺部;它们悄悄改变气道细胞中关键保护基因的工作方式。PM2.5提升了DNMT3A,后者添加的化学标签会抑制GPX4这道“防护盾”。当这道防护被削弱时,细胞更易发生铁死亡并释放促炎分子,这些分子使儿童的气道收缩和堵塞,从而加重哮喘。这些发现不仅强化了清洁空气政策和室内空气防护的重要性,也指向未来可能的药物策略——例如直接作用于肺部以保护或恢复GPX4功能——以帮助生活在污染环境中的儿童更容易呼吸。
引用: Wu, X., Dai, L., Li, R. et al. Fine particulate matter exacerbates childhood asthma via DNMT3A-mediated modulation of GPX4 DNA methylation. Sci Rep 16, 5566 (2026). https://doi.org/10.1038/s41598-026-35962-z
关键词: 大气污染, 儿童哮喘, PM2.5, 表观遗传学, 肺部炎症