Clear Sky Science · zh
OCT4与人源LIN28B核小体结合的结构分析
细胞如何访问隐藏的遗传指令
你体内的每个细胞都携带相同的DNA,但在任一细胞类型中,只有一小部分遗传指令被使用。这种控制在很大程度上来自DNA如何紧密地缠绕在称为组蛋白的蛋白质上,形成被称为核小体的结构。这样的紧密包装会将关键的DNA片段对细胞的读写机器隐藏起来。本研究考察了一种特殊蛋白质OCT4如何在目标DNA被缠绕并部分隐藏在核小体内时仍能找到并结合它——这一过程对干细胞身份和细胞重编程至关重要。
为什么先锋因子对干细胞很重要
OCT4属于一小类但功能强大的蛋白,称为先锋转录因子。与大多数DNA结合蛋白不同,先锋因子能够渗入紧密压缩的“关闭”基因组区域并帮助开启基因,在塑造细胞身份和将成体细胞重编程回类干细胞状态中发挥关键作用。OCT4与SOX2、KLF4和c-MYC等伙伴协同作用以诱导多能性——使干细胞能够分化为几乎任何细胞类型的特性。准确了解OCT4如何搭接核小体上被缠绕的DNA,对于解读细胞如何改变命运以及在研究和医学中更精确地操控细胞身份至关重要。
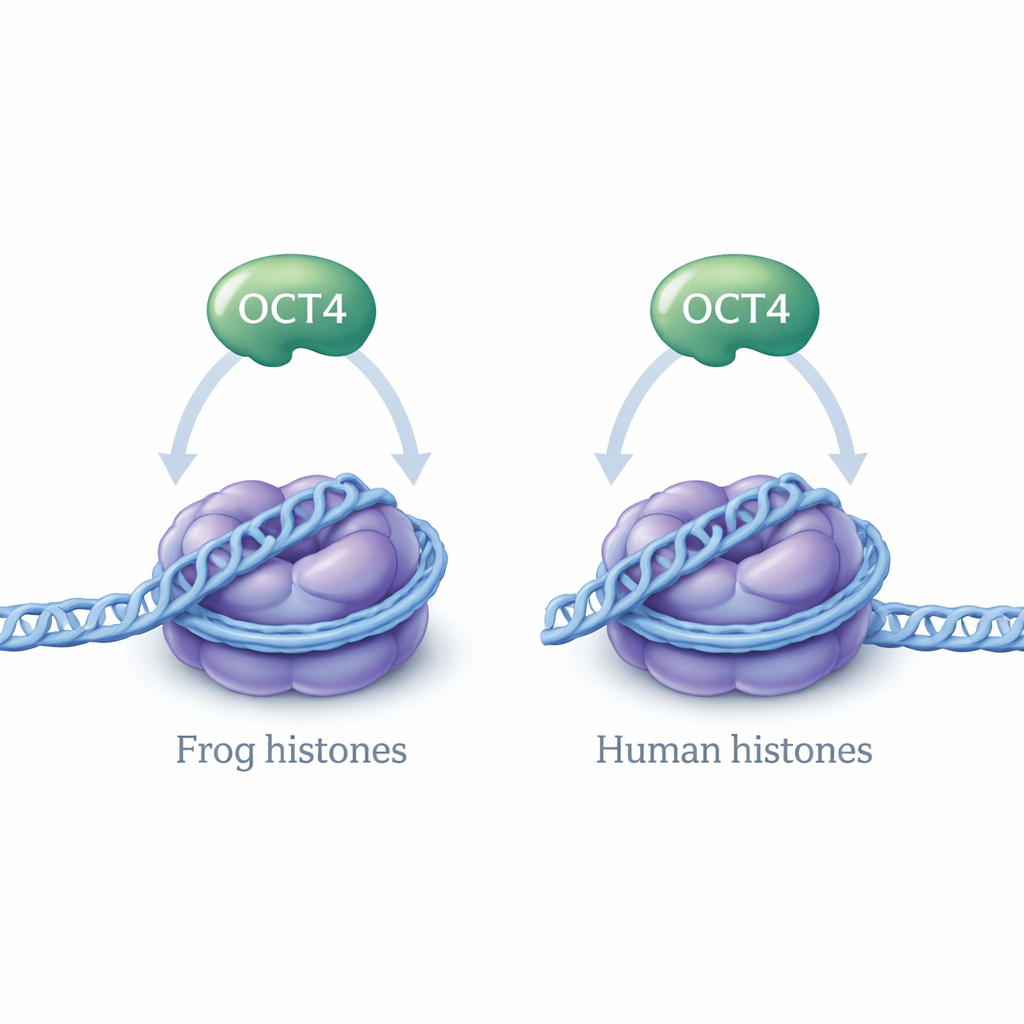
检验物种差异是否重要
大多数核小体的结构研究使用来自非洲爪蟾(Xenopus laevis)或人类的组蛋白,因为这些蛋白非常相似但并非完全相同。它们氨基酸序列中的微小差别理论上可能改变DNA的缠绕方式或像OCT4这样的调控蛋白的结合方式。在先前的工作中,作者表明当人源LIN28B基因的一段特定调控DNA被用爪蟾组蛋白组装成核小体时,OCT4可以与之结合。在这项新研究中,他们提出了一个简单但重要的问题:当核小体由人源组蛋白而非爪蟾组蛋白构建时,OCT4是否表现相同?
构建并探测LIN28B核小体
为了解答这一问题,研究人员在体外用一段182碱基的LIN28B DNA片段,分别与人源或爪蟾组蛋白蛋白质,采用模拟细胞环境的“缓慢透析”方法重建了核小体。凝胶实验确认两种组蛋白八聚体都能有效形成核小体。随后他们检查这些核小体在LIN28B DNA上的位置。凝胶实验和随后的酶切测序(MNase-seq)显示,LIN28B DNA可以在组蛋白核心上采取多种定位,这种行为在将核小体加热到体温时也未发生改变。关键是,组蛋白来自爪蟾还是人类对DNA的定位或OCT4的结合紧密度没有明显影响。
可视化核小体上的OCT4
团队随后使用冷冻电镜(cryo-EM)对含有人源组蛋白的LIN28B核小体上结合OCT4的结构进行成像。从大约15,000个颗粒中,他们重建了约6埃分辨率的三维图谱。图像显示,OCT4的两个DNA结合部分都接触到位于核小体进出口附近的同一段暴露DNA,即所谓的连接区。这正是之前在用爪蟾组蛋白构建的核小体上观察到的结合位点和取向。当将早期模型拟合到新的cryo-EM图谱中时,匹配效果很好,表明OCT4–LIN28B核小体复合体的整体构象在两种物种间基本相同。
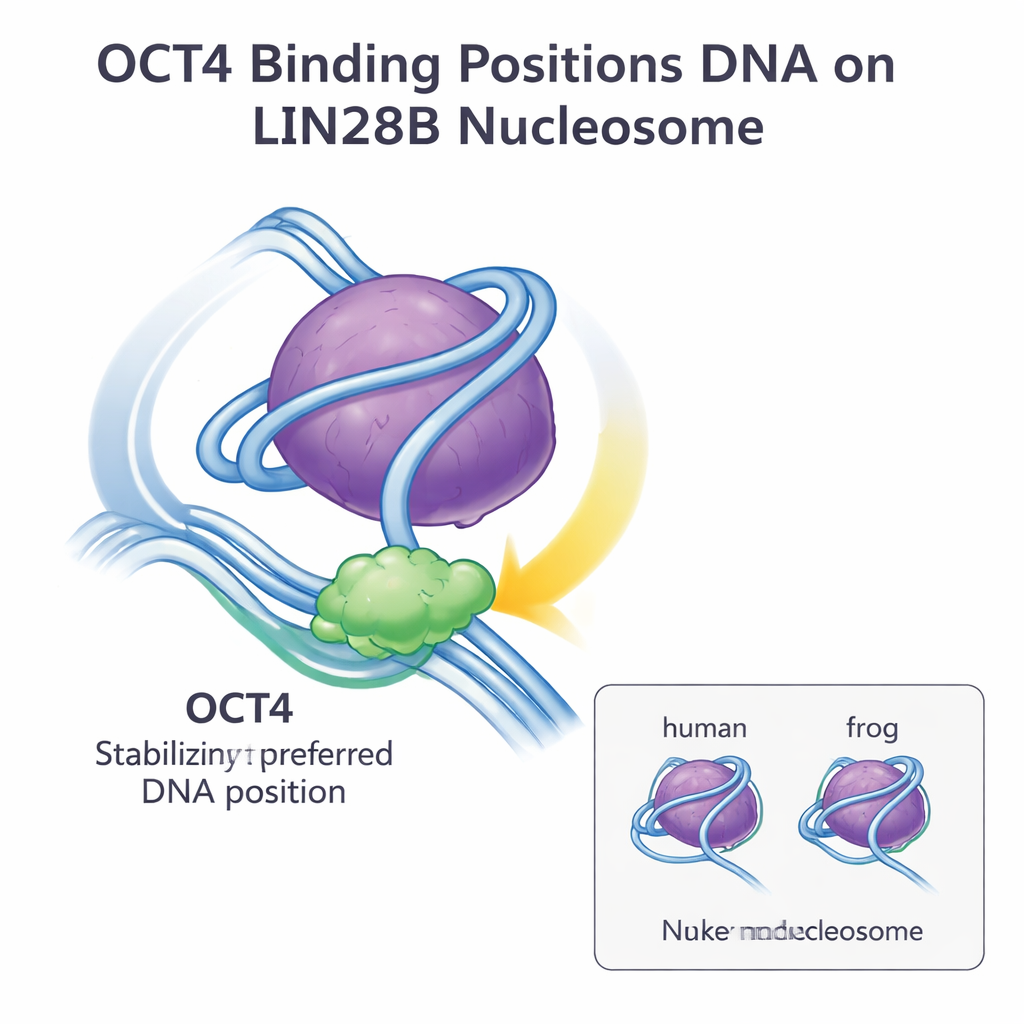
打开染色质的一般策略
综合来看,这些发现表明,爪蟾与人类组蛋白之间的微小序列差异不会改变OCT4识别和结合LIN28B核小体的方式。LIN28B DNA自发地在组蛋白核心上处于多种可能位置,但OCT4结合能选择并稳定一种优选位置,从而使更多结合位点对OCT4及其伙伴更易接触。这种“DNA定位与稳定”策略似乎是先锋因子进入封闭染色质并促进其他调控因子协同结合的一种普遍方式。对非专业读者而言,结论是核小体的基本设计以及像OCT4这样的关键调控蛋白与其协作的方式在物种间高度保守,这强化了用模式生物获得的见解能够可靠地帮助理解人类基因调控与干细胞生物学的观点。
引用: Sinha, K.K., Halic, M. Structural analysis of OCT4 binding to human LIN28B nucleosomes. Sci Rep 16, 5704 (2026). https://doi.org/10.1038/s41598-026-35959-8
关键词: 先锋转录因子, OCT4, 核小体结构, 染色质可及性, 干细胞基因调控