Clear Sky Science · zh
水通道蛋白-4的超分子聚集如何塑造星形胶质细胞的集体迁移与力学特性
大脑细胞如何协同移动以实现修复
当大脑受伤或出现炎症时,其支持细胞——星形胶质细胞会迅速聚集以保护、修复或隔离受损区域。本研究探讨了一个意想不到的因素,决定了这些细胞协同移动的效率:称为水通道蛋白‑4(AQP4)的小型水通道。通过观察AQP4分子在星形胶质细胞膜上是如何聚集或分散,研究人员揭示了大脑“水管系统”如何协助协调集体细胞运动,以及慢性炎症如何扰乱该过程。
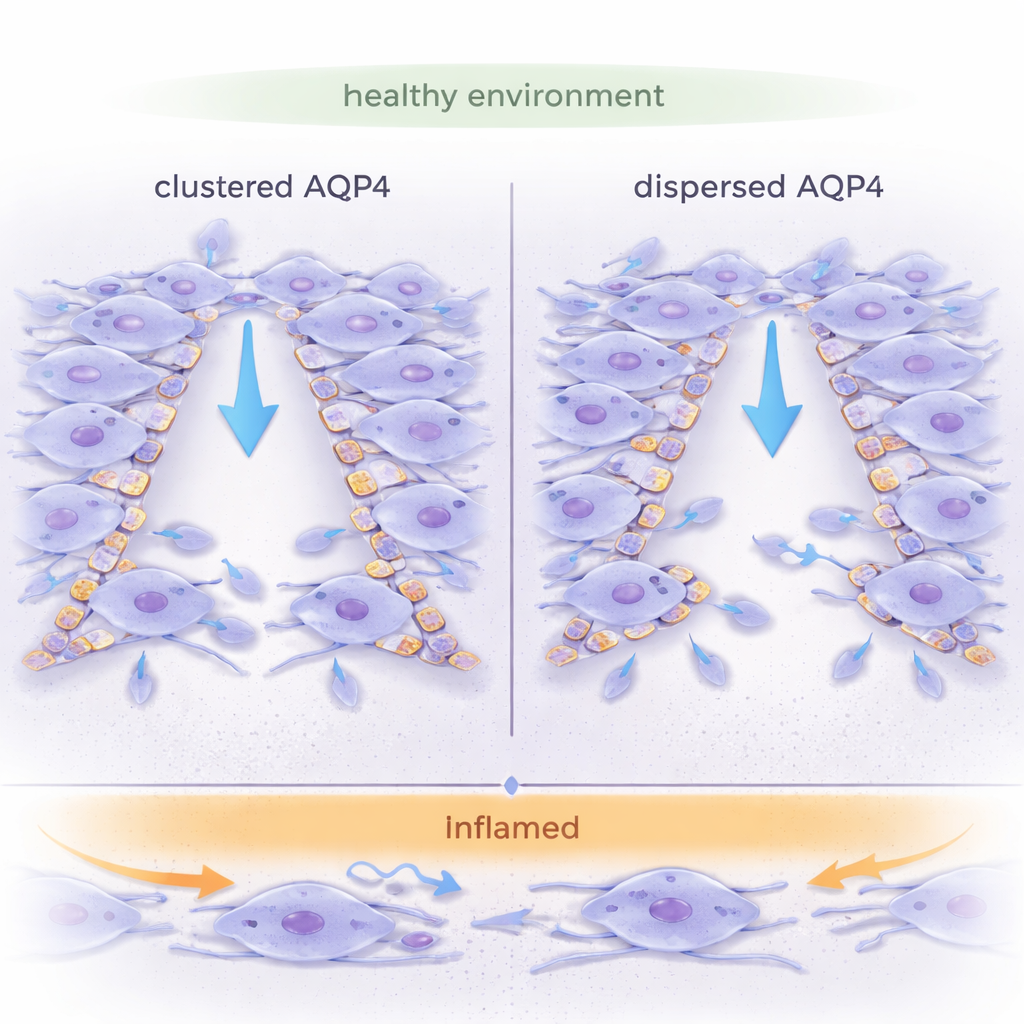
细胞上的水通道
星形胶质细胞呈星状,参与维持脑内稳态、引导发育并应对损伤。它们富含AQP4,这是一种形成孔道、允许水快速进出细胞的蛋白。与许多其他水通道不同,AQP4可以组装成大型晶体样斑块,称为正交粒子阵列(OAPs),或者保持为较小、分散的单位(四聚体)。AQP4的组织方式被认为会影响细胞的形变与运动,但以往大多研究集中于单个细胞。本研究提出更贴近生理的问题:AQP4的组织如何影响整片星形胶质细胞层像在脑组织伤口愈合时那样协同迁移?
在健康与炎症条件下测试细胞迁移
研究人员培养了两种小鼠星形胶质细胞:能够形成AQP4阵列的正常细胞,以及经基因改造(OAP缺失)不表达主要阵列形成型AQP4、因此主要携带分散四聚体的细胞。随后他们在人为密集细胞层上制造“划痕”以模拟伤口,并观察细胞闭合缝隙的速度和平滑度。为模拟慢性受伤的大脑,他们还在测试前一周将部分培养物置于两种炎性分子IL‑1β和TNF‑α的环境中。利用时间流逝成像和一种称为粒子图像测速(PIV)的计算机视觉方法,他们不仅量化了细胞移动的距离和速度,还评估了整个细胞层运动的直线性、协调性与应变分布。
分散的通道,使运动更顺畅
在无炎症条件下,携带分散AQP4(OAP缺失)的星形胶质细胞在集体迁移方面明显更胜一筹:它们愈合伤口更快,移动更有方向性和线性,领先的前沿平滑且连续,邻近细胞以连贯的“片层”方式移动。相比之下,具有聚集AQP4(野生型)的星形胶质细胞表现出更不规则的前缘,伴随许多独立的突出与内部形变,表明细胞之间存在稍微不同方向的牵拉。对细胞层内应变的测量证实,OAP缺失的细胞层承受的内部拉扯更少,运动更均一、协调。
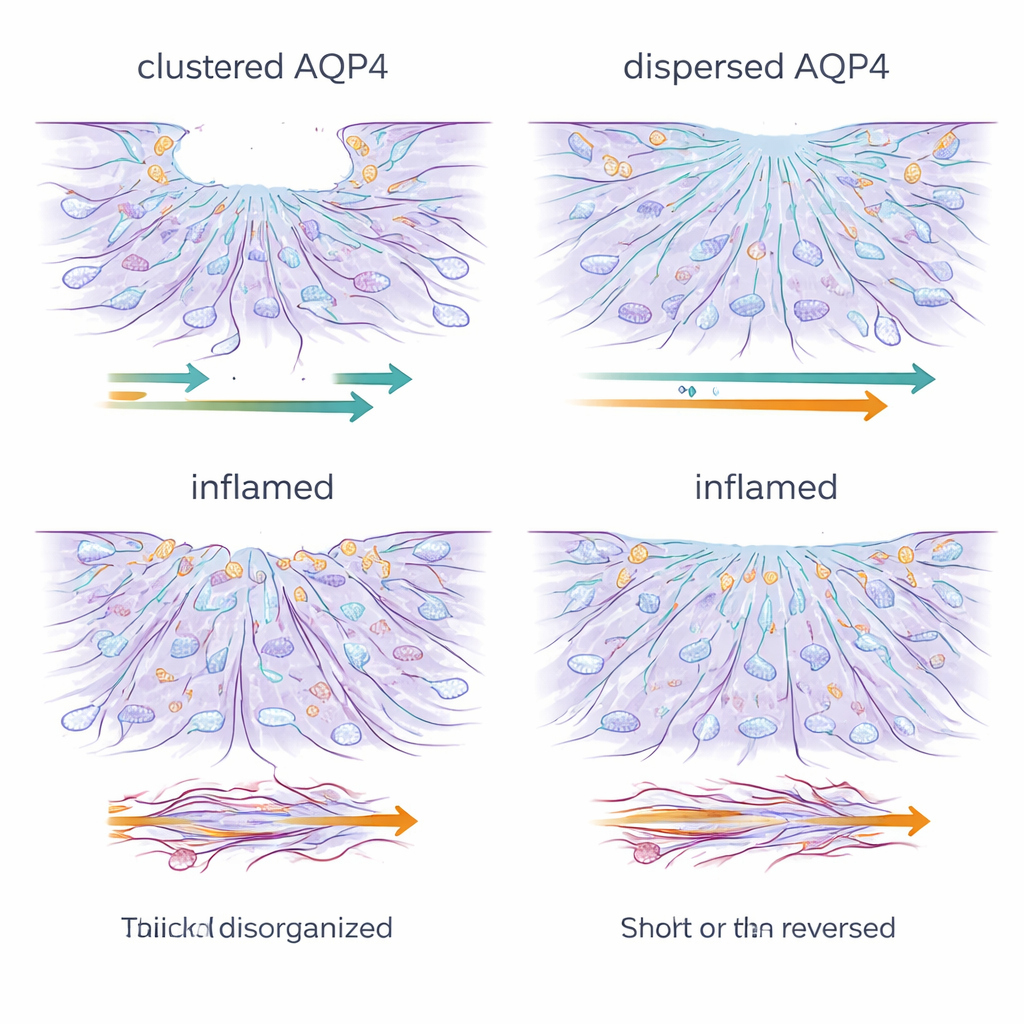
炎症使修复团队停滞并混乱
长期暴露于炎性信号显著改变了这一格局。无论AQP4如何组织,受处理的星形胶质细胞都成为较差的创面修复者:它们几乎不移动,有时甚至向后漂移,扩大了缺口。显微观察显示,向前移动所需的精细动态细胞边缘结构——伪足和丝状伪足——消失,取而代之的是厚重、僵硬的肌动蛋白应力纤维。同时,AQP4和连蛋白‑43(形成星形胶质细胞间通讯通道的关键蛋白)的水平显著下降。原本帮助星形胶质细胞作为协调单元运作的间隙连接网络被破坏,染料传递实验证实远程细胞间通信严重减弱。
这对大脑健康有何意义
这些发现表明,决定星形胶质细胞作为群体高效移动的,不仅是AQP4的含量,还有其排列方式。分散的AQP4似乎能减少细胞间的内部阻力,促进更直、更协调的运动,而大型簇状排列则与更不稳定、拉扯明显的运动方式相关。慢性炎症在很大程度上压倒了这些优势:它重塑细胞骨架、抑制水通道与通讯通道,并将有序的修复队伍变成僵硬且连接不良的细胞片。对非专业读者来说,结论是大脑的水通道与细胞间通信系统不仅被动支持神经元——它们积极影响支持细胞在受伤后的动员方式。理解并最终调整AQP4的组织及炎性信号,可能为改善脑修复、限制瘢痕形成,甚至影响脑肿瘤扩散开辟新路径。
引用: Barile, B., Mennona, N.J., Mola, M.G. et al. Supramolecular aggregation of aquaporin-4 shapes astrocyte collective migration and mechanics. Sci Rep 16, 6021 (2026). https://doi.org/10.1038/s41598-026-35900-z
关键词: 星形胶质细胞, 水通道蛋白‑4, 脑炎症, 细胞迁移, 胶质瘢痕