Clear Sky Science · zh
儿童高分级胶质瘤中BIRC2和BIRC3表达降低与更长生存期相关
为什么儿童脑肿瘤需要新的线索
儿童高分级胶质瘤是最致命的儿童脑肿瘤之一,现有的手术、放疗和化疗仅能使少数患者获益。本研究提出了一个简单但至关重要的问题:这些肿瘤内部是否存在分子层面的“生存开关”,帮助癌细胞逃避死亡?这些开关能否解释为何有些儿童比其他人活得更久?
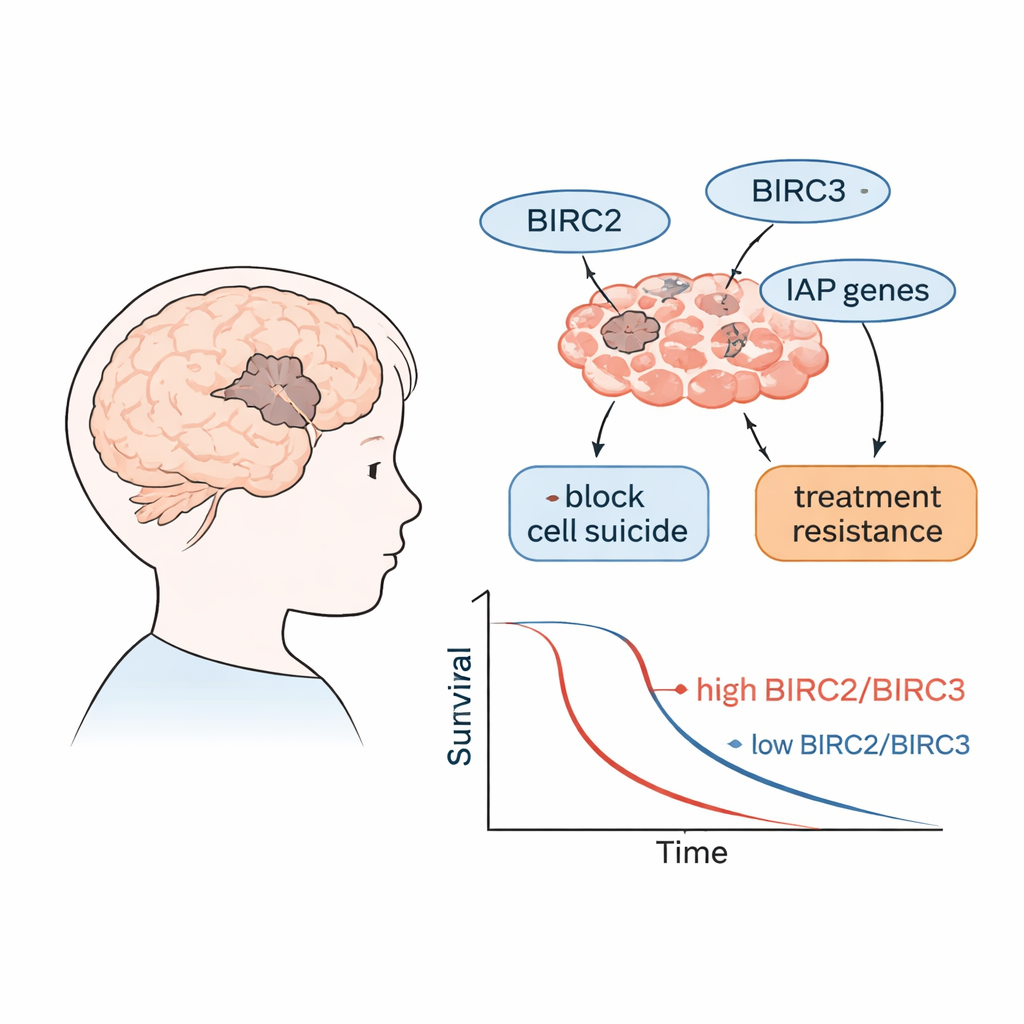
阻止癌细胞死亡的蛋白质
我们的细胞配备有一种内在的自我销毁系统,通常称为程序性细胞死亡或凋亡,用于清除受损或有害的细胞。一类称为IAPs(凋亡抑制蛋白)的蛋白可以阻断这套自毁机制。编码这些蛋白的基因被称为BIRC基因。在许多癌症中,IAPs的表达过高,帮助肿瘤细胞忽视死亡信号并持续生长。研究者关注了该家族的若干成员,包括BIRC2和BIRC3,以及一些与促进或抑制细胞死亡相关的基因,以观察它们在儿童侵袭性脑肿瘤中的活性。
研究来自年轻患者的真实肿瘤样本
研究团队分析了26名年轻患者的肿瘤样本,这些患者均在一所儿科神经肿瘤中心接受治疗,并被诊断为最具侵袭性的胶质瘤。研究者利用手术中取下并保存的组织,测量了多种与细胞存活和死亡相关基因的活性,如BIRC2、BIRC3、BIRC5、BIRC6、BIRC7、NAIP、XIAP、DIABLO、XAF1、CASP3和CASP9。他们还将这些分子读数与临床特征进行了比较:每位患者的生存期、无进展生存期,以及常见肿瘤标志物的存在情况,比如Ki‑67(增殖指标)、PD‑1(免疫检查点)、Olig2、p53、GFAP和一种名为miR‑155‑5p的小型调控RNA。
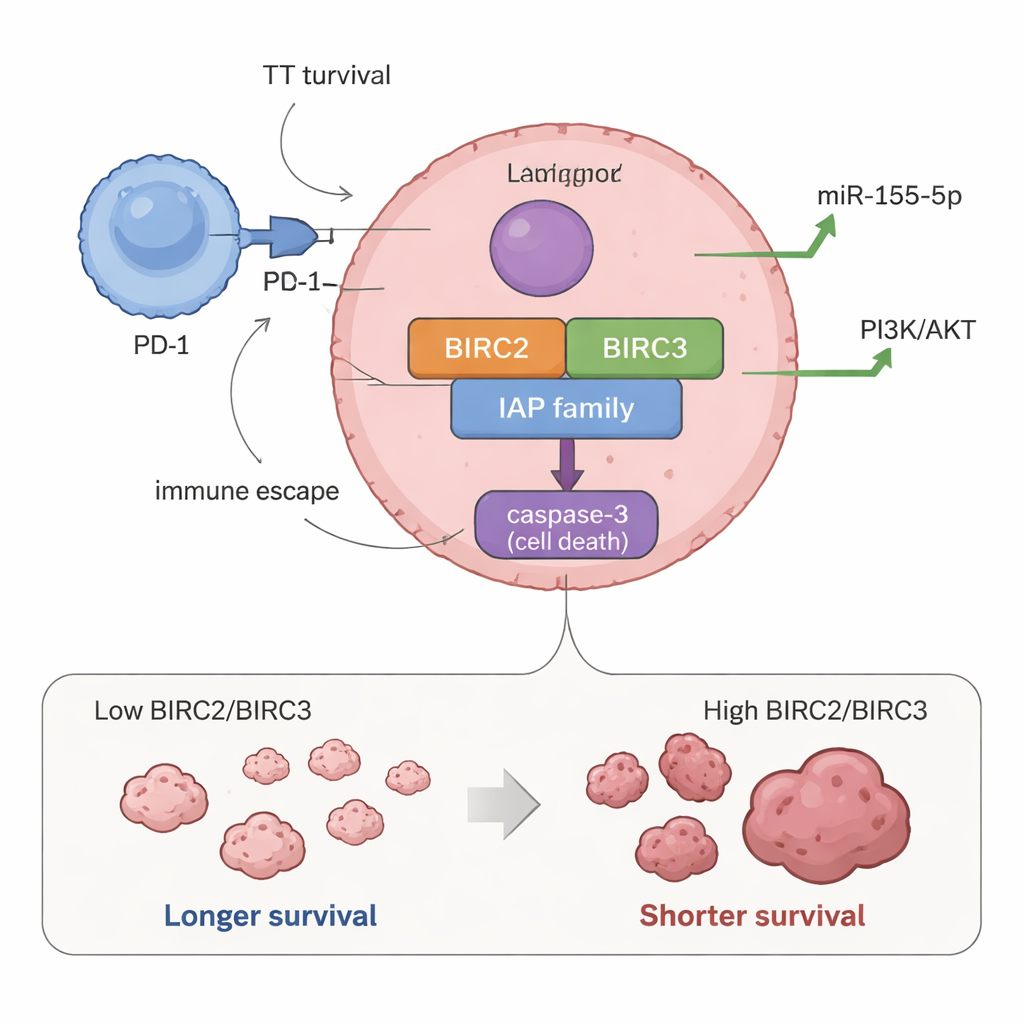
与较短生存期相关的生存开关
当研究者将基因活性与患者结局对比时,有两个基因脱颖而出。那些肿瘤中BIRC2和BIRC3水平较高的儿童,整体生存期和无进展生存期往往更短。换言之,当这些“别死”开关被更强烈激活时,疾病表现得更具侵袭性。高表达BIRC2和BIRC3的肿瘤还与较高水平的miR‑155‑5p相关——这种小RNA此前被证明能推动细胞向生长方向发展并抑制细胞死亡,表明这些分子可能协同作用,使肿瘤对治疗更为顽固。
与肿瘤生长和免疫逃逸的关联
研究还探讨了这些生存开关如何融入更广泛的肿瘤微环境。出人意料的是,一些可促进或调节细胞死亡的基因,如NAIP、BIRC3和XAF1,在缺乏增殖标志物Ki‑67的肿瘤中更为活跃,这提示生长与死亡信号之间存在复杂平衡。较高的BIRC3和XAF1水平倾向于出现在具有更多PD‑1(一种帮助癌症逃避免疫系统的关键“刹车”)表达的肿瘤中。此外,执行细胞死亡的核心分子CASP3的更高活性与PD‑1表达有强关联,提示癌细胞与免疫细胞之间的相互作用可能会重塑肿瘤内死亡机制的使用或阻断方式。
这对未来治疗可能意味着什么
对面对儿童高分级胶质瘤的家庭和临床医生来说,这些发现暂时不会改变现有治疗,但提供了重要线索。研究表明,尤其是BIRC2的高活性(以及可能的BIRC3)标志着更具耐受性、易复发的肿瘤,使这些基因成为不良预后潜在的警示信号。由于IAP蛋白已在成人癌症中作为药物靶点被研究,新的结果提出了这样的可能性:旨在关闭这些生存开关的药物将来可能与现有的脑肿瘤治疗或针对PD‑1的免疫疗法联合使用。本研究规模较小且具有探索性,其结论需在更大样本和蛋白水平上得到确认,但它指向了这样一种未来:通过检测这些关键开关来更好地预测儿童肿瘤的结局,并最终为更有针对性、更有效的治疗提供指导。
引用: Petniak, A., Gil-Kulik, P., Zarychta, J. et al. Reduced expression of BIRC2 and BIRC3 associated with longer survival in pediatric high-grade gliomas. Sci Rep 16, 6665 (2026). https://doi.org/10.1038/s41598-026-35887-7
关键词: 儿童脑肿瘤, 胶质瘤, 细胞凋亡, BIRC2 BIRC3, 免疫治疗