Clear Sky Science · zh
人绒毛膜促性腺激素在炎性小鼠新生儿缺氧缺血模型中减少脑囊性软化和抑钙蛋白阳性中间神经元退变
为何一种孕期激素与新生儿大脑有关
当婴儿的大脑在出生前后缺氧时,这种损伤可能导致终生问题,如脑瘫、癫痫或学习困难。医生试图通过降温治疗来限制这种损伤,但当感染或炎症同时存在时,降温的疗效有限。本研究提出了一个令人意外的问题:人绒毛膜促性腺激素(hCG)——即妊娠试验中检测到的那种激素——在缺氧和炎症同时发生时是否能保护新生儿大脑?
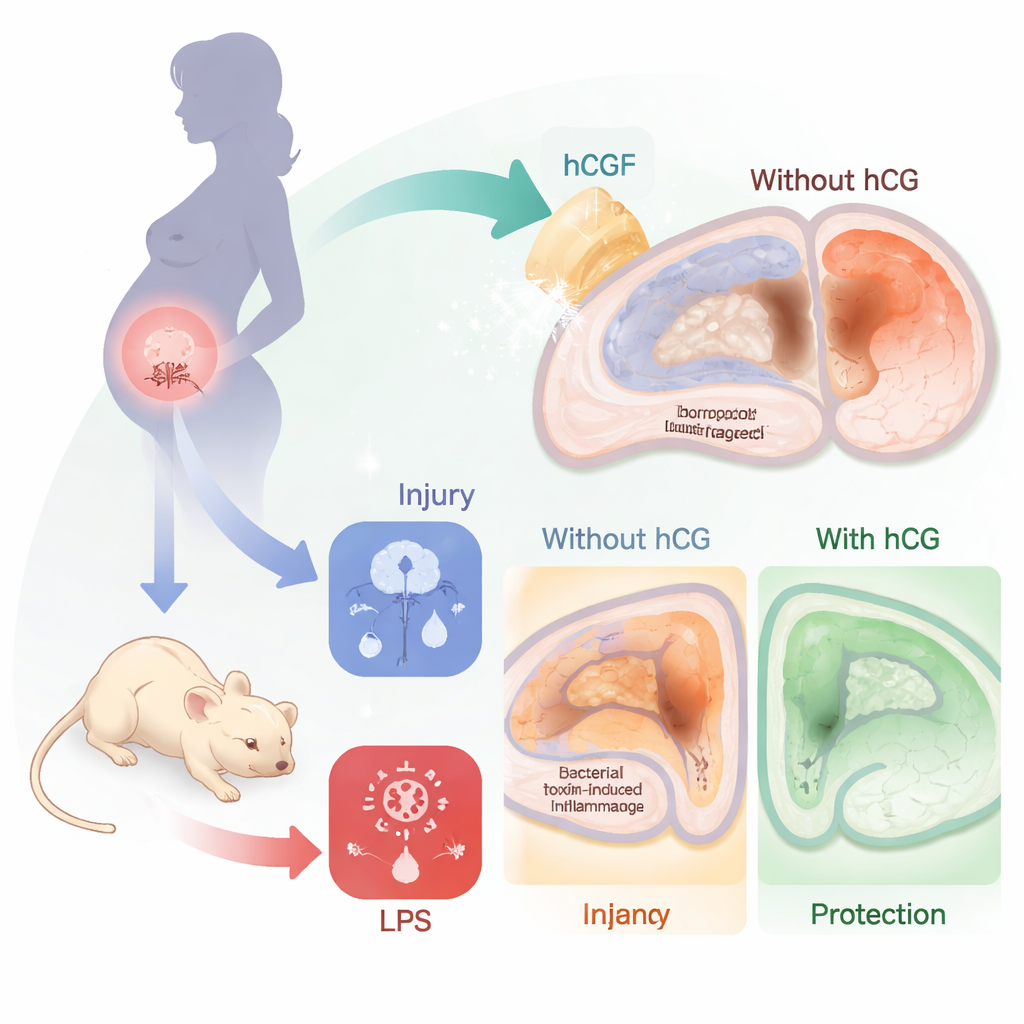
缺氧、感染与对大脑的双重打击
在现实中,重症新生儿常常同时面临多个问题。大脑缺氧和血流不足,称为缺氧缺血,已经会触发肿胀、细胞死亡和长期瘢痕形成。感染或强烈炎症通过激活脑内外的免疫细胞使情况恶化。此前在动物和人类中的研究已表明,当存在强烈炎性信号时,当前的主要治疗——治疗性降温——效果有限。因此,作者建立了这种“二重打击”的模型——缺氧缺血加炎症——并检验hCG是否能减轻由此产生的脑损伤。
在小鼠中构建类似新生儿的大脑损伤模型
研究人员使用的鼠龄大致对应足月人类新生儿。他们先向鼠仔注射脂多糖(LPS),这是一种来自细菌细胞壁的分子,可强烈激活免疫系统。十八小时后,他们短暂中断大脑一侧的血流并让鼠仔暴露于低氧环境,重现一次短暂但有害的缺氧缺血事件。这种组合产生的脑损伤比单纯缺氧更严重,包括海马和大脑皮层出现肉眼可见的充满液体的空腔,这些区域对记忆和高级认知至关重要。研究组还观察到一类由抑钙蛋白标记的抑制性神经元显著丧失,这些细胞有助于维持大脑活动的平衡,在发育性和运动障碍中常被破坏。
检验一种天然孕期激素的保护作用
为了观察hCG是否能减轻这些损伤,另一组鼠仔在炎性触发前两小时接受了单次hCG剂量。数日后检查其大脑时,差异明显。接受hCG的鼠仔在海马和皮层中的囊状空洞更少且更小,这些区域的总体组织丢失明显低于仅接受生理盐水的鼠仔。重要的是,hCG治疗并未抑制生长或引起明显副作用,表明在该模型中所用的保护剂量耐受性良好。
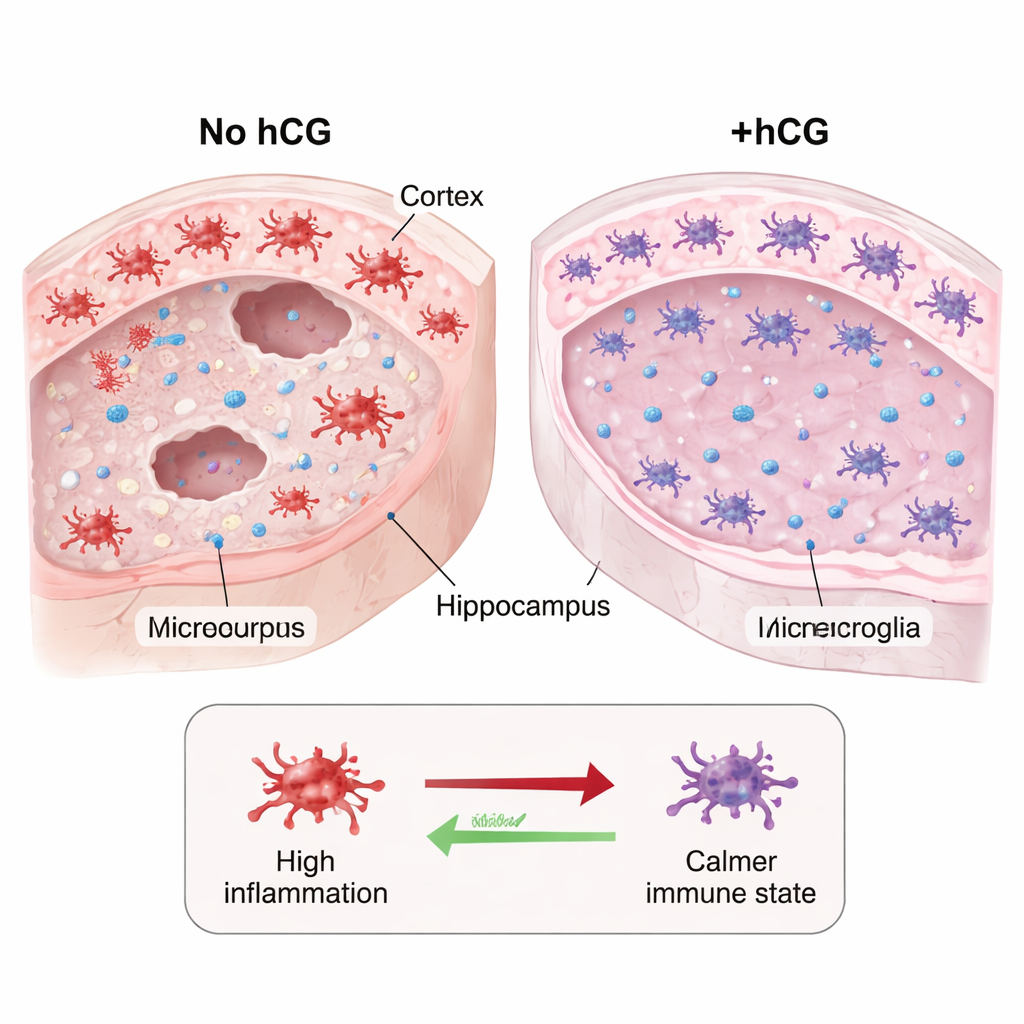
保全易受损细胞并抑制脑内免疫活动
随后研究进一步观察了哪些脑细胞得到了保护。在未处理的小鼠中,联合损伤后皮层、纹状体和海马中的许多抑钙蛋白阳性中间神经元丧失。接受hCG处理的动物中,这类细胞保留得多得多,抑钙蛋白染色得以保存。同时,关键区域中激活的小胶质细胞——用标记物Iba1标记——数量在hCG处理组也较少。鉴于已知hCG能将免疫反应转向较低炎性状态并在其他情境中支持神经元存活,这些发现提示其可能既通过平抑有害炎症又通过直接滋养易受损的神经细胞来保护新生儿大脑。
这对未来护理可能意味着什么
对非专业读者来说,核心信息是:一种在妊娠期自然产生的激素在小鼠中能够降低由缺氧和炎症共同引起的脑损伤。尽管这项工作仍处于早期临床前阶段,并且使用的是损伤前的预防性给药,但它提示hCG或类似作用的药物可能成为增强高风险新生儿现有治疗的有前景候选。如果未来研究确认在损伤后及与降温联合使用时hCG是安全且有效的,它有朝一日报帮助更多婴儿避免围产期严重并发症后常见的长期残疾。
引用: Miller, B., Crider, A., Aravamuthan, B. et al. Human chorionic gonadotropin decreases cerebral cystic encephalomalacia and parvalbumin interneuron degeneration in a pro-inflammatory model of mouse neonatal hypoxia-ischemia. Sci Rep 16, 6851 (2026). https://doi.org/10.1038/s41598-026-35852-4
关键词: 新生儿脑损伤, 缺氧缺血性脑病, 炎症, 人绒毛膜促性腺激素, 抑钙蛋白中间神经元