Clear Sky Science · zh
KIN17通过PI3K-AKT-mTOR通路促进肾脏肿瘤的起始和进展
这项肾癌研究为何重要
肾癌的检测率在上升,但对许多患者而言,一旦癌症扩散仍然难以控制。本研究通过显微镜下——深入到癌细胞内分子层面——探究驱动肾脏肿瘤生长和侵袭的机制,并评估一种实验性药物是否能遏制这一过程。研究结果指向一个鲜为人知的蛋白质——KIN17,作为肾癌的新型促癌因子,并提出了通过口服药物间接针对这一靶点的可能策略。
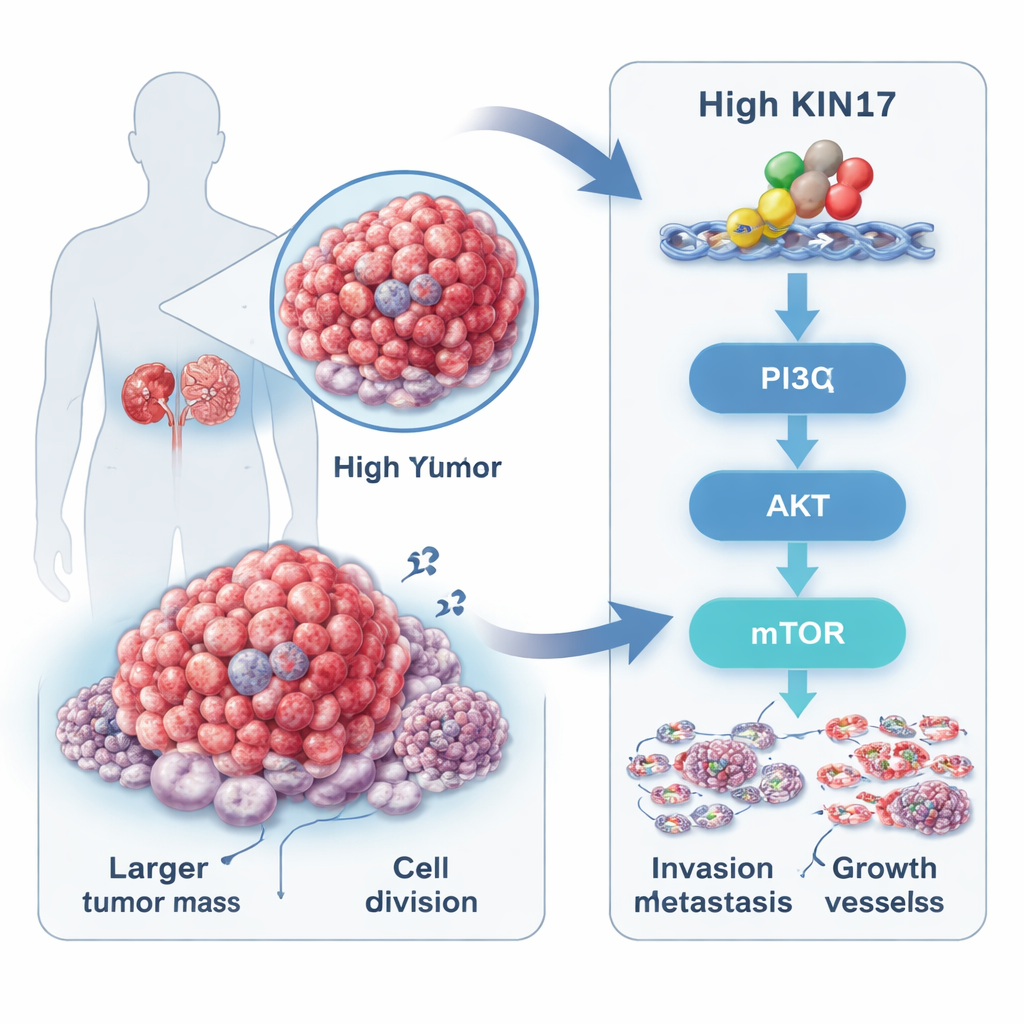
肾脏肿瘤中的一个隐匿驱动因子
肾细胞癌是最常见的肾癌类型,常常起病无症状,且常在晚期才被发现。研究者关注了名为KIN17的蛋白,长期以来它以在DNA保护和复制中的作用为人所知,但最近才被发现与多种癌症相关。通过分析公开的癌症数据库和88例患者的肿瘤样本,他们发现肿瘤组织中KIN17表达明显高于邻近的非癌组织。肿瘤中KIN17含量高的患者通常肿瘤体积更大、分级更高、分期更晚、远处转移更多,且总体生存时间短于低KIN17患者。这一模式表明KIN17并非旁观者,而是与肿瘤侵袭性密切相关。
在癌细胞中检验KIN17的作用
为了解KIN17在肾癌细胞内的实际作用,团队构建了实验室细胞系,分别下调或上调KIN17。当他们降低KIN17表达时,细胞增殖变慢、克隆形成减少,迁移和穿透人工基质的能力下降。更多细胞停留在细胞周期的静止期并进入死亡程序,显示出更高的凋亡水平。相反,过表达KIN17时细胞增殖加快,DNA复制更活跃,封闭划痕样细胞间隙更迅速,侵袭性增强。这些实验表明KIN17像加速踏板一样推动肾癌细胞的生长和扩散。
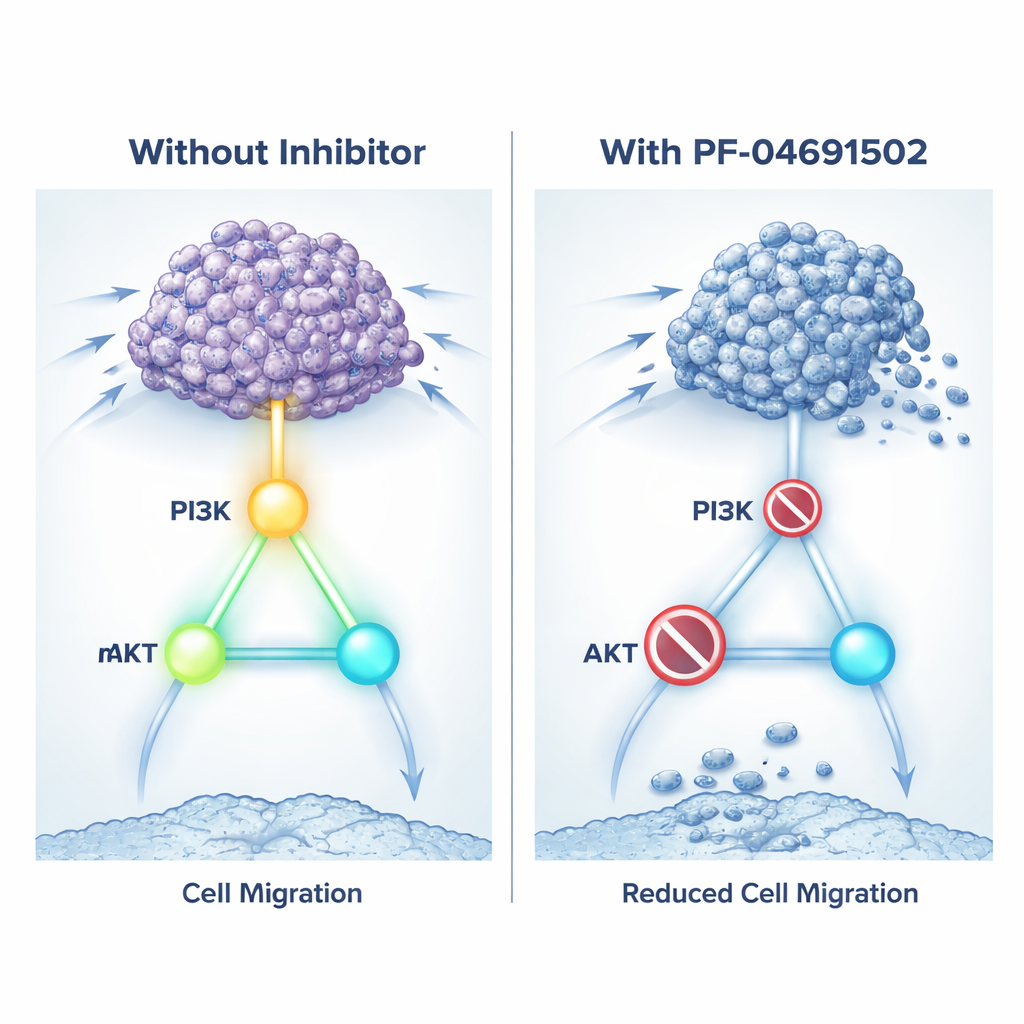
被捕捉到的生长通路
研究者接着探究KIN17如何发挥作用。基因表达和蛋白质检测显示出细胞内一个著名的生长与存活网络——PI3K–AKT–mTOR通路的参与。该通路常被比作一个中心控制枢纽,指示细胞何时生长、分裂并避免死亡。高表达KIN17的肾癌细胞在该通路关键组分上具有更高的“激活”信号——以磷酸化修饰表现——尽管这些蛋白的总量并未显著改变。当降低KIN17时,这些激活标记减少,与细胞运动和侵袭相关的分子也发生了变化。在小鼠实验中,由高KIN17细胞形成的肿瘤长得更大更快,组织染色也显示该生长通路在这些肿瘤中高度激活。
用双重抑制药物压低信号
由于现有药物尚不能直接抑制KIN17,团队尝试了另一种策略:关闭它所控制的生长通路。他们使用了PF‑04691502,这是一种同时抑制PI3K和mTOR的实验性药物,是通路上的两个关键开关。在体外培养中,对高KIN17的肾癌细胞施用该抑制剂后,细胞增殖减慢、迁移与克隆形成能力下降,并促使更多细胞走向死亡。该药物还降低了PI3K、AKT和mTOR的磷酸化水平,并减少了与侵袭相关蛋白的表达。在携带肾肿瘤的小鼠中,每日给药使过表达KIN17的肿瘤缩小,细胞分裂标记减少而细胞死亡信号增加。简言之,该药物通过沉默这一偏好的生长通路,削弱了KIN17的有害作用。
这对患者可能意味着什么
对面临肾癌的患者而言,这些发现提出了两个有希望的方向。首先,检测肿瘤样本中的KIN17水平可能帮助医生评估癌症的侵袭性及其转移风险。其次,严重依赖KIN17的肿瘤可能对抑制PI3K–AKT–mTOR通路的药物特别敏感,例如PF‑04691502或其他正在临床试验中的双靶点抑制剂。尽管要将任何新治疗推向临床仍需大量后续工作,这项研究绘制出了一条清晰的因果链——从KIN17,通过关键生长通路,至失控的肿瘤扩张——并证明切断这条链可以在实验室和动物模型中减缓肾癌进展。
引用: Wen, Y., Lyu, L., Zhang, H. et al. KIN17 facilitates the initiation and progression of renal tumor progression through the PI3K-AKT-mTOR pathway. Sci Rep 16, 5721 (2026). https://doi.org/10.1038/s41598-026-35851-5
关键词: 肾细胞癌, KIN17, PI3K AKT mTOR, 靶向治疗, PF-04691502