Clear Sky Science · zh
抗PD1治疗进展时晚期黑色素瘤患者来源的细胞外囊泡蛋白含量发生变化
为什么血液中微小信使可能预示癌症治疗效果
对于晚期黑色素瘤患者,强效的新型免疫疗法有时能使肿瘤缩小消失——但在许多病例中,癌症很快反扑。该研究考察了肿瘤释放到血液中的微观“包裹物”,以确定它们是否能在无需活检的情况下、及早揭示谁可能从抗PD1治疗中获益,谁可能需要其他策略。
小囊泡,大线索
我们的血液中携带着无数纳米级小囊泡,称为细胞外囊泡。这些是被膜包裹的微小包裹,细胞用它们来发送分子信号。癌细胞也会释放这些囊泡,并把反映肿瘤及其微环境状况的蛋白质装入其中。因为这些囊泡在循环系统中自由存在,可以从简单的血样中分离出来,而不必切取肿瘤组织。研究人员想知道,晚期黑色素瘤患者血中囊泡的蛋白货物是否能在抗PD1免疫疗法(这一类广泛使用的药物通过“松开”免疫细胞的制动来发挥作用)开始前或早期提示个体的治疗反应。
随访患者治疗过程
研究团队对九名接受抗PD1药物治疗的晚期黑色素瘤患者进行了研究。血样在三个时点采集:治疗开始前、首次给药后不久,以及在疾病进展时或如果未进展则在九个月时采集。从每个样本中,科学家们分离出细胞外囊泡并使用高端质谱技术记录其蛋白质组成。经过严格的数据筛选,他们侧重于969种可靠测量的蛋白质。随后将这些蛋白质分组为代表主要生物过程的网络——例如免疫活性、细胞黏附、血液凝固和能量代谢——并比较这些模式在疾病受控的患者与肿瘤持续生长的患者之间的差异。
蛋白模式中蕴藏的早期反应信号
即使在治疗开始前,囊泡也已在最终的应答者与非应答者之间呈现差异。后来表现较好的患者,其囊泡通常富含与细胞间接触和某些对紫外线的保护性反应相关的蛋白——紫外线是皮肤癌的关键因素。相反,一些免疫相关蛋白和炎症标志在随后出现疾病进展的患者中更为丰富,这暗示一种“热但方向错误”的免疫环境可能会削弱疗效。通过聚焦于单个分子,研究人员构建了一个由八种蛋白组成的特征签名——本质上是蛋白水平的加权组合——将患者分为高风险和低风险两组,预测疾病早期恶化。在这组小样本中,该签名显示出有前景的区分能力。
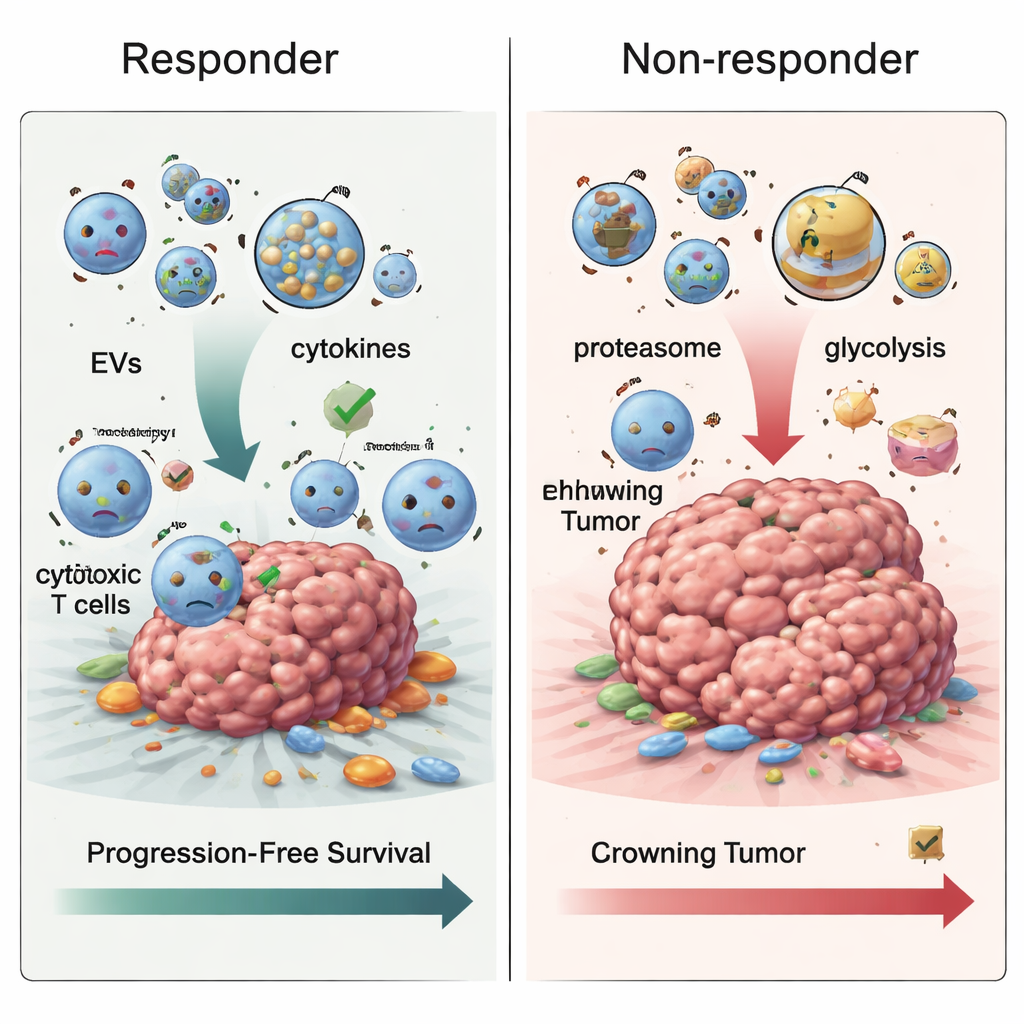
耐药可能随时间如何发展
当团队检查治疗开始后采集的样本时,出现了另一种模式。在病情进展的患者中,细胞外囊泡中富集了参与细胞废物处理机器——即蛋白酶体——的蛋白,以及参与能量生产路径(如糖酵解,许多肿瘤依赖的糖类燃烧过程)的蛋白。这些变化与耐药肿瘤通过重塑代谢和蛋白质处理来在免疫攻击中存活的想法相吻合。将三个时点的变化一起追踪,研究人员还观察到在非应答者中与血液凝固相关的蛋白随时间倾向于下降,而与向免疫系统呈递肿瘤片段相关的蛋白则升高——但矛盾的是,这并未转化为更好的肿瘤控制,表明这些信号被打包进囊泡的方式可能实际上阻碍了有效的免疫杀伤。
这对患者意味着什么
简而言之,该研究表明血流中的微小囊泡携带着关于黑色素瘤肿瘤与免疫系统在抗PD1治疗下相互作用的详细分子指纹。在治疗前和治疗期间测得的这些囊泡中特定蛋白模式,可能帮助医生预测谁更有可能获得更长时间的疾病控制,以及谁可能因炎症和代谢改变而出现耐药。尽管该工作仅基于九名患者,需要在更大队列中得到验证,但它指向一个前景:通过常规抽血即可指导并调整黑色素瘤免疫疗法,使这些强效药物更精准、更有效。
引用: Trilla-Fuertes, L., Gámez-Pozo, A., Laso-García, F. et al. Protein content of extracellular vesicles from patients with advanced melanoma changes upon progression to anti-PD1 therapy. Sci Rep 16, 5891 (2026). https://doi.org/10.1038/s41598-026-35848-0
关键词: 黑色素瘤 免疫疗法, 细胞外囊泡, 血液生物标志物, 抗PD1 耐药, 蛋白质组学