Clear Sky Science · zh
用于硼中子俘获治疗的表面引导患者定位系统的开发与评估
更精准地瞄准抗癌中子束
硼中子俘获治疗(BNCT)是一种有前景的癌症疗法,能够选择性地损伤肿瘤细胞,同时尽可能保护周围健康组织。但要实现这种精确性,医生必须将患者精确地放置在固定中子束前——经常需要达到毫米级精度。本文介绍了一种新的相机与机器人引导的定位系统,旨在让这一精细布位更快速、更准确,并减少对技师稳定操作与主观判断的依赖。
为何定位如此重要
与许多能围绕患者旋转并重塑射线束的现代放疗设备不同,BNCT依赖的是重量大、固定的中子源,束流的调整选项有限。必须由患者移动到恰当位置,而不是转动光束。传统上,工作人员使用激光、皮肤记号和手动床位移动来完成这一过程。该流程既慢又高度依赖操作人员技能,且可能留下小的定位误差,从而改变肿瘤及邻近器官实际接受的剂量。随着BNCT中心开始用于头颈等复杂、难以到达部位肿瘤的治疗,这些限制成为了一个严重障碍。
高科技助手:相机、软件与机器人
为了解决这一问题,研究团队构建了一套集成的表面引导BNCT(SG‑BNCT)系统,结合了三大部分:名为NeuMANTA的专用治疗计划软件、一对双目立体视觉相机,以及载有治疗床的六轴工业机器人。在NeuMANTA中,医生在CT图像上规划BNCT治疗,标注中子束通过的确切点位和患者皮肤上的三个小参考点(或称配准标记)。这些标记在计划图像中定义了患者的位置,并通过数学变换矩阵将该计划与真实治疗室坐标系关联起来。
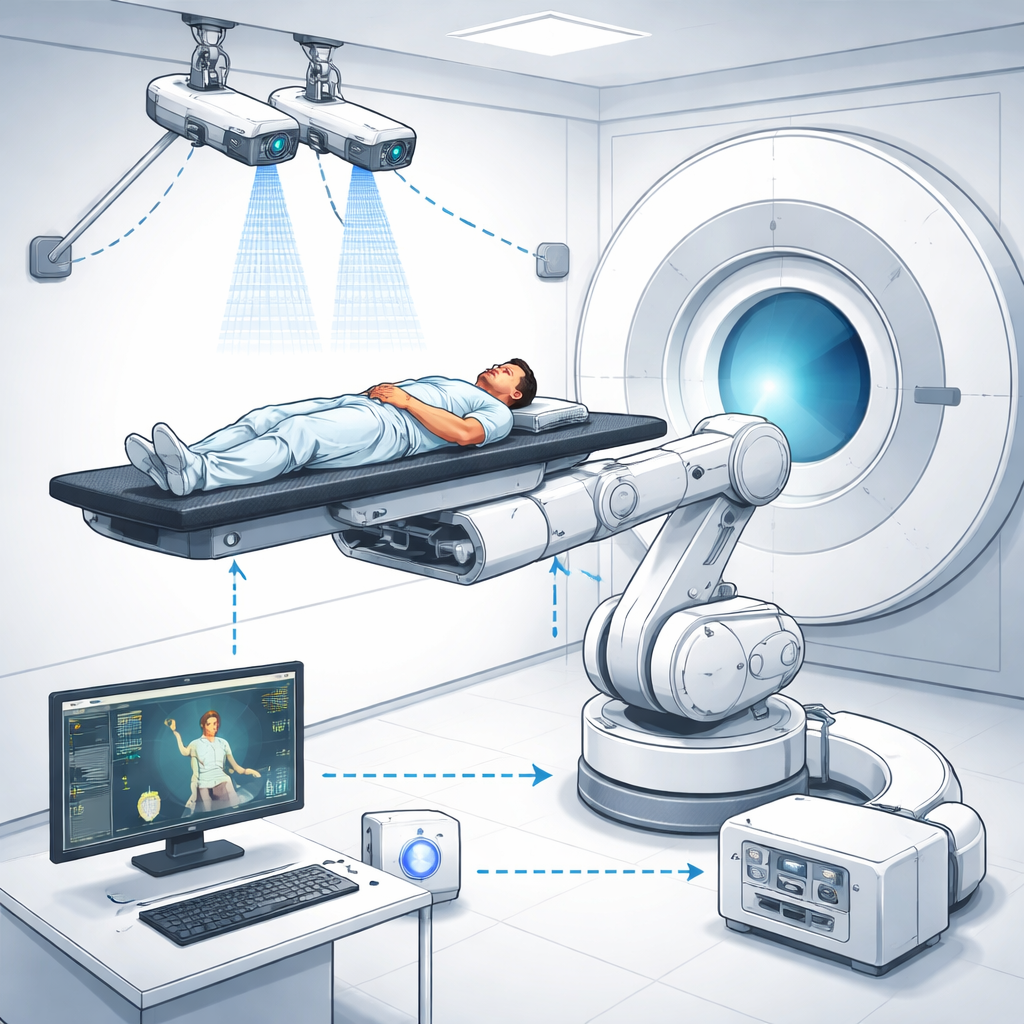
3D相机如何观察并校正布位
在治疗室内,两台高分辨率相机从不同角度监视患者,类似于人眼。系统使用在一千多张图像上训练的现代目标检测算法(YOLO)快速识别患者表面的相同配准标记。通过比较每个标记在左右相机视图中的呈现方式,计算机重建它们的三维位置并生成详细的表面点云。利用三个非共线标记,系统重建出患者坐标系并将其与治疗计划中定义的坐标系进行比较。计划位置与实际位置之间的任何不匹配都会被转换为平移与旋转指令——共六个自由度——发给支撑治疗床的工业机器人。
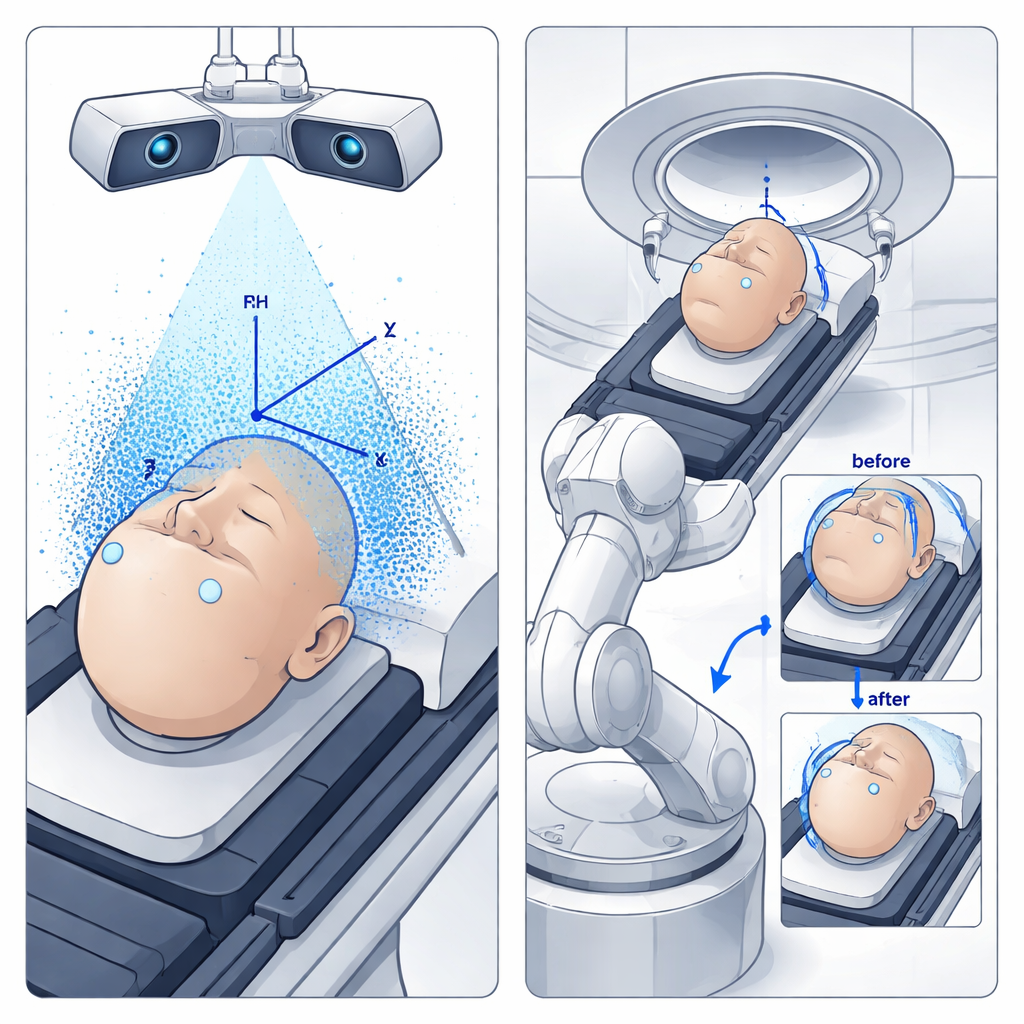
使用替代患者进行测试
在将系统用于真实患者之前,团队用一具具有解剖特征的模型人(人形体模)进行了测试,该体模配有在CT扫描中及相机可见的内部与表面标记。他们在NeuMANTA中创建了多个不同束向的治疗布位,然后让SG‑BNCT系统通过自动移动体模来复现这些计划。放置在中子束孔中心的激光作为实际束的替代,因此研究者可以直接测量体模最终位置与目标的偏差,包括沿束轴方向(源到皮肤的距离)以及垂直于束轴平面内的侧向偏差。
系统达到了多接近的精度?
在24组实验布位中,系统的定位误差在两方向上通常均低于1毫米,单次移动中最差的误差沿束轴约为2到3毫米。作者将这些残留差异归因于三个主要来源:CT图像层厚、立体相机的小幅校准不确定性,以及软件检测标记时的像素级微小不精确。重要的是,该系统设计为闭环工作:它反复重新测量标记位置、更新三维对齐并指令机器人做进一步精细运动,直到剩余误差低于预设阈值。在这些迭代测试中,最终偏差持续降至远低于1毫米,在深度和侧向两个方向均实现了亚毫米级对齐。
这对患者意味着什么
对于可能从BNCT获益的患者——尤其是位于复杂或敏感部位的肿瘤患者——这种表面引导、机器人辅助的定位系统有望提供更可靠、更高效的治疗。通过将治疗计划软件直接与能看到真实患者的相机以及能执行精确运动的机器人连接,该方法减少了对手动激光对齐和人为猜测的依赖。尽管当前版本在实时运动跟踪方面速度仍不够,且迄今仅进行了静态测试,但结果表明该技术可常规实现亚毫米精度的患者定位。随着速度改进和硬件的耐辐射化,该方法有望成为临床上更安全、更一致的BNCT治疗的可靠支撑。
引用: Chen, J., Xie, QL., Ping, JJ. et al. Development and evaluation of surface-guided patient position system for boron neutron capture therapy. Sci Rep 16, 5818 (2026). https://doi.org/10.1038/s41598-026-35834-6
关键词: 硼中子俘获治疗, 患者定位, 立体视觉, 医疗机器人, 表面引导