Clear Sky Science · zh
两种获得性癫痫大鼠模型中基因表达和甲基化改变的共性
为何基因变化与癫痫有关
癫痫影响数百万人,其中约三分之一患者的癫痫发作无法被现有药物完全控制。大多数药物只是抑制大脑中的电活动风暴,但并不能阻止癫痫本身的发生。该研究探讨了DNA上的持久化学标记以及基因开关的变化,是否能解释一个健康大脑如何变为癫痫状态——以及这些变化在不同类型的疾病中是否存在共性。
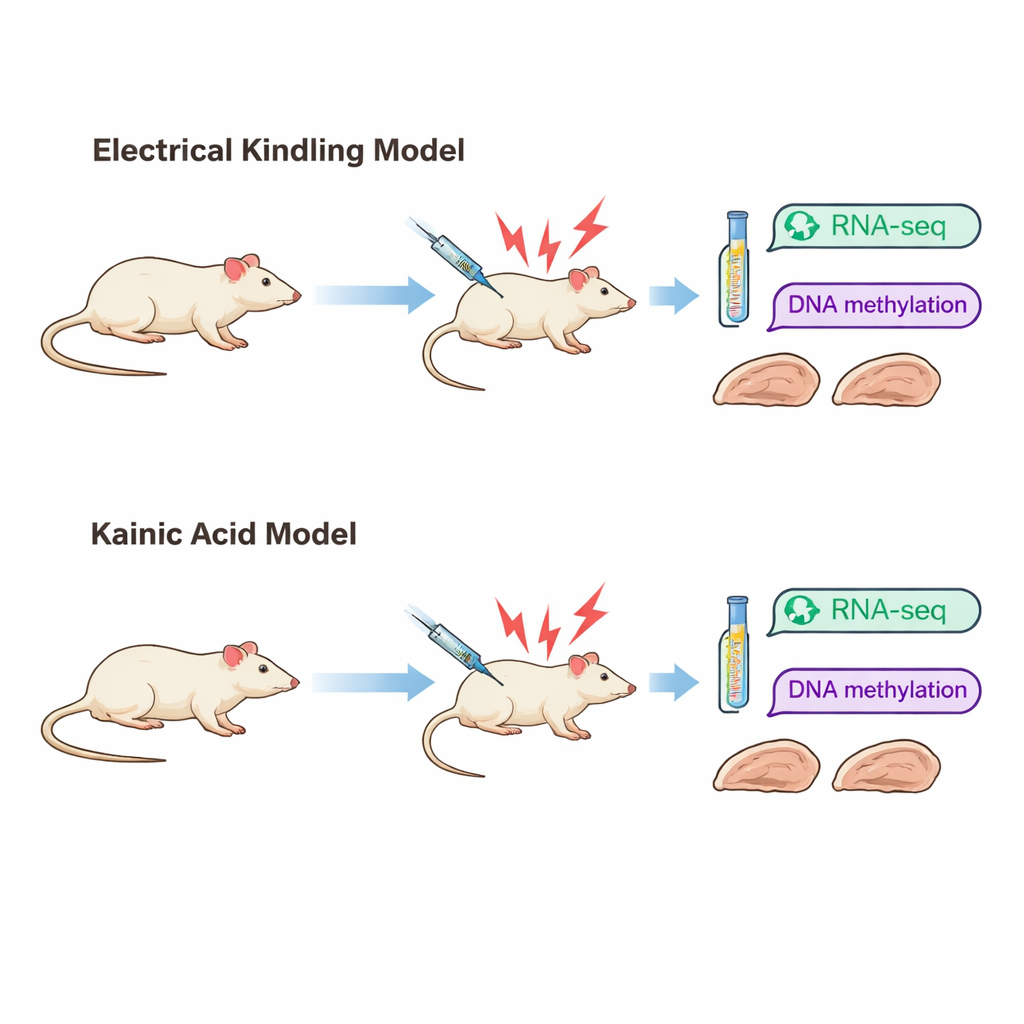
通向相同疾病的两条不同路径
研究人员聚焦于颞叶癫痫,这是一种常见且常常难以治疗的癫痫类型。他们使用了两种成熟的大鼠模型,模拟癫痫产生的不同途径。在“点燃(kindling)”模型中,对海马的一部分反复施加短暂电刺激,逐渐使发作变得容易被诱发。在“鼠曲霉酸(kainic acid)”模型中,一种化学物质引发强烈的癫痫发作,随后会在较晚出现自发性发作。尽管两种模型最终在外观上都表现为严重的痉挛性发作,但其脑损伤特征截然不同。点燃模型的大鼠组织结构大体保留,而接受鼠曲霉酸处理的大鼠在海马关键区域表现出明显的细胞丧失和瘢痕形成。
解读大脑的基因活动
为了观察这些不同通路在分子水平上如何影响大脑,团队在每种模型大鼠经历三次严重发作后检查了海马。他们通过RNA测序测量基因的活跃程度,并使用一种称为减少代表性亚硫酸氢盐测序(reduced-representation bisulfite sequencing)的方法绘制DNA上的甲基化标记图谱。基因活性变化反映了细胞如何响应和适应,而甲基化标记通常被视为一种更长期的“记忆”,可影响基因的开启或关闭。
基因活性变化超越DNA标记
两种模型产生了显著不同的基因活性模式。点燃模型中变化的基因数量比鼠曲霉酸模型多出十倍以上。然而,当研究者将两份基因名单重叠时,仍发现有一百多个基因在两种模型中都有变化,而且大多数变化方向一致。一个例子是Mmp9,这个基因与脑细胞重塑其连接以及与发作相关的损伤有关;它在两种模型中都显著上调。这些共同的变化表明,即使初始触发因素和可见的脑损伤不同,癫痫发生过程也存在核心的基因响应。
DNA标签讲述不同的故事
当研究团队检查DNA甲基化时,情况有所不同。两种模型都显示出许多基因的甲基化发生改变,并且两者之间存在相当数量的重叠。然而,在同一模型中同时表现出甲基化和表达改变的基因仅是适度的子集,而在两种模型中都这样表现的基因则更少。在一些共同的基因中,例如Nedd9和Ptpre,表达在两种模型中都上升,但个别位点的DNA甲基化变化方向在模型之间可能是相反的。总体来看,并不存在一个简单的“甲基化增加就意味着基因活性降低”或反之的规律。这表明,在这些癫痫模型中,大多数基因活性变化并非由广泛的DNA甲基化变化直接驱动。
这对未来治疗的意义
对于期望更好癫痫疗法的人来说,这些发现既带来警示也提供指引。研究表明,在癫痫发展过程中开启的基因程序可能具有很强的模型特异性,而且DNA甲基化只是更大、更复杂的调控图景中的一部分。在单一动物模型中识别出的有希望的基因靶点可能无法泛化,因此在向人体治疗推进之前,应在多种模型中进行验证。与此同时,那些在不同模型中在表达和甲基化上都发生变化的少数基因,可能代表开发旨在改变疾病进程的疗法的更可靠起点,这类疗法的目标不仅是抑制发作,而是阻止癫痫的形成。
引用: Purnell, B.S., Hur, J., Ruskin, D. et al. Commonalities in gene expression and methylation changes across two rat models of acquired epilepsy. Sci Rep 16, 5095 (2026). https://doi.org/10.1038/s41598-026-35826-6
关键词: 癫痫发生, DNA甲基化, 基因表达, 颞叶癫痫, 大鼠模型