Clear Sky Science · zh
KChIP1 剪接变体通过促进 P/C 型失活特征调节 Kv4 通道
微小孔道如何塑造大脑的电节律
大脑中的每一次思考、记忆和运动都依赖于神经细胞中的快速电信号。这些信号由微观孔道——离子通道——精细调控,允许带电粒子进出细胞。本文探讨了一种辅助蛋白 KChIP1 的细微变异如何显著改变一种通道家族(Kv4 通道)的行为,从而改变神经元发放重复电活动的难易程度。
作为大脑制动踏板的钾通道
Kv4 通道承担所谓的 A 型钾电流,该电流在神经元的胞体和树突中开启和关闭都很迅速。此电流有助于确定神经元的发放阈值以及它在低频输入下跟随信号的保真度。Kv4 通道并非独立工作:它们与辅助蛋白组装成三元复合体,包括 DPP 蛋白和 KChIP 蛋白。这些伙伴影响通道关闭的速度以及它们重新准备开启的速率。此前的大多数研究认为 KChIP 通常使 Kv4 通道在关闭后更快恢复,从而使神经元能够迅速响应重复输入。
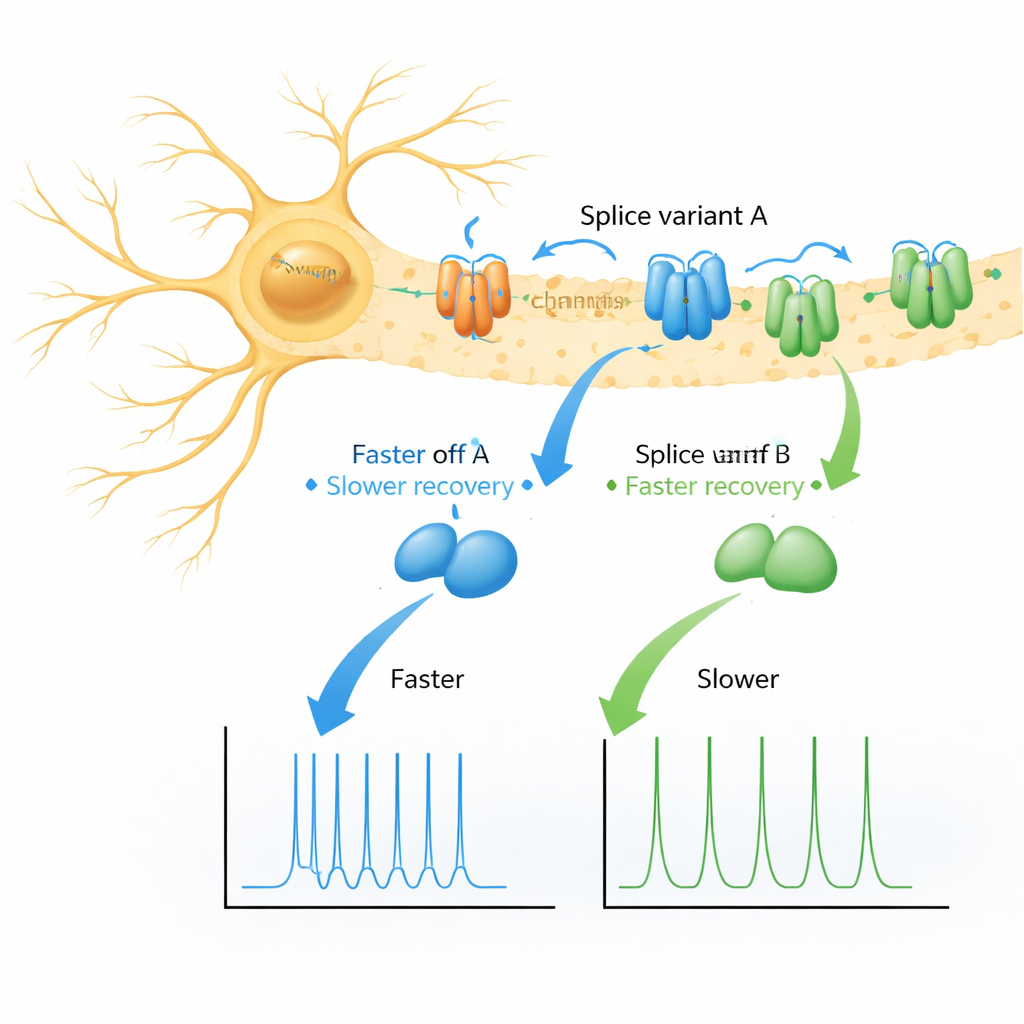
两种蛋白变体,两种恢复模式
作者集中研究了 KChIP1 的两种几乎相同的剪接变体,称为 1a 和 1b,它们仅在 1b 的 N 端有一段短的芳香族“尾巴”不同。研究者在蛙卵细胞这一受控试验平台上表达了几种 Kv4 通道类型:单独表达、与每种 KChIP1 变体共表达、与 DPP 共表达,或与两种辅助蛋白同时共表达。正如预期的那样,1a 和 1b 都在电压台阶过程中轻微改变了通道的关闭行为,但并未引起剧烈变化。令人意外的是在检查通道关闭后恢复的过程时:与 1a 或 1b 配对的通道并非单一、平滑地恢复就绪状态,而是显示出两个不同的恢复阶段——一个快速阶段和一个慢得多的阶段,其中 1b 导致的慢通路占比明显更大。
揭示一个隐匿的慢通路
当 Kv4 通道在没有 KChIP1 的情况下表达时,它们沿一条简单的快速通路恢复,DPP 的存在甚至使恢复更快。加入 KChIP1 改变了这一模式。与 1a 一起时,大多数通道仍然快速恢复,但有一小部分通道绕道进入慢恢复。与 1b 一起时,进入慢通路的通道比例大得多,使恢复时间延长到秒级。这一效应在所有测试的 Kv4 亚型中都出现,并且即便在存在 DPP 时也持续存在,表明慢通路是 KChIP1 含量复合体的内在特性,而非特定通道或实验设置的伪像。作者还发现 1b 将通道的“关闭”电压范围向更负方向移动,进一步使它们在持续活动中更倾向于处于不可用状态。
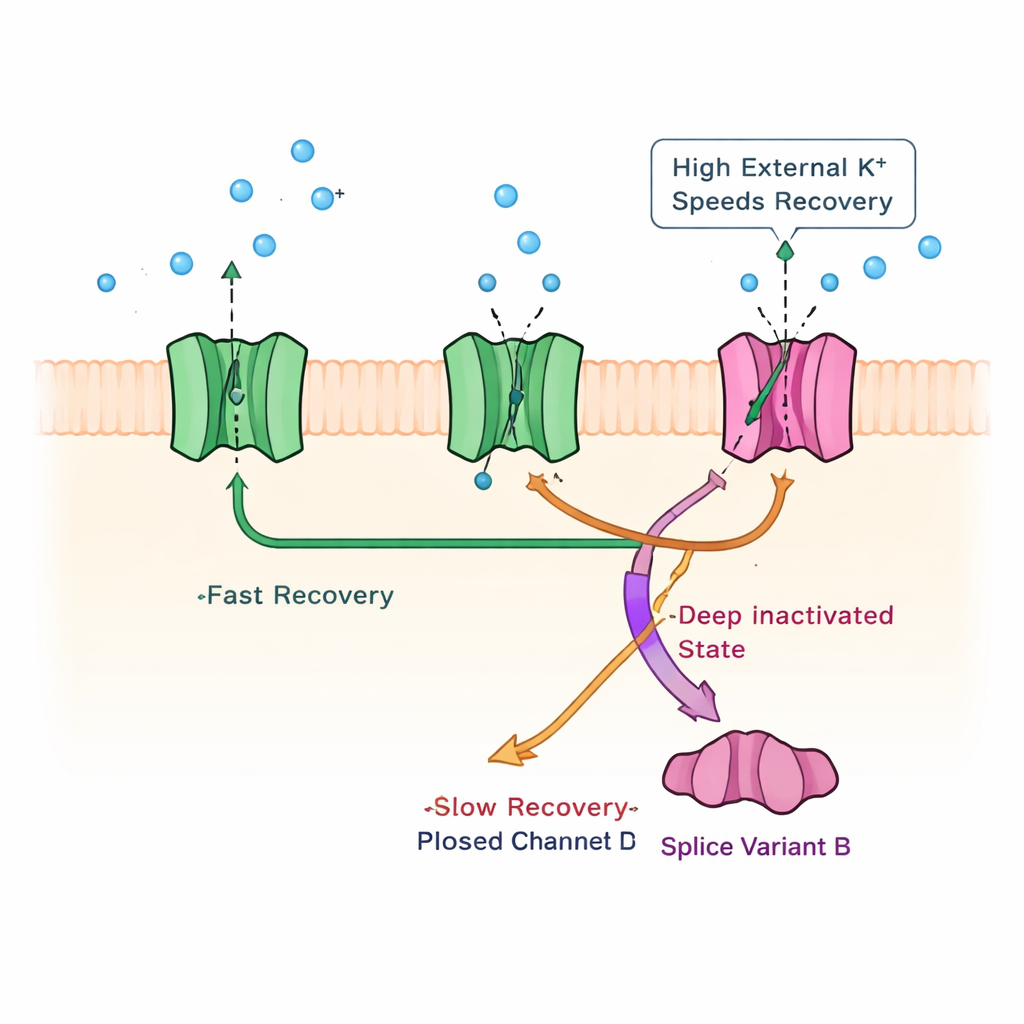
发现一种沉睡的失活机制
为了解导致这种慢恢复的通道内部物理改变,研究团队考察了其它钾通道中已知的失活机制。他们通过截去通道内尾的一部分来排除了经典的“球棒链”阻断机制;慢相仍然存在。随后他们使用高外钾浓度,这一技巧已知可改变其它通道中的孔基失活过程。在这些条件下,电流关闭变得更快,但关键是,慢恢复相本身也专门加速了,仿佛高钾将通道从一种深度、持续时间很长的阻断状态中释放出来。对通道门控片段的策略性突变进一步支持了这样一种观点:KChIP1b 促进了一条以孔为中心的失活路径——在 Kv4 通道中通常较弱——它与通道通常的更快的闭态失活并存。
这对大脑活动有何意义
这些发现表明,通过选择表达 KChIP1a、KChIP1b 或两者的混合物,神经元可以精细调节 A 型电流在脉冲之间恢复的速度。在富含 KChIP1b 的细胞中,相当大一部分 Kv4 通道被“停放”在一种深度且恢复缓慢的失活状态中,限制了它们在快速发放期间的可用性。这可能使某些抑制性中间神经元——在脑回路中协调和抑制活动的细胞——能够以更高的频率或不同的时序模式发放。本质上,辅助蛋白的一个微小剪接差异解锁了钾通道的一个隐性制动模式,为大脑控制自身电节律增加了一层新的灵活性。
引用: Cao, W., Tachtsidis, G. & Bähring, R. KChIP1 splice variants modulate Kv4 channels by promoting P/C-type inactivation features. Sci Rep 16, 2632 (2026). https://doi.org/10.1038/s41598-026-35770-5
关键词: Kv4 钾通道, KChIP1 剪接变体, A 型电流, 神经元兴奋性, 通道失活