Clear Sky Science · zh
具有生理相关性的钝化钼-和铼‑焦磷酸放射性示踪剂形式及其对甲状腺素转运蛋白淀粉样变性敏感性的基础
为什么这则心脏影像报道重要
随着年龄增长,许多人心脏中会出现无声的错误折叠蛋白沉积,称为淀粉样物。部分沉积物,尤其是由一种名为甲状腺素转运蛋白(transthyretin)产生的沉积,会使心脏僵硬并导致严重疾病。临床上,医生越来越依赖一种称为99mTc‑PYP(锝‑99m 焦磷酸盐)的放射性示踪剂在扫描中可见这些沉积。然而令人意外的是,这种示踪剂在体内的确切形态以及它为何似乎“偏好”某些淀粉样类型一直不清楚。本文将理论与实验相结合,揭示了该示踪剂在类血液条件下的真实结构,以及这种构型如何可能使其定位于有害的甲状腺素转运蛋白纤维。
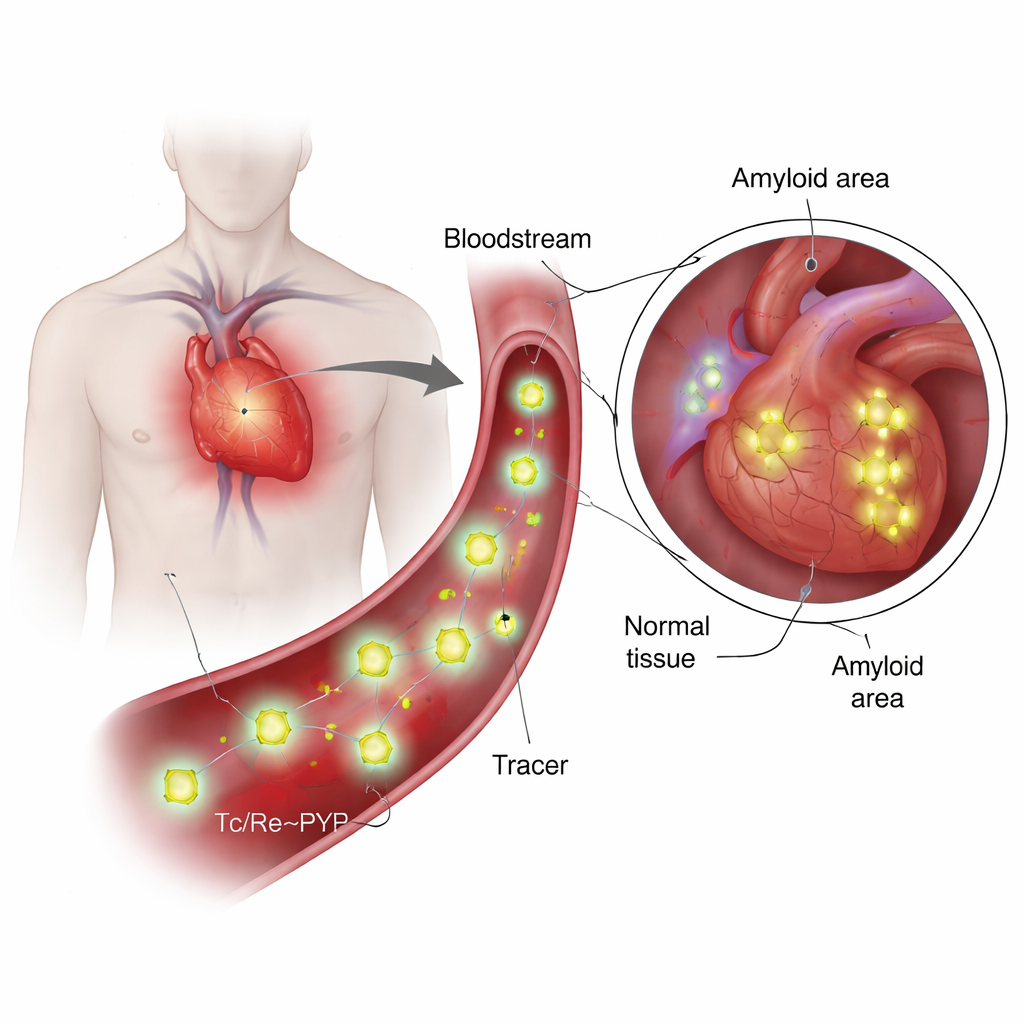
这些示踪剂是什么,何以与众不同?
99mTc‑PYP 已用于影像骨骼数十年,因为它倾向于在钙和矿物代谢活跃的区域聚集。近来临床发现它还能区分两种主要的心脏淀粉样变性:一种由免疫球蛋白轻链(AL)构成,另一种由甲状腺素转运蛋白(ATTR)构成。在 ATTR 中,心脏在 PYP 扫描上常常显著显影,而 AL 病例即便钙沉积相似也往往暗淡。这一不一致提出了关键问题:示踪剂是仅仅粘附在钙上,还是直接与淀粉样蛋白相互作用?回答这个问题需要知道示踪剂在类血液条件下的真实化学结构,而早期工作对此只有大致的描绘。
用更安全的替代物观察不可见之物
由于锝具有放射性且在医疗制剂中含量极微,许多实验室技术难以直接研究它。作者因此使用与锝密切相关的元素铼(rhenium)作为替代,铼在尺寸和配位偏好上几乎相同但化学处理更方便。他们在模拟临床 PYP 试剂盒的条件下制备了铼‑焦磷酸混合物,并用一系列工具进行了检测:高水平量子化学计算、紫外-可见吸收、各种振动光谱(红外和拉曼)、核磁共振、质谱以及锡穆斯堡尔谱学。结合这些方法,他们检验了多种候选结构,并缩小了在中性pH(类似血液)下可能存在的物种范围。
一种灵活但可识别的分子形状
综合证据指向一个共同的“核心”结构:一个八面体配位的配合物,其中处于+4 氧化态的锝或铼原子与两个焦磷酸根和两个水分子配位。简言之,金属位于由氧原子构成的近乎八面体的笼子中心,焦磷酸根充当多齿的锚点,水分子占据剩余位点。该二水合二焦磷酸单元并非刚性结构。由于焦磷酸臂可以扭动并与配位水形成分子内氢键,分子在溶液中会采样多种略有不同的构象。计算和光谱表明这些变化会移动其光吸收和振动指纹,解释了实验谱带为何较宽以及早期研究为何难以确定单一明确的结构。
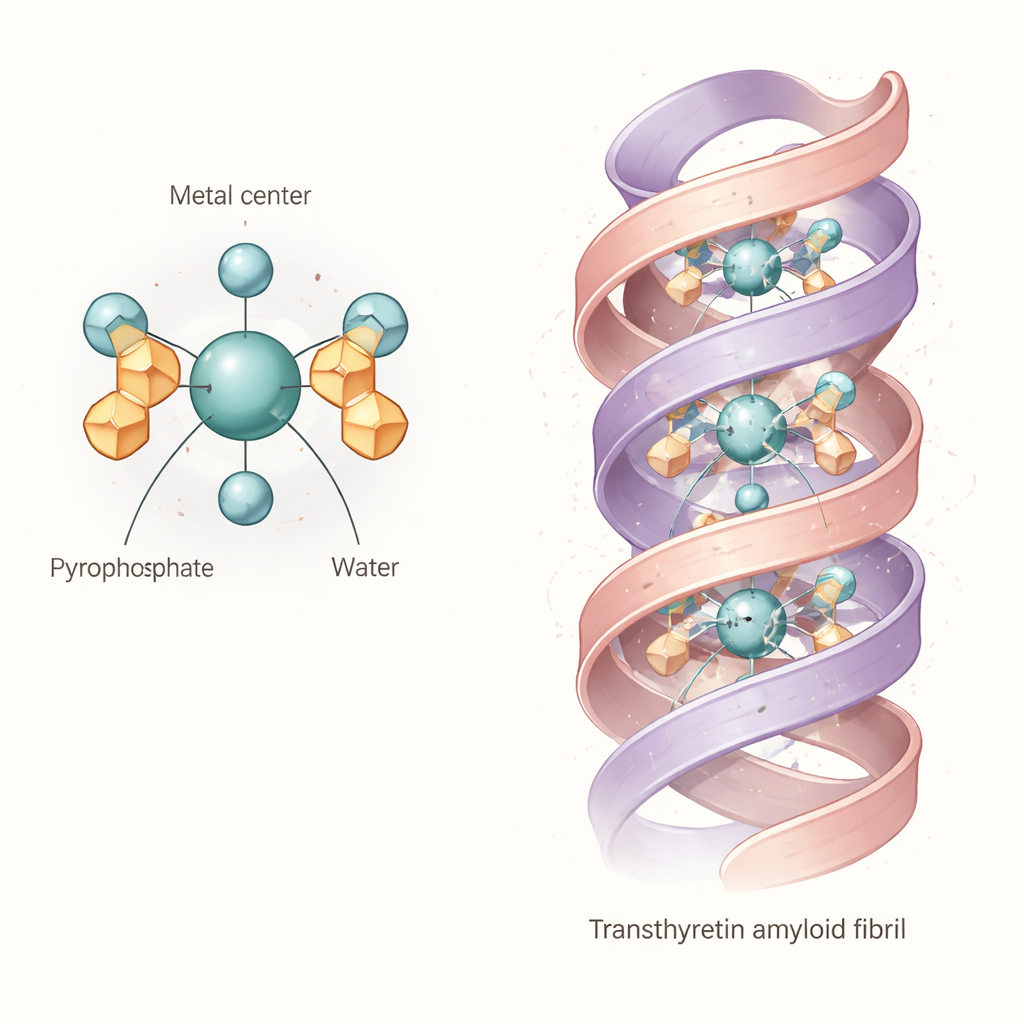
这对结合心脏淀粉样有什么意义
作者随后探讨这种灵活的配合物是否有可能直接嵌入甲状腺素转运蛋白淀粉样纤维。他们基于一处详尽的人源甲状腺素转运蛋白纤维的冷冻电镜结构,用建模的锝‑焦磷酸配合物进行了计算对接搜索。结果显示,二水合二焦磷酸单元可以嵌入沿纤维延伸的中心通道,与衬里腔体的带电侧链形成多处氢键和盐桥。这表明,至少对于某些甲状腺素转运蛋白纤维构型,示踪剂并非仅标记附近的矿物沉积;它可能被蛋白质骨架直接抓住。示踪剂自身的结构可塑性很可能帮助它适应真实患者纤维中稍有差异的口袋和电荷分布。
对诊断和未来示踪剂的启示
对非专业读者而言,关键信息是:广泛使用的 PYP 心脏扫描所依赖的示踪剂,比先前认识到的更为微妙且具有对蛋白的识别性。在生理条件下,它更适合作为一个小型、含水的金属‑焦磷酸笼,能灵活变形并与甲状腺素转运蛋白淀粉样通道形成多点接触。这一认识有助于解释为何该示踪剂在某些淀粉样疾病中信号强烈而在另一些则不明显,以及为何蛋白或其环境的微小变化会导致灵敏度的意外丧失。通过阐明示踪剂的工作形态和电荷分布,这项研究为设计更具选择性的下一代影像或治疗剂奠定了基础,旨在更精确识别心脏及其他部位的致病纤维。
引用: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
关键词: 心脏淀粉样变性, 甲状腺素转运蛋白, 锝焦磷酸盐, 分子影像, 放射性示踪剂化学