Clear Sky Science · zh
使用松弛试验和数值模拟对绵羊与人类主动脉瓣组织进行比较分析,以开发生物假体瓣膜
为何心脏瓣膜材料至关重要
每一次心跳,主动脉瓣都会开合以确保血液朝正确方向流动。在人的一生中,该瓣膜会运动数十亿次,一旦失效,通常需要置换为人工瓣膜。机械瓣耐久但需要终生服用抗凝药;更柔软的生物瓣感觉更自然但可能会磨损失效。本研究提出一个务实的问题:经过精细处理的绵羊(羊羔)主动脉瓣组织能否在性能上足够接近人类瓣膜——甚至优于当前常用材料——从而用于制造更耐久、更安全的生物假体心脏瓣膜?
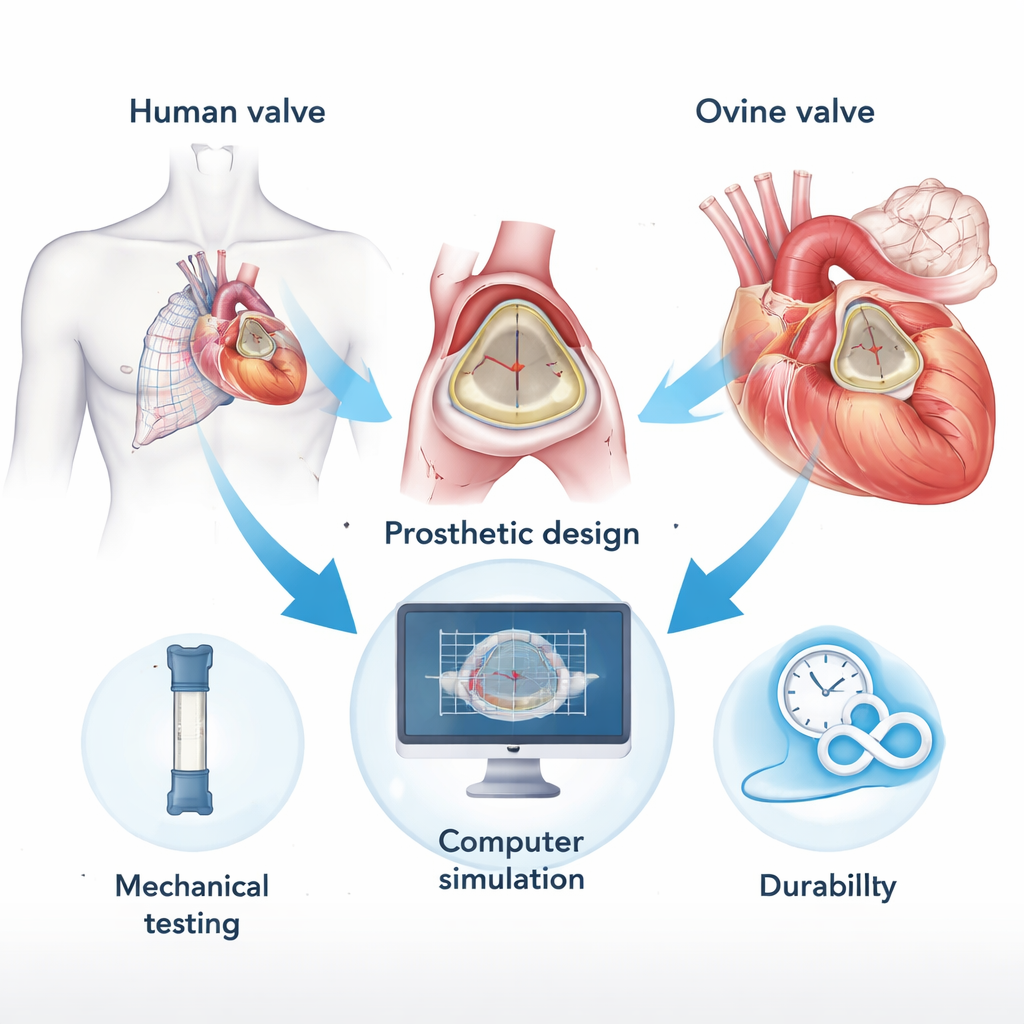
寻找更好的替代材料
目前的生物(生物假体)瓣膜通常采用牛心包组织制成,这类组织随着时间会变硬并发生降解。作者们探索了一种替代方案:使用绵羊的真实主动脉瓣组织,经过化学处理以保存组织并减少免疫反应与钙化。他们将这些经处理的绵羊组织与天然人类主动脉瓣薄片进行比较,重点考察组织的拉伸、松弛及承受体内负荷的能力。由于瓣膜性能在很大程度上取决于胶原纤维的结构和行为——这些细小纤维赋予瓣膜强度与柔韧性——找到一种其纤维行为类似或优于人组织的材料至关重要。
将瓣膜组织置于试验
研究团队从绵羊瓣膜叶的最强且最均匀的区域切取了小而精确成形的样本,然后对其进行化学固定,模拟商业瓣膜的处理工艺。他们将这些小条样本单向拉伸至断裂,记录其所能承受的力和刚度。经处理的绵羊组织的弹性模量约为20兆帕,而文献中人类瓣膜样本的范围大约为6到28兆帕。绵羊组织表现出略低的刚度但在断裂时更大伸长,这对现代经导管微创瓣膜尤其有利:这类瓣膜需要紧密压缩装入导管,并在心内展开而不发生撕裂。
在恒定载荷下瓣膜如何软化
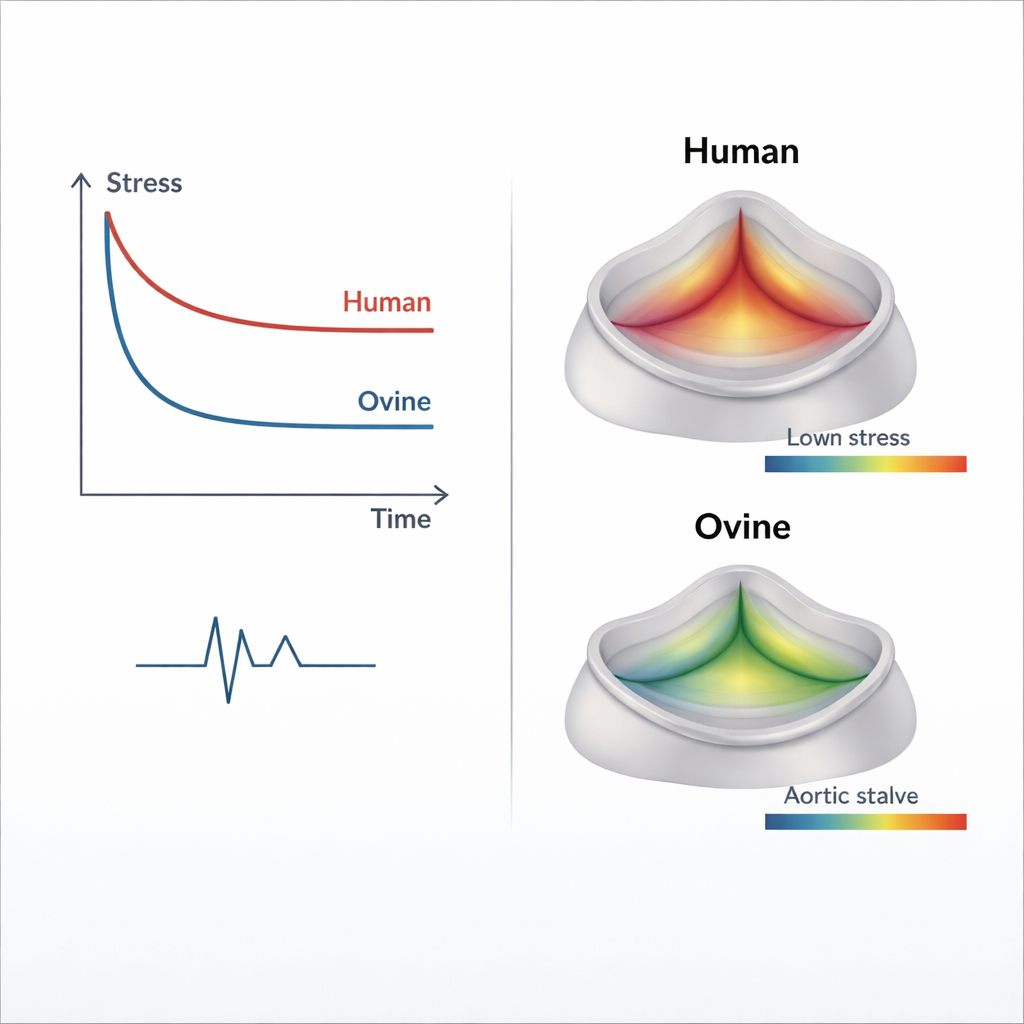
瓣膜并非刚性弹簧;它们具有粘弹性,意味着在被拉伸时会缓慢松弛并重新分配应力。为捕捉这种随时间变化的行为,研究者进行了应力松弛试验:他们将每个样本迅速拉伸到其断裂应变的固定分数并保持五分钟,观察内部应力如何衰减。人类瓣膜薄片在300秒内约损失21%的初始应力,而经处理的绵羊组织损失约41%,这表明绵羊瓣膜更具粘弹性,能更好地吸收冲击并随时间分散载荷。研究者使用一种称为准线性粘弹性(quasi-linear viscoelasticity)的标准数学框架,对这些数据拟合了详细模型,提取出描述瞬时弹性响应与较慢松弛阶段的参数。
模拟跳动的心脏
为了了解这些差异在工作心脏内的含义,团队在常用工程软件中建立了一个三维主动脉瓣计算模型,并赋予其人类或经处理绵羊组织的材料属性。随后他们施加来自左心室与主动脉的真实压力波,追踪虚拟瓣膜随心跳的开合。在峰值开启期(收缩期),经处理绵羊瓣膜叶的最大应力约为0.36兆帕,约为人类组织模型中0.72兆帕的一半。在闭合期(舒张期),应力与应变模式从附着缘向叶片中央“腹部”迁移,这与临床上观察到的瓣膜退变位置一致。总体而言,绵羊模型显示出比人类组织更低或分布更有利的应力,并且低于早期研究中报道的牛心包应力水平。
这对未来心脏瓣膜意味着什么
简而言之,研究表明经过精心处理的绵羊主动脉瓣在弯曲和松弛特性上接近人类瓣膜,但可能具有更低的峰值应力和更高的柔韧性。这些特性对于制造能够更好地承受心脏内反复开合、尤其适用于经导管植入并经历剧烈压缩与扩展的生物假体瓣膜,具有良好前景。尽管仍需更复杂的测试——包括多方向拉伸、更长时间的疲劳研究以及完整的流固耦合模拟——但这项工作将绵羊主动脉瓣组织指向了下一代更柔软、更耐用心脏瓣膜替代材料的有力候选者。
引用: Masoumi, S.F., Rassoli, A., Changizi, S. et al. Comparative analysis of ovine and human aortic valve tissue for bioprosthetic valve development using relaxation tests and numerical simulation. Sci Rep 16, 7315 (2026). https://doi.org/10.1038/s41598-026-35729-6
关键词: 主动脉瓣, 生物假体瓣膜, 绵羊心脏组织, 粘弹性, 有限元模拟