Clear Sky Science · zh
m6A 甲基化相关 mRNA 与甲状腺癌的相关性
为何 RNA 的细微变化对甲状腺癌重要
甲状腺癌通常可以治愈,但仍有部分患者面临疾病复发或转移。该研究聚焦于一种新兴的生物学层面,称为 RNA “标记”,即在细胞内的 RNA 分子上添加小的化学标签。研究者提出了一个具体问题:在没有自身免疫性甲状腺疾病的乳头状甲状腺癌患者中,这些 RNA 标签是否发生了可能推动癌症发展的变化,且这些变化是否能指示新的诊断或治疗途径?
聚焦无免疫疾病的甲状腺肿瘤
许多甲状腺癌患者同时伴有自身免疫性甲状腺疾病,这种对甲状腺的免疫攻击会使生物学图景变得复杂。为避免这种混杂,研究团队选择了 26 名其乳头状甲状腺癌发生时无自身免疫迹象的患者。从每位患者处收集了一块肿瘤组织和一块邻近的非癌变甲状腺组织。在其中 3 名患者的样本中,研究人员进行了广泛的基因启动/沉默状况调查以及对一种称为 m6A 的特定化学标签在 RNA 上的负载情况的测量,m6A 是人类细胞中最常见的内部 RNA 修饰。
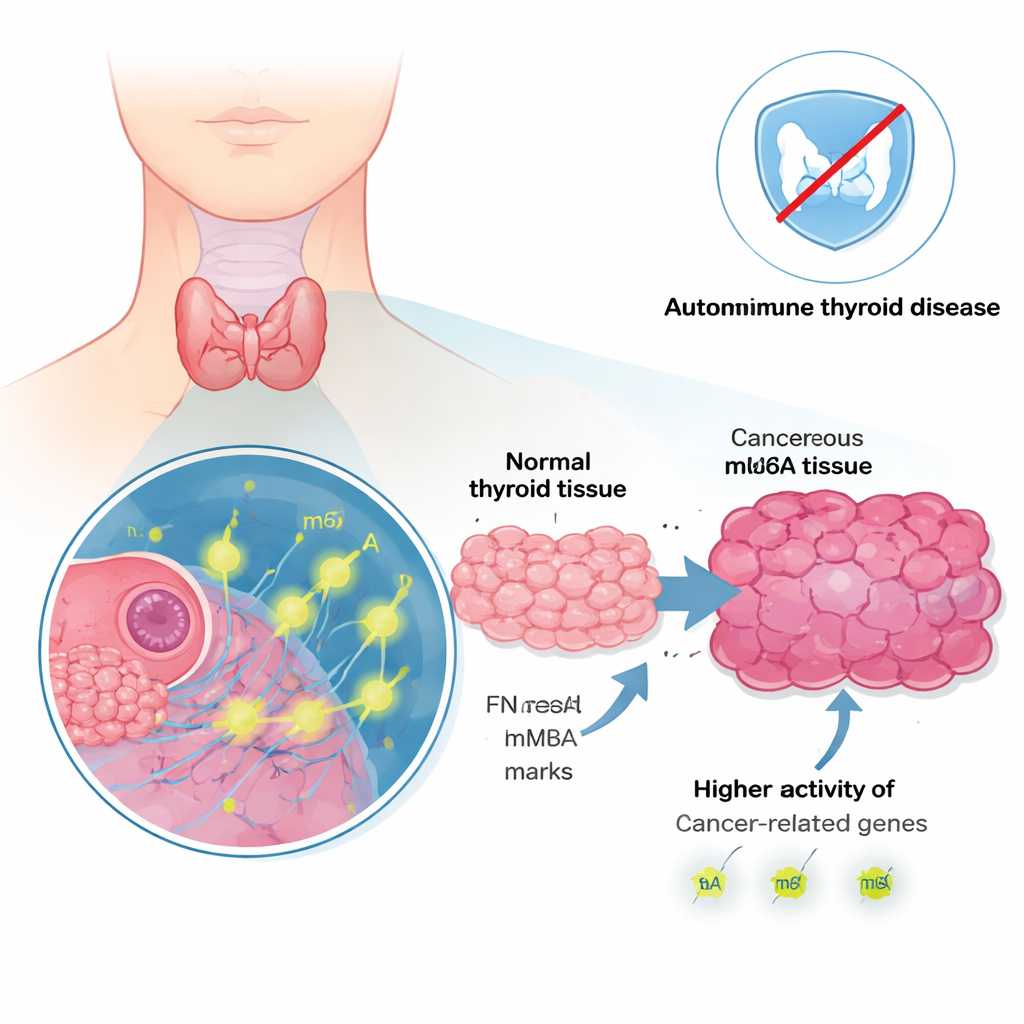
与癌症相关基因和通路的激增
当研究者将肿瘤组织与邻近的健康组织比较时,发现有 486 个基因在癌组织中表达上调,39 个基因表达下调。许多显著上调的基因已被证明与癌症生长、转移或治疗耐受有关。其中包括 LAMB3、FN1 和 NMU 等基因,它们有助于细胞与周围基质及邻近细胞的相互作用。计算分析显示,上调基因聚集在已知促进癌症的通路中,包括与细胞分裂、应激反应以及细胞与免疫系统之间通讯相关的信号网络。换言之,肿瘤已明显将基因活动重新编程为有利于生长和侵袭的方向。
RNA 标记与一个关键“阅读器”被激活
接下来的问题是这些癌症中 RNA 上的 m6A 标签是否发生了变化。通过生化检测,团队发现肿瘤组织总体 m6A 水平高于配对的正常组织。随后他们检查了控制这一标记系统的基因:“写入者”负责添加 m6A、“擦除者”负责去除 m6A,以及“阅读者”结合被标记的 RNA 并影响其后续命运。在肿瘤中,只有一种阅读者脱颖而出:称为 IGF2BP2 的阅读蛋白显著高表达。早期研究表明,IGF2BP2 能结合 m6A 标记的 RNA,使其更稳定并更易被翻译成蛋白。在乳头状甲状腺癌中,IGF2BP2 已被关联到更具侵袭性的行为、更差的预后以及更强的淋巴结转移能力。
哪些 RNA 带有额外的标记——以及为何重要
通过将 m6A 映射与相同样本中的基因表达测量相结合,研究者鉴定出在肿瘤中更强烈被标记的 367 条 RNA,以及标记减少的 12 条 RNA。引人注意的是,大多数被高度标记的 RNA 属于同一批整体表达上调的促癌基因列表。对于 147 个基因,肿瘤同时显示出更高的 m6A 水平和更高的表达,包括 FN1、LAMB3、NMU 和 CDKN2B。网络分析表明,这些基因处在控制肿瘤细胞如何附着环境、如何响应炎症信号以及如何重塑周围组织的系统核心位置——这些是侵袭和转移的关键步骤。团队还发现数十个被标记的长链非编码 RNA,其中包括与已知癌症通路相关的那些,暗示 RNA 标记可能不仅影响编码蛋白的信使 RNA,也作用于微调基因行为的调控性 RNA。
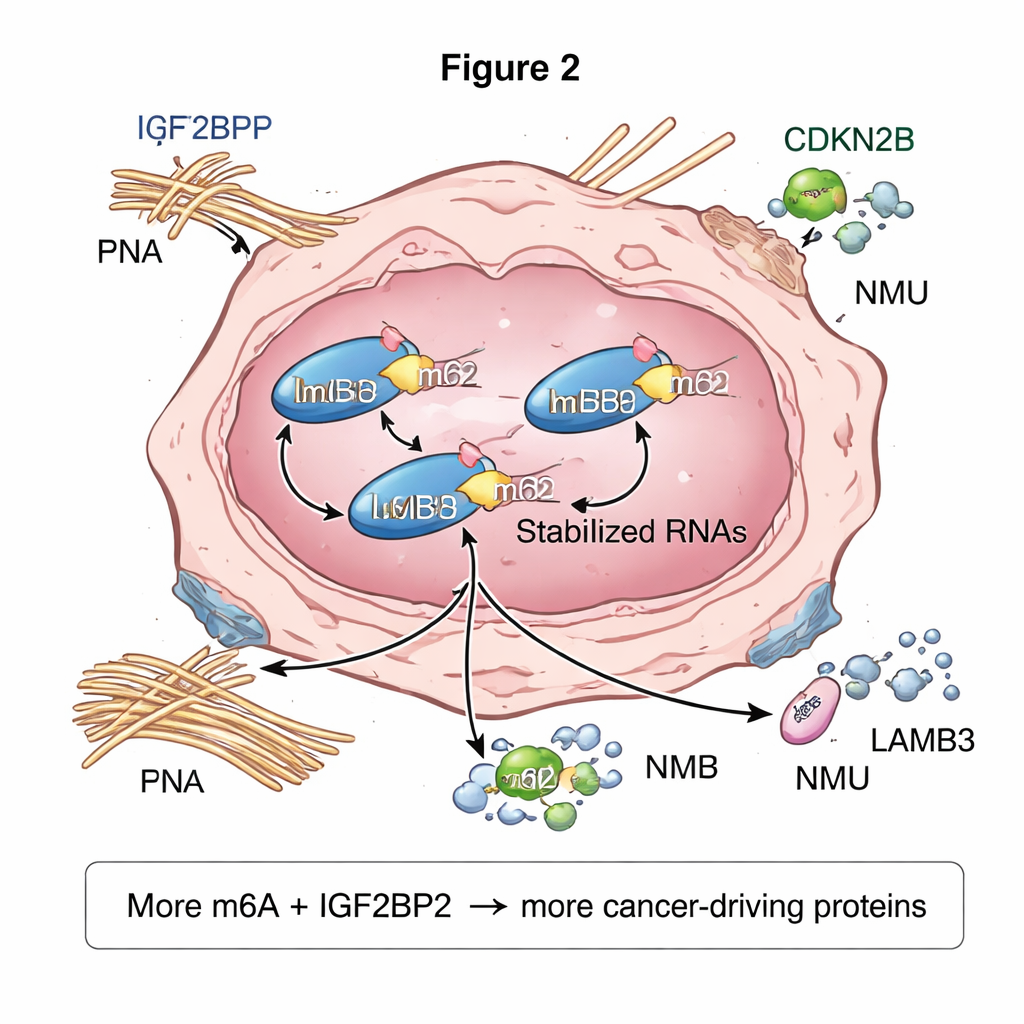
这对患者可能意味着什么
对非专业读者来说,核心信息是:乳头状甲状腺癌——即便发生在没有自身免疫性甲状腺疾病的患者中——似乎利用一种 RNA 上的化学标记系统来放大促癌网络。肿瘤细胞表现出更高的整体 m6A 水平和更大量的阅读蛋白 IGF2BP2,这两者共同稳定并增强了关键促癌基因的产物。尽管这项工作主要基于对一小群患者的高级计算与实验室分析,但它突出了若干具体参与者——例如 IGF2BP2 以及被 m6A 标记的基因 FN1、LAMB3 和 NMU——作为值得进一步探索的潜在诊断标志或靶向治疗对象。未来研究需在更大样本量和实验模型中验证这些发现,但结果表明 RNA 上的“表观遗传”标记是甲状腺癌生物学中一个重要且可能可被药物干预的层面。
引用: Jiang, Z., Luo, S., Lin, Y. et al. Correlations of m6A methylation-related mRNAs with thyroid cancer. Sci Rep 16, 5688 (2026). https://doi.org/10.1038/s41598-026-35712-1
关键词: 乳头状甲状腺癌, RNA 甲基化, m6A 修饰, IGF2BP2, 癌症生物标志物