Clear Sky Science · zh
HIV Vpr 诱导 SNCA 反义启动子去甲基化,导致神经认知功能受损
为什么 HIV 仍会影响大脑
得益于现代抗逆转录病毒药物,感染 HIV 的人群寿命更长、健康状况更好。然而,即便血液中的病毒得到良好控制,许多人仍会出现记忆、注意力和运动方面的问题。本研究通过聚焦一种小型病毒蛋白 Vpr 以及一种在帕金森病中也起关键作用的脑蛋白——α‑突触核蛋白,来探究这些症状的成因。理解这两种分子如何相互作用,或可解释 HIV 如何加速大脑衰老,并为保护大脑提供新的思路。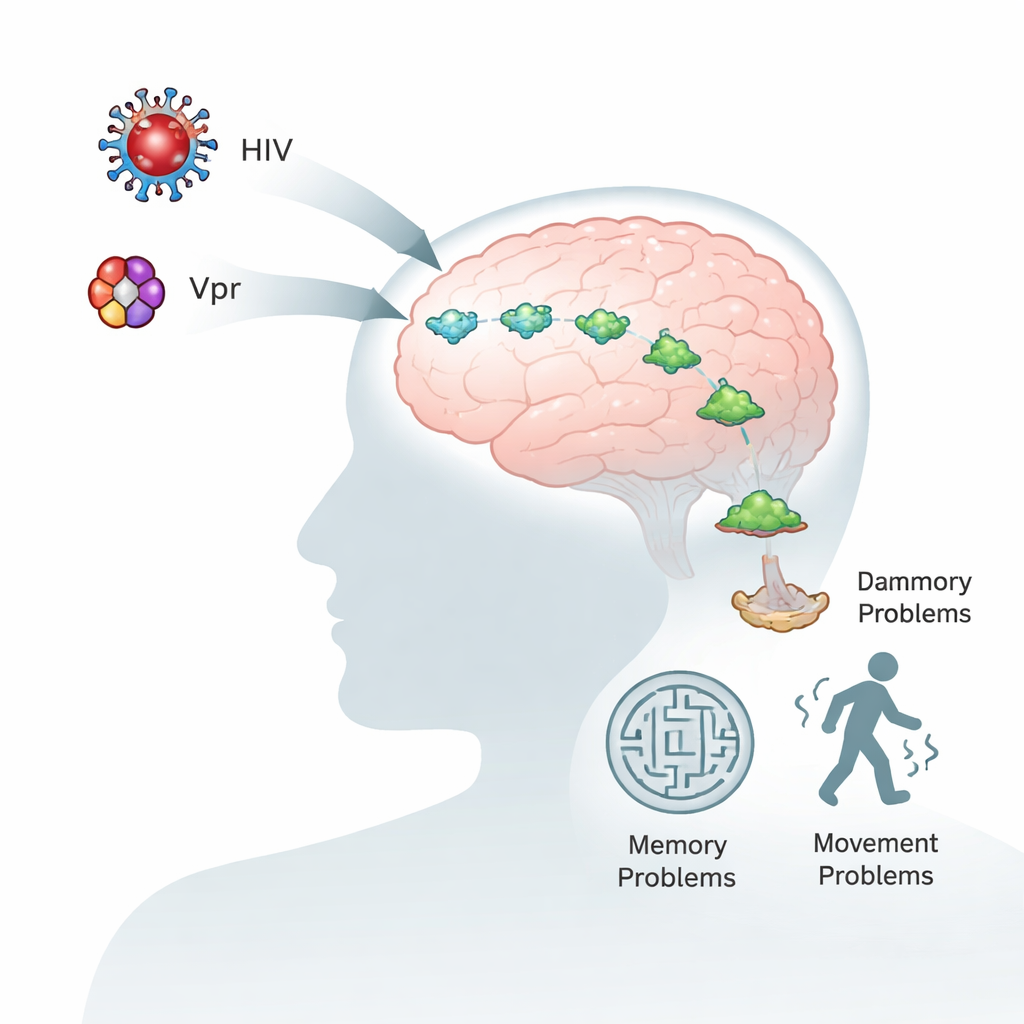
处于 HIV 与帕金森交汇处的脑蛋白
α‑突触核蛋白是一种帮助神经细胞通讯的蛋白,尤其在控制运动与记忆的脑区中重要。当 α‑突触核蛋白过量积累时,会形成团聚体,损害突触、加重能量产生的线粒体负担,并促发炎症。这类团聚体是帕金森病的标志之一。作者显示在小鼠正常老化过程中,α‑突触核蛋白也会积累,并且 HIV 的 Vpr 蛋白会在类神经细胞中进一步提升其水平。这使 α‑突触核蛋白成为 HIV 相关认知问题与经典运动障碍之间的关键枢纽。
病毒蛋白如何改写细胞的“标点符号”
每个细胞都在 DNA 上使用化学标签——常被比作分子的标点符号——来开关基因表达。该研究聚焦于 α‑突触核蛋白基因内一处鲜为人知的调控开关,称为反义启动子。在健康细胞中,这一开关在很大程度上被甲基基团标记,从而保持相对抑制。研究者发现 Vpr 在该区域的特定位点去除这些甲基标记,这一过程称为去甲基化。标记一旦被移除,反义启动子变得更为活跃,推动更多 α‑突触核蛋白的产生,为有害团聚的形成创造条件。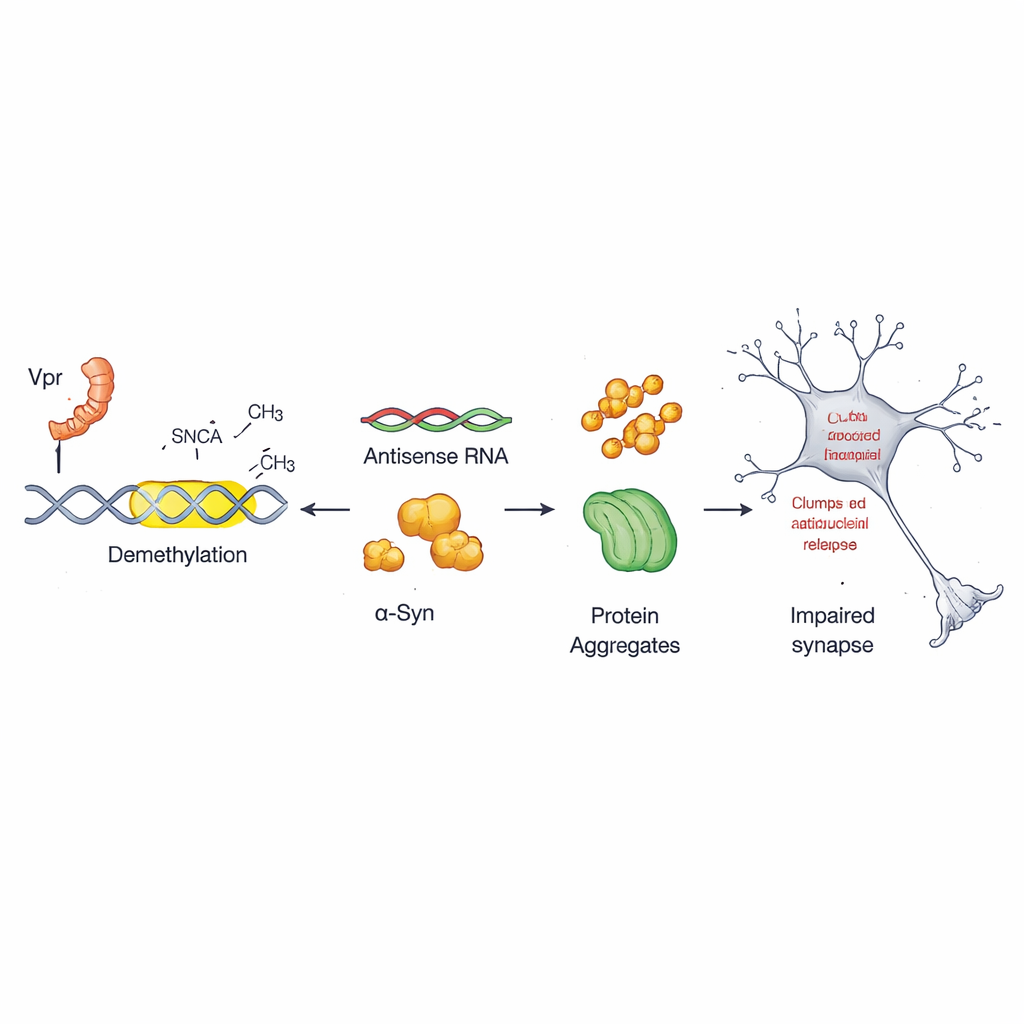
来自细胞、小鼠与人脑的证据
在培养的人类类神经细胞和原代小鼠神经元中,研究者表明添加 Vpr 会随时间增加 α‑突触核蛋白的转录本和蛋白水平。一种广泛促使 DNA 去甲基化的药物在一定程度上复制了这些效应,强调了表观遗传控制的作用。相比之下,一种名为 DMOG 的化合物可阻断去甲基化酶,阻止 Vpr 完全激活反义启动子。团队随后分析了来自有无 HIV 的人类脑样本。HIV 阳性供体的大脑——无论在抗逆转录病毒治疗前后——在相同 DNA 区域的甲基标记更少,且 α‑突触核蛋白及其反义转录本水平更高,特别是在有 HIV 相关痴呆的供体中更为明显。这表明病毒在大脑中留下了持久的表观遗传“伤痕”。
从分子变化到记忆问题
为将这些分子层面的变化与行为联系起来,研究者考察了 Vpr 对小鼠脑回路的影响。当他们将 Vpr 应用于小鼠海马切片——海马是记忆形成的重要区域——发现神经元之间的基本信号强度未改变,但强化连接的能力(即长时程增强,LTP)下降。在活体小鼠中,将 Vpr 靶向注入海马会导致动物在一项要求记住物体位置的空间记忆任务中表现较差。综合这些实验,表明 Vpr 诱导的 α‑突触核蛋白变化不仅是生化层面的异常,而是转化为突触功能减弱和可测量的记忆缺陷。
这对感染 HIV 的人意味着什么
该研究提出了一条清晰的事件链:HIV 释放 Vpr,Vpr 重编程控制 α‑突触核蛋白的关键 DNA 开关,蛋白质积累并形成团聚,神经元逐渐丧失通讯与支持记忆的能力。由于类似的 α‑突触核蛋白问题是帕金森病的病理基础,这项工作暗示 HIV 与经典神经退行性疾病可能共享重叠机制。重要的是,这些发现指出了潜在的新策略——例如稳定反义启动子处 DNA 甲基化的药物或限制 α‑突触核蛋白积累的干预——以减缓或预防 HIV 相关的认知衰退与运动问题。
引用: Santerre, M., Wang, Y., Kalamarides, D. et al. HIV Vpr induces demethylation of the SNCA antisense promoter, leading to neurocognitive impairment. Sci Rep 16, 6078 (2026). https://doi.org/10.1038/s41598-026-35691-3
关键词: HIV 相关神经认知障碍, α-突触核蛋白, 表观遗传学, DNA 甲基化, 帕金森样症状