Clear Sky Science · zh
基于Acoramidis的离子液体作为稳定甲状腺转运蛋白的潜在剂:DFT计算、分子对接与ADMET研究
为什么为一种罕见心脏病开发口服药如此困难
甲状腺转运蛋白淀粉样变性(ATTR)是一种严重疾病,血液中的一种蛋白在心脏和神经中堆积,逐步造成损伤。一种新药Acoramidis可以帮助阻止这种堆积,但存在一个实际问题:该药在水中溶解性差,这使得作为口服药时难以被身体吸收。本研究探索了一种巧妙策略,将Acoramidis重新设计为类似盐的形式,称为离子液体,可能使药物更易于吞服并提高疗效。
把有前景的药物变成可服用的形式
要使一片药丸起效,必须先在胃肠道的水性液体中溶解,然后穿过肠壁进入血液。Acoramidis在稳定甲状腺转运蛋白(TTR)方面非常有效,有助于阻止与ATTR相关的有害蛋白聚集,但它溶解性差且口服生物利用度低。研究人员通过将Acoramidis与不同带电配对分子化学结合,设计出三种新的离子液体版本(IL1、IL2 和 IL3)。这些版本更像流动的盐而非刚性晶体,可能提高药物的溶解性和体内分布。 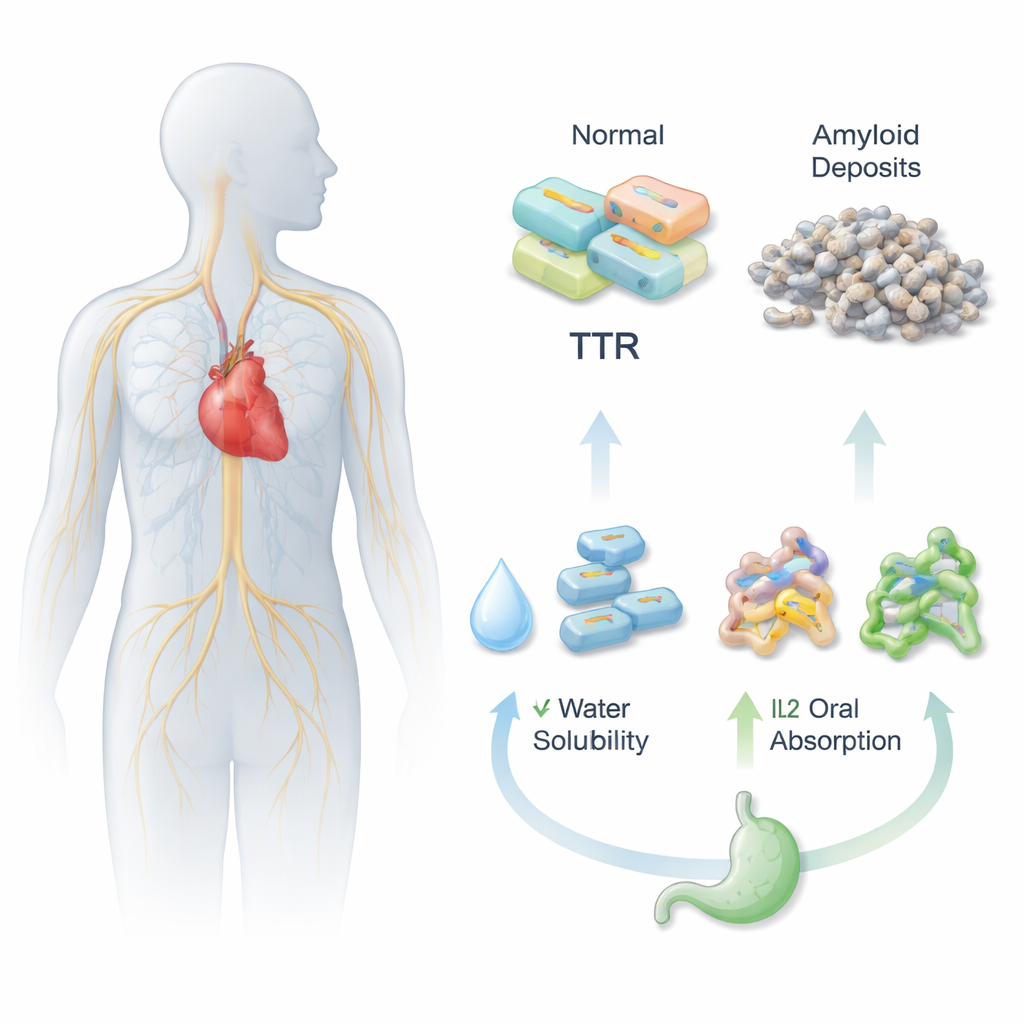
在计算机上探测新分子
研究团队没有直接进入动物或人体试验,而是使用先进的计算方法预测这些新形式的表现。量子化学计算估算了每种分子的极性——这是预测水溶性的关键指标——以及电子响应性,这与它们如何与蛋白相互作用相关。IL1表现突出,具有最高的偶极矩和最强的电子响应性,表明其在水中应具有更好的溶解性,并能与靶点形成更强、更灵活的相互作用。能量计算还表明,IL1比原始药物和另外两种离子液体具有更高的热稳定性,这意味着它在到达靶点之前更不容易分解。
药物与靶点的结合有多紧密
接着,研究人员使用分子对接这一虚拟“锁与钥匙”测试,查看Acoramidis及其三种离子形式如何契合TTR蛋白的结合通道。所有四种化合物都能对接到TTR的正确区域,但IL1形成了最紧密的结合,具有最有利的结合能以及多个稳定相互作用——尤其是与蛋白关键氨基酸之间的氢键。这种更强的结合表明IL1可能比母体药物更能维持TTR的安全四聚体结构,从而帮助预防导致淀粉样沉积的有害解体和错误折叠。
这些新形式会被身体吸收并清除吗?
最后,团队使用在线药理学工具评估身体可能如何处理这些化合物——它们的溶解性、穿过肠壁的能力、在血液中的循环以及最终清除情况。预测结果显示,三种离子液体的水溶性均优于Acoramidis,其中IL3显示出最高的原始溶解度。肠道渗透性和总体口服吸收率在三种离子液体中都有所改善,IL1和IL2在肠道穿透与预测生物利用度之间表现出最佳平衡。血浆蛋白结合、清除率和半衰期等指标也发生了变化,表明离子液体形式在口服给药后可能提供更可靠的体内暴露,IL1再次展现出特别有利的特征。 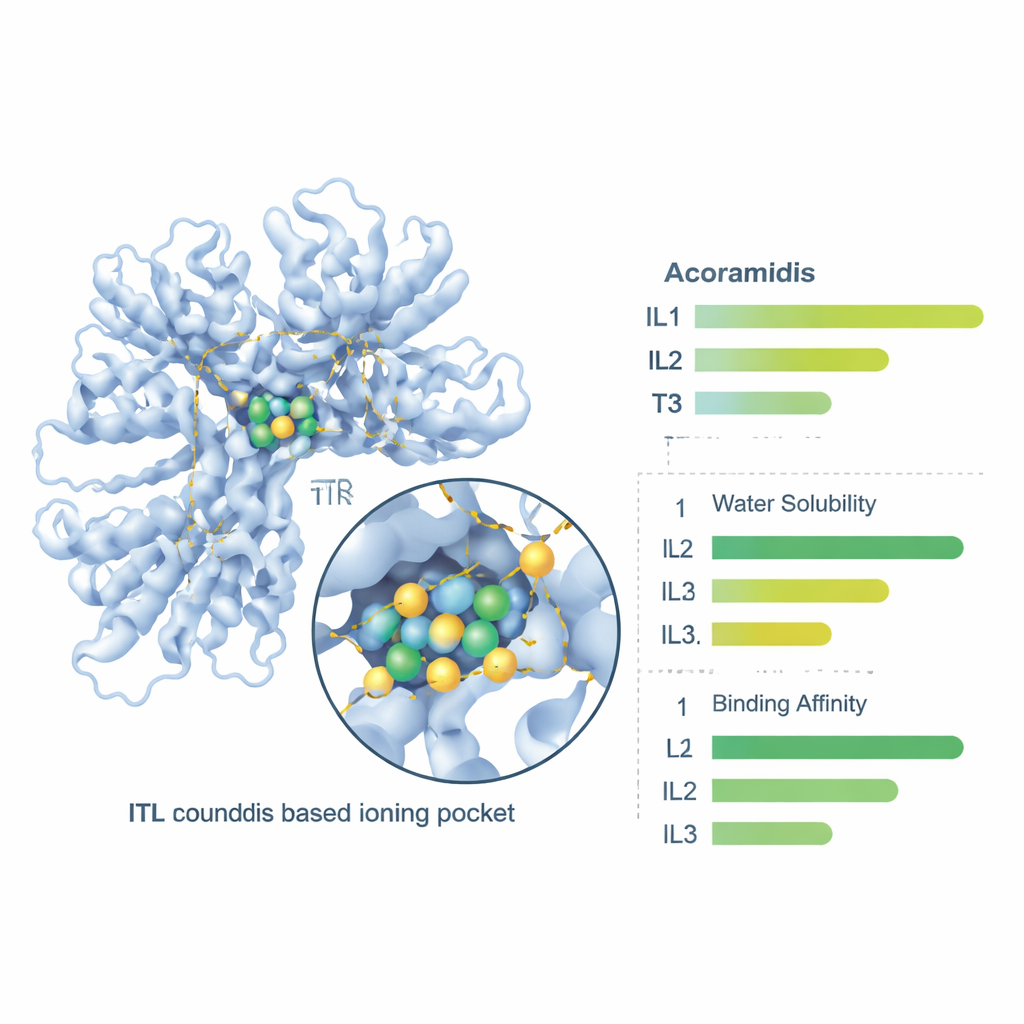
这对未来ATTR治疗意味着什么
对于非专业读者来说,主要信息是:Acoramidis在治疗这种罕见但严重的心脏和神经疾病方面已显示出希望,但其差的溶解性限制了口服给药的效果。通过将Acoramidis设计成特定的离子液体,本研究通过完全基于计算的测试表明,有可能开发出溶解性更好、与蛋白靶点结合更强且吸收更高效的版本。在三位候选者中,IL1在稳定性、结合能力、溶解性和预测口服吸收之间似乎达到了最佳平衡,使其成为未来实验室和临床开发的有力先导,目标是提供更有效、易于服用的ATTR治疗方案。
引用: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
关键词: 甲状腺转运蛋白淀粉样变性, Acoramidis, 离子液体, 蛋白质错误折叠, 口服给药