Clear Sky Science · zh
针对DENV-1和DENV-3的多表位疫苗的计算机设计
为什么登革热疫苗仍然重要
登革热不再是罕见的热带疾病;它现在威胁着逾100个国家的数十亿人,并在亚洲、拉丁美洲及其他地区经常压垮医院。尽管已有两种获批疫苗上市,但防护效果并不均衡,尤其对从未感染过登革热的人以及多个血清型同时流行的地区效果有限。本研究提出了一个及时的问题:计算机引导的设计能否帮助我们构建更安全、更精确的疫苗,专门针对经常同时发生的两种登革病毒共感染?
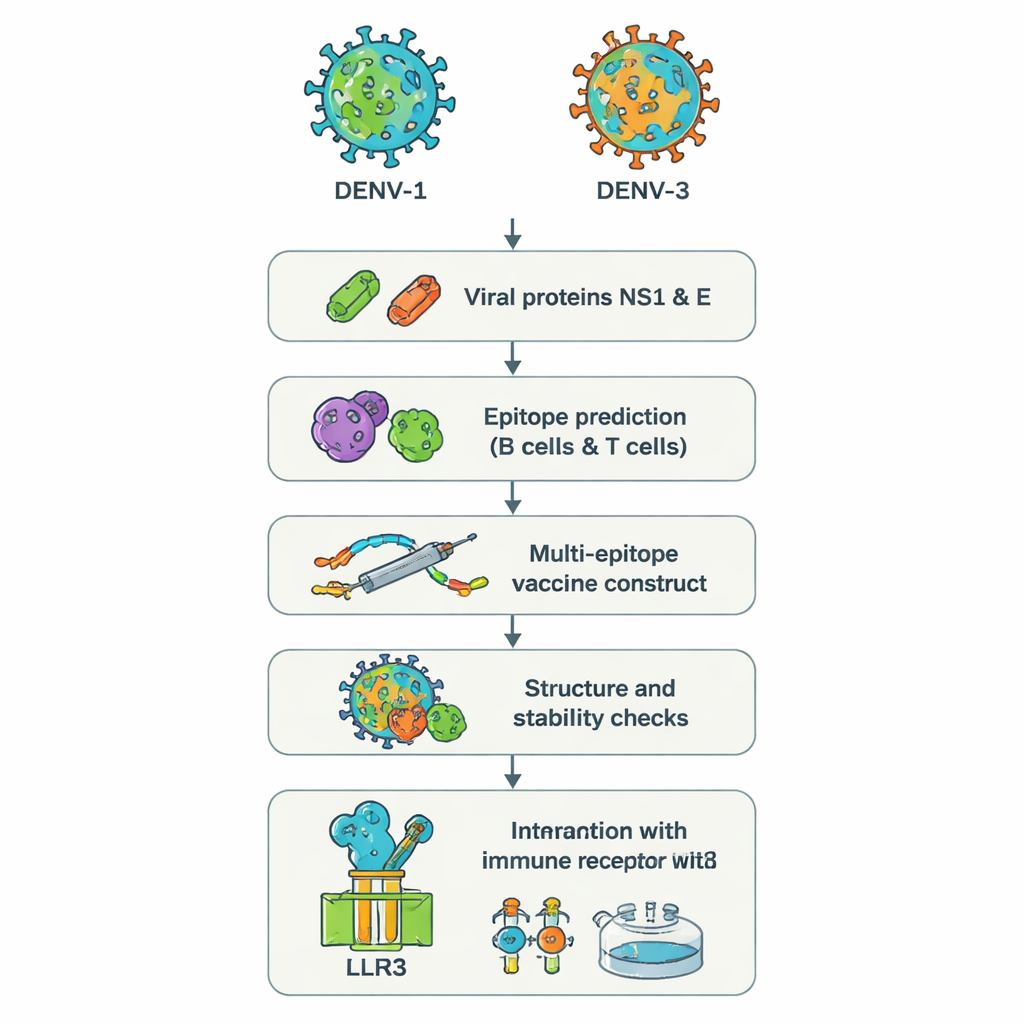
两种狡猾的病毒血清型及其问题所在
登革病毒有四个版本,称为血清型DENV‑1到DENV‑4。任何一种感染都可能引起高热、剧烈疼痛,某些情况下可导致危及生命的出血或休克。令人担忧的是,再次感染不同血清型有时会使病情加重而不是改善,因为已有抗体可能帮助新病毒更容易进入细胞,这一过程称为抗体依赖性增强。在最近的爆发中,临床报道出现同时感染DENV‑1和DENV‑3的患者,这种组合与更严重的病情和混淆性的检测结果相关。现有疫苗不能可靠地保护所有年龄组和所有血清型,尤其是对既往未暴露人群,因此在防御上留下了危险的空白。
从分子层面设计疫苗
研究人员没有在实验室培养完整病毒,而是使用了一种有时称为“逆向疫苗学”的方法。他们从DENV‑1和DENV‑3中两种病毒蛋白NS1和E的基因序列出发。这些蛋白在病毒入侵细胞和免疫系统识别中起关键作用。强大的在线工具扫描蛋白序列,定位出最可能被人体B细胞(产生抗体)和T细胞(杀死被感染细胞并协调免疫反应)识别的短片段——表位。从数百个候选中,团队选择了一小组被预测对免疫系统高度可见、在两种血清型之间共享且能够触发有益抗病毒信号(如干扰素‑γ)的表位。
构建单一的多功能疫苗分子
所选表位随后在数字上拼接成一个长的人工蛋白,即“多表位”疫苗。短的氨基酸连接子作为柔性间隔,使每个表位保持构象并对免疫细胞可及。额外加入了一段基于天然人源抗菌肽β‑防御素的片段,作为佐剂以增强整体反应。计算分析预测最终构建体含有575个氨基酸,具有稳定性、亲水性(因此更易溶解),并不太可能成为过敏原。进一步的结构预测工具生成了三维模型,并检查大多数构件是否处于现实的空间位置,类似于已知蛋白结构中的情况。
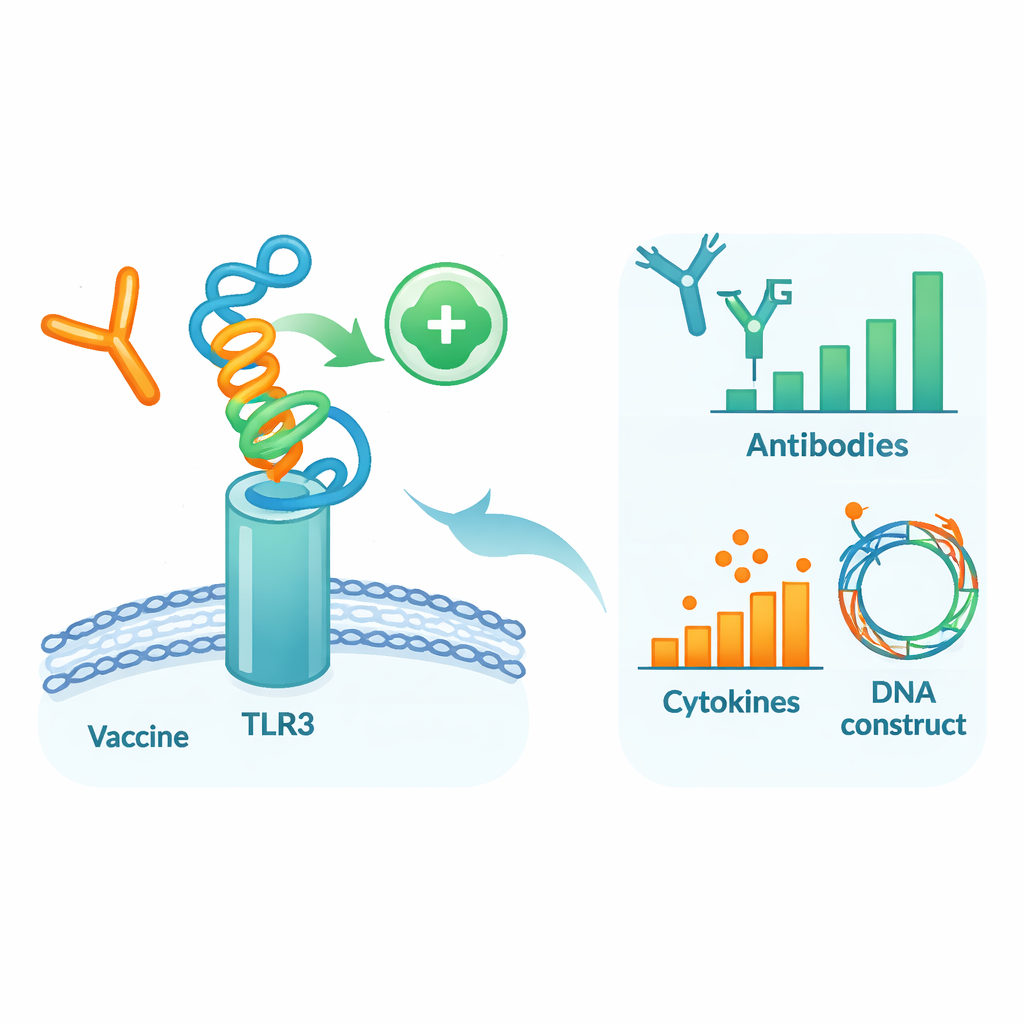
在虚拟人体中测试候选疫苗
为了观察该设计蛋白在类似人体环境中的表现,作者运行了一系列详细的计算机模拟。首先,他们将疫苗模型与免疫细胞表面的感受器蛋白TLR3对接,TLR3可检测病毒物质并帮助启动早期防御。分子动力学模拟——原子运动的虚拟“电影”——表明疫苗与TLR3形成了稳定的复合体,具有有利的结合能和大量氢键。对运动和能量的额外分析指出了两分子中作为接触“热点”的特定区域。随后,使用免疫系统模拟器模拟了数月内三剂疫苗接种。虚拟免疫系统产生了强烈的保护性IgG抗体波、持久的B细胞和T细胞记忆,以及与强烈抗病毒反应一致的信号分子。
从计算模型到可供实验的蓝图
最后,研究人员将疫苗的遗传密码优化以便在常用实验微生物中高效表达,并成功将该优化的DNA序列插入标准表达质粒,为未来的实验检测做准备。简言之,他们的工作提供了一个针对精心挑选的DENV‑1和DENV‑3片段的新型登革热疫苗的详尽蓝图,该疫苗被预测为稳定且安全,并应能强烈激活免疫系统的两条防线。尽管这些结果纯属计算预测,必须在细胞、动物乃至最终的人体实验中得到验证,但它们展示了现代生物信息学如何迅速为像登革热共感染这样复杂问题生成定制的疫苗候选者。
引用: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
关键词: 登革热疫苗, 多表位, DENV-1, DENV-3, 免疫信息学