Clear Sky Science · zh
整合蛋白质组学与代谢组学分析揭示阿霉素耐药急性髓系白血病细胞的氨基酸代谢紊乱
为何部分白血病药物失效
化疗已显著改变急性髓系白血病(AML)这一快速发展的血液癌症的治疗前景。然而,许多患者出现疾病复发,原因在于癌细胞学会了在原本可杀死它们的药物面前存活。本研究提出了一个简单但关键的问题:当白血病细胞对阿霉素(一种常用的化疗药)产生耐药性时,细胞内部发生了哪些变化?这些变化是否能指引出恢复药物效力的新策略?
窥探白血病细胞内部
为探明这一点,研究者比较了常用的人类AML细胞系HL60与其被诱导产生阿霉素耐药性的姊妹系HL60/R。研究并非只关注单个基因或蛋白,而是采用两种广泛且互补的方法。蛋白质组学测量了数千种蛋白——这些蛋白是细胞执行各类功能的主力分子;代谢组学检测了数百种小分子代谢物,包括脂类、糖类和氨基酸。通过整合这些“组学”层次,研究团队构建了耐药细胞与仍然敏感细胞之间差异的细致图景。
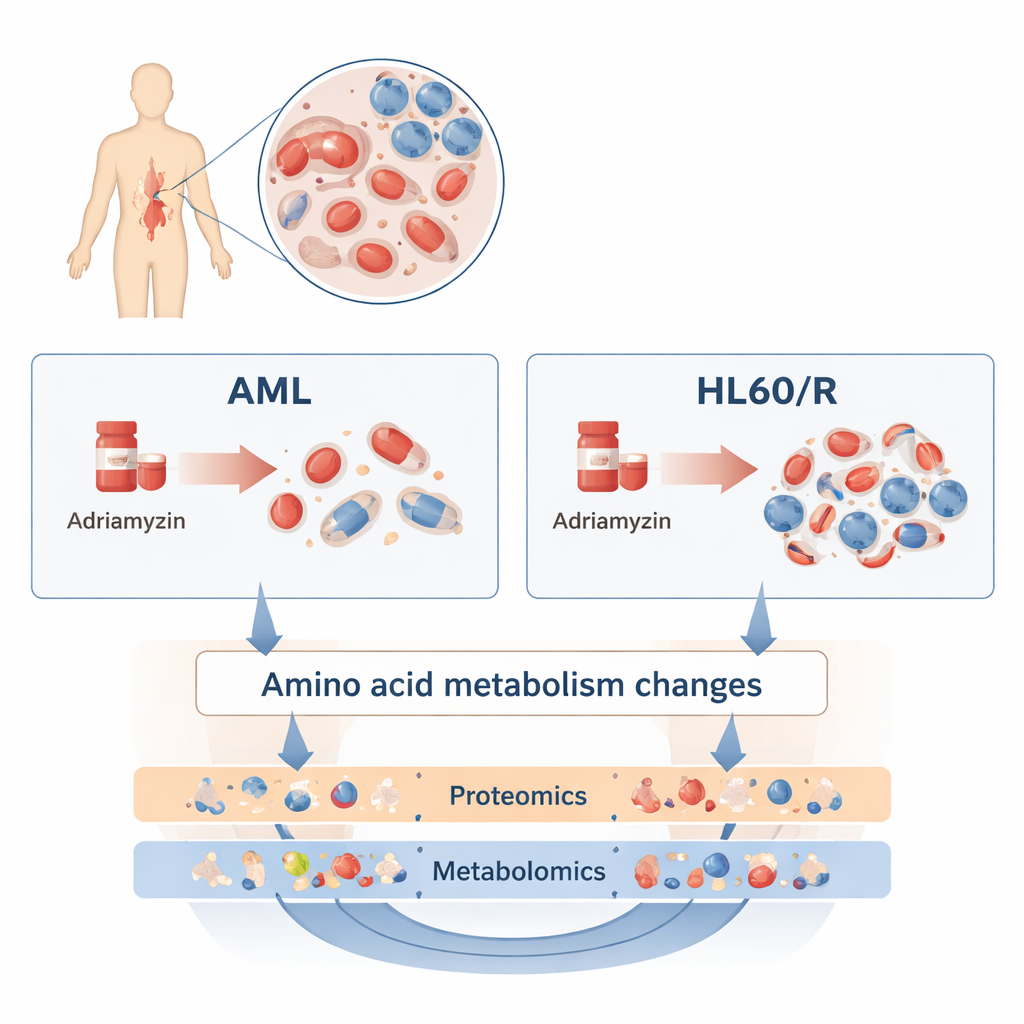
细胞机制的大规模重编程
蛋白质组学调查揭示了广泛的改变:在阿霉素耐药细胞中有逾3,200种蛋白的丰度较正常HL60细胞显著升高或降低。许多这些蛋白聚集在调控能量利用和应激反应的通路中。特别是cAMP信号通路、HIF‑1通路(帮助细胞应对低氧)以及氧化磷酸化(线粒体中主要的能量生成过程)相关蛋白发生了改变。这些变化表明,耐药的白血病细胞通过重新编程其呼吸、增殖和信号传导方式来抵御化疗。
代谢转向氨基酸途径
代谢组学分析呈现了互补的观点。在约1,400种检测到的代谢物中,有260种在耐药细胞中显著改变。统计模型明确区分了耐药与非耐药细胞,表明耐药具有一致的代谢特征。当将这些改变的代谢物映射到已知生化通路时,若干途径尤为突出。许多受影响最显著的通路与氨基酸相关——蛋白质的构件,尤其包括丙氨酸、天冬氨酸、谷氨酸、半胱氨酸、甲硫氨酸和谷胱甘肽相关途径。其它网络如嘌呤和嘧啶代谢(对DNA和RNA至关重要)以及某些脂质代谢也受到了干扰,强调耐药伴随广泛的代谢重塑。
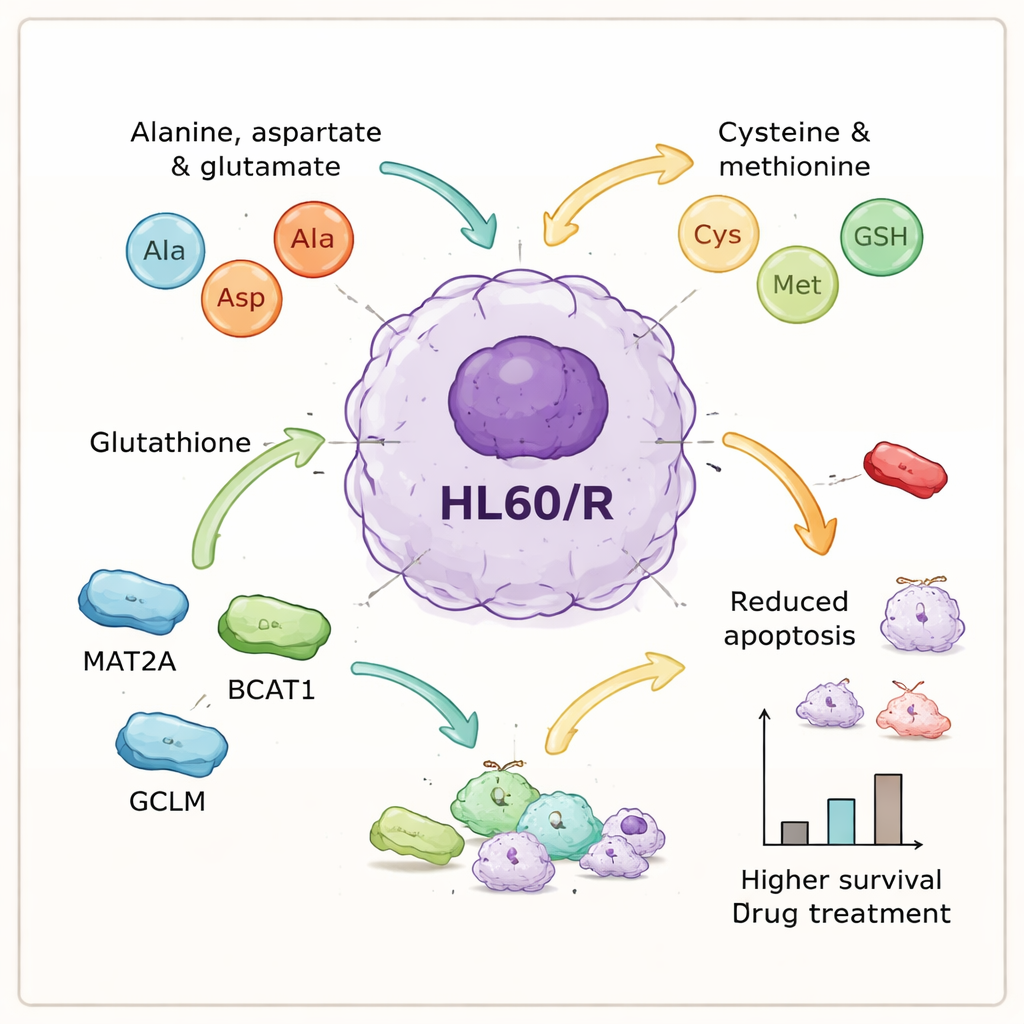
帮助癌细胞存活的关键分子
通过整合蛋白与代谢物数据,作者锁定了一组与氨基酸相关、似乎对耐药至关重要的过程。他们选定了与这些通路相关的六种蛋白——GOT1、GPX1、AHCY、MAT2A、BCAT1和GCLM——做进一步检测。实验室验证显示,其中五种在耐药细胞中含量增加,支持氨基酸代谢被上调的观点,而一种抗氧化酶GPX1则减少。为探讨因果关系,团队用小干扰RNA下调了耐药细胞中三种上调的蛋白——MAT2A、BCAT1和GCLM。敲低这些蛋白后,细胞在药物处理后出现显著更多的程序性细胞死亡,这意味着它们失去了大部分对阿霉素获得的保护能力。
对未来治疗的意义
综上所述,这些发现表明阿霉素耐药的AML细胞存活并非仅由于单一突变,而是因为它们重塑了内部化学状态,其中氨基酸代谢是一个核心枢纽。通过将更多资源分配到特定的氨基酸与谷胱甘肽通路,细胞似乎更能应对应激、修复损伤并在化疗暴露下避免死亡。对非专业读者而言,关键的信息是:耐药并非随机发生,而是遵循可识别的模式,这些模式可以被测量并有望成为干预靶点。长期来看,针对像MAT2A、BCAT1或GCLM等特定氨基酸代谢蛋白的药物,若与阿霉素或类似药物联合使用,可能为临床提供新工具,以预防或克服急性髓系白血病患者的耐药问题。
引用: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
关键词: 急性髓系白血病, 药物耐药, 阿霉素, 氨基酸代谢, 多组学