Clear Sky Science · zh
用于高通量筛选 Piezo1 调节剂的功能性且稳健的细胞模型
为什么细胞里的微小压力传感器很重要
每当血液在血管中流动,或我们仅仅在房间内行走时,细胞都会感受到微小的机械力。一个称为 Piezo1 的关键“压力传感器”蛋白帮助细胞将这些力转化为电信号和化学信号,从而维持组织的健康。由于 Piezo1 参与血管生长、骨骼强度、免疫功能以及某些罕见遗传疾病,药物开发者渴望找到能够调节其活性的分子。本文介绍了一种新的、更快速的筛选方法,使用工程化细胞和基于光的读出,取代传统那些缓慢且劳动强度大的技术。
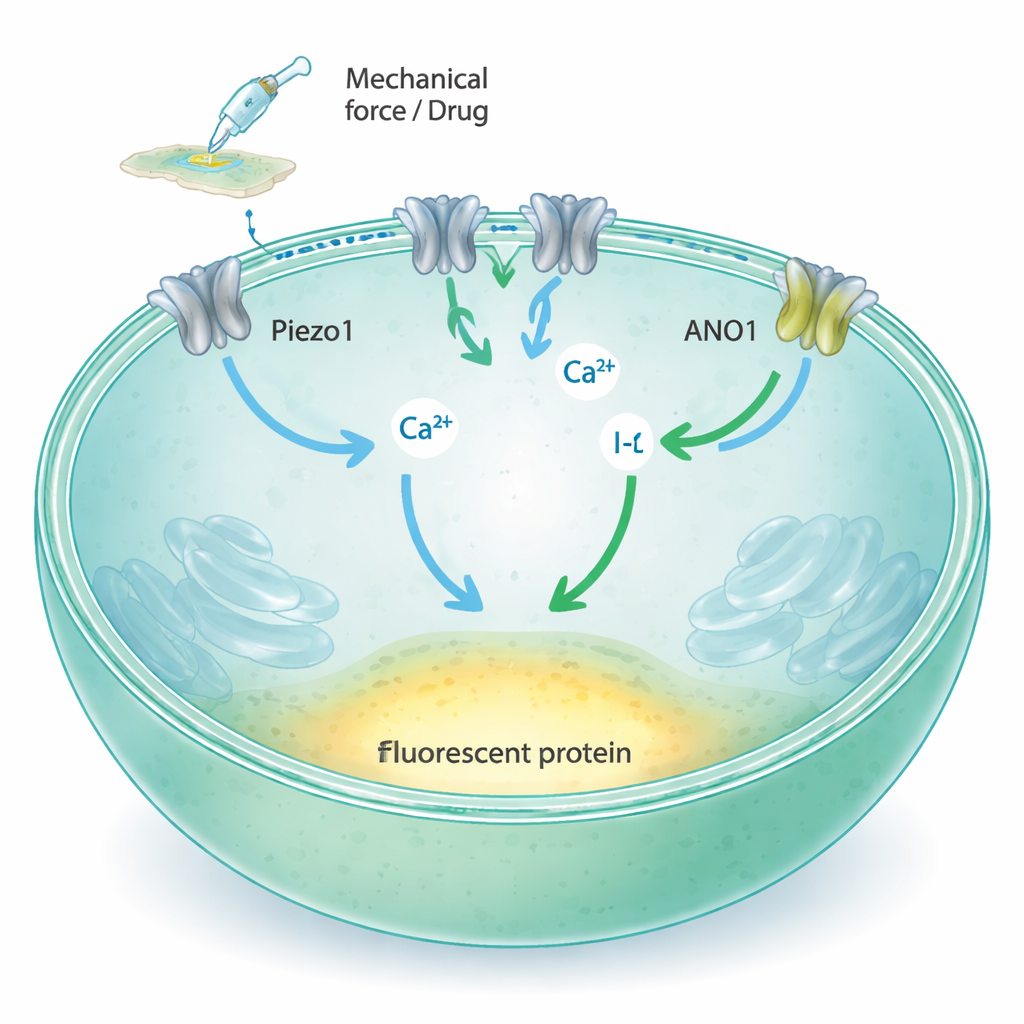
把触觉转换为光信号
Piezo1 是位于细胞膜上的通道,当膜被拉伸或受压时会打开,允许钙离子和其他带电离子流入细胞。研究此类通道的传统方法依赖精细的玻璃电极或特定的荧光报告分子,这些方法虽然强大,但难以扩展到现代药物发现所需的数万次试验。作者的目标是将 Piezo1 活性转换为一种简单的光学变化,使微孔板读板机能够快速在大量样本中同时测量。他们的想法是将 Piezo1 与另外两个组分连接:对钙反应的另一个离子通道 ANO1,以及一种在碘离子暴露时会变暗的改造型黄色荧光蛋白。
构建响应性的检测细胞
研究人员以 Fischer 大鼠甲状腺(FRT)细胞为起点,这类细胞天然产生 Piezo1 且能很好地贴附在标准塑料板上。他们确认这些细胞表达 Piezo1 而不表达其近缘蛋白 Piezo2,并证明这些细胞中的 Piezo1 对流体流动和机械探针刺激会产生钙内流。接着,他们将 ANO1 通道和对碘敏感的荧光蛋白(YFP‑H148Q/I152L)导入细胞。当细胞内钙升高时,ANO1 打开允许碘离子进入;随着碘在荧光蛋白周围累积,荧光强度随之下降。显微镜、流式细胞术和电生理记录显示,ANO1 和荧光传感器在细胞中高表达且按预期工作。
从药物作用到可测量的荧光变化
在这一由三部分组成的系统中,研究团队建立了一个简单的因果链:如果某个测试分子激活 Piezo1,钙进入细胞,ANO1 打开,碘涌入,荧光信号下降;如果某个分子阻断 Piezo1,信号则保持明亮。他们使用已知的 Piezo1 激活剂(Yoda1、Jedi1、Jedi2)和阻断剂(Ruthenium Red、GsMTx4)验证了这一逻辑。激活剂引起剂量依赖性的荧光下降,其灵敏度值与先前报道的数据相符;阻断剂则呈相反模式,随浓度增加使响应减弱。只有在钙和碘同时存在时该检测才有效,这强调了信号确实依赖于由 Piezo1 介导的钙内流及随后 ANO1 介导的碘流入。统计学指标如 Z 因子和信噪比表明,该方法在工业规模筛选中足够稳定和可靠。
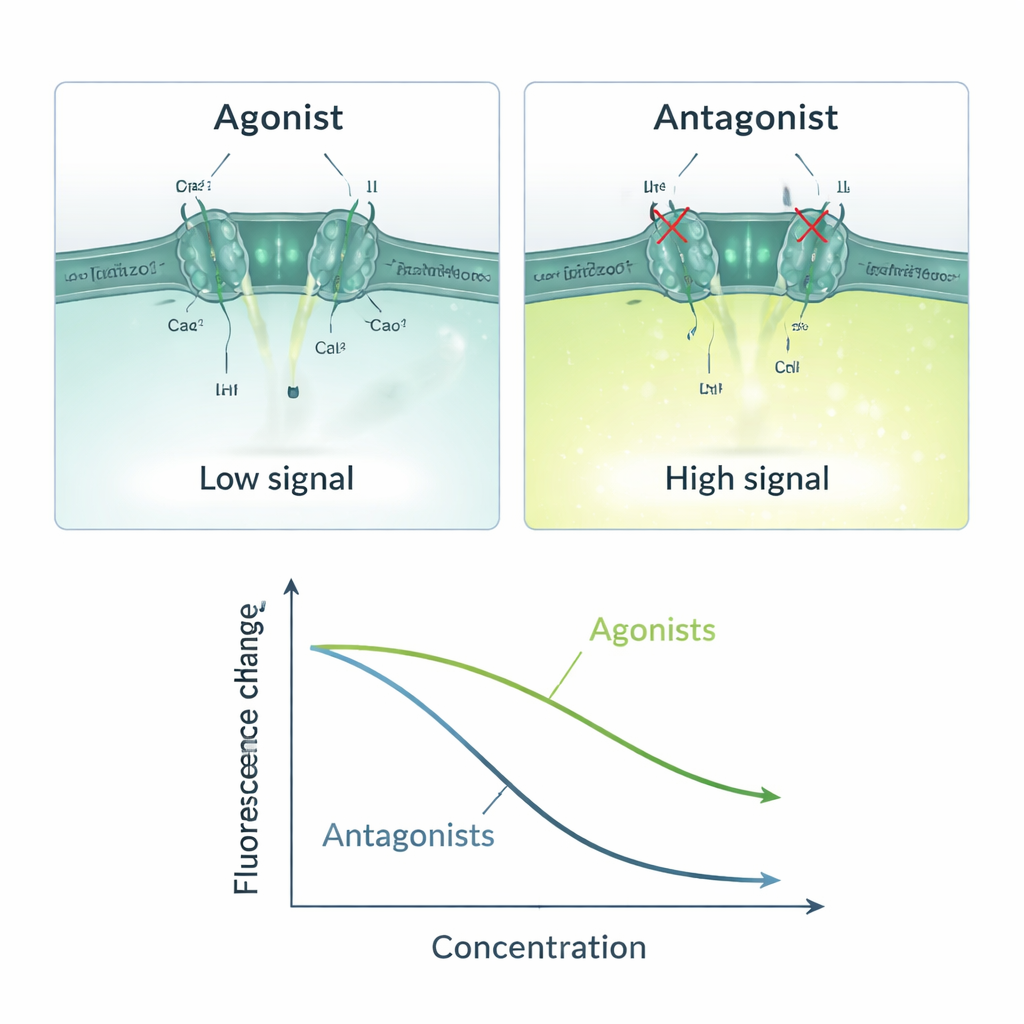
快速、可扩展的检测但有一定限制
该新细胞模型可在约 14 秒内完成单孔测量,并能在大约 22 分钟内扫描完整的 96 孔板,且可适配可同时读取数百孔的仪器。经抗生素选择,工程化细胞在多代中保持稳定,允许随时间重复实验。由于读出为光学信号并使用标准微孔板设备,该方法相对低成本且易于推广。然而,作者指出该检测是间接的:任何作用于 Piezo1 信号链上游或下游步骤的化合物——例如直接作用于 ANO1 或其他钙处理蛋白——都可能产生假阳性。因此,筛选出的命中仍需用更直接的方法(如电生理学)进行确认。
这对未来治疗意味着什么
通俗地说,研究人员构建了一个实验室“烟雾报警器”,每当某个化合物推动 Piezo1 打开时就会变暗,而当 Piezo1 被阻断时则保持明亮。这个报警器灵敏、快速且易于大规模运行,适合用作寻找能调节机体机械感受器药物的第一道筛选。虽然它不能替代更详尽的后续检测,但这一细胞模型为发现可能用于治疗血管疾病、骨病、免疫问题以及其他与细胞感知和响应物理力相关的疾病的分子提供了有力的起点。
引用: Liu, X., Zheng, K., Wang, Y. et al. A functional and robust cellular model for high-throughput screening of piezo1 modulators. Sci Rep 16, 6048 (2026). https://doi.org/10.1038/s41598-026-35673-5
关键词: Piezo1 通道, 机械敏感离子通道, 高通量筛选, 基于细胞的检测, 药物发现