Clear Sky Science · zh
硫化银纳米颗粒通过靶向血管生成和基质金属蛋白酶信号通路对三阴性乳腺癌细胞系的放射增敏作用
让难治的乳腺癌更易被攻克
三阴性乳腺癌是最难治疗的乳腺癌类型之一。它通常生长迅速、早期转移,并且缺乏许多现代药物所依赖的常见分子“靶点”。放疗常作为治疗手段,但这些肿瘤往往对放射顽固耐受。本研究提出了一个简单而有趣的问题:微小的银颗粒能否增强放疗效果,同时抑制肿瘤新生血管生成和扩散能力?
用于放疗的微小银帮手
研究人员将注意力集中在银纳米颗粒上——直径以十亿分之一米计量的超小银球。由于银的密度大且与X射线强烈相互作用,这些颗粒能将放射效应集中在其积聚处。研究团队使用了两种常用的三阴性乳腺癌细胞模型,并与一株非肿瘤性乳腺细胞系进行比较。他们首先测试了银纳米颗粒单独的毒性,发现癌细胞在远低于正常细胞的剂量下被杀死,提示存在一个有利的治疗窗口。通过数学方法分析颗粒与放射的相互作用,结果表明两者联合产生的杀癌效应明显强于任何单一治疗。
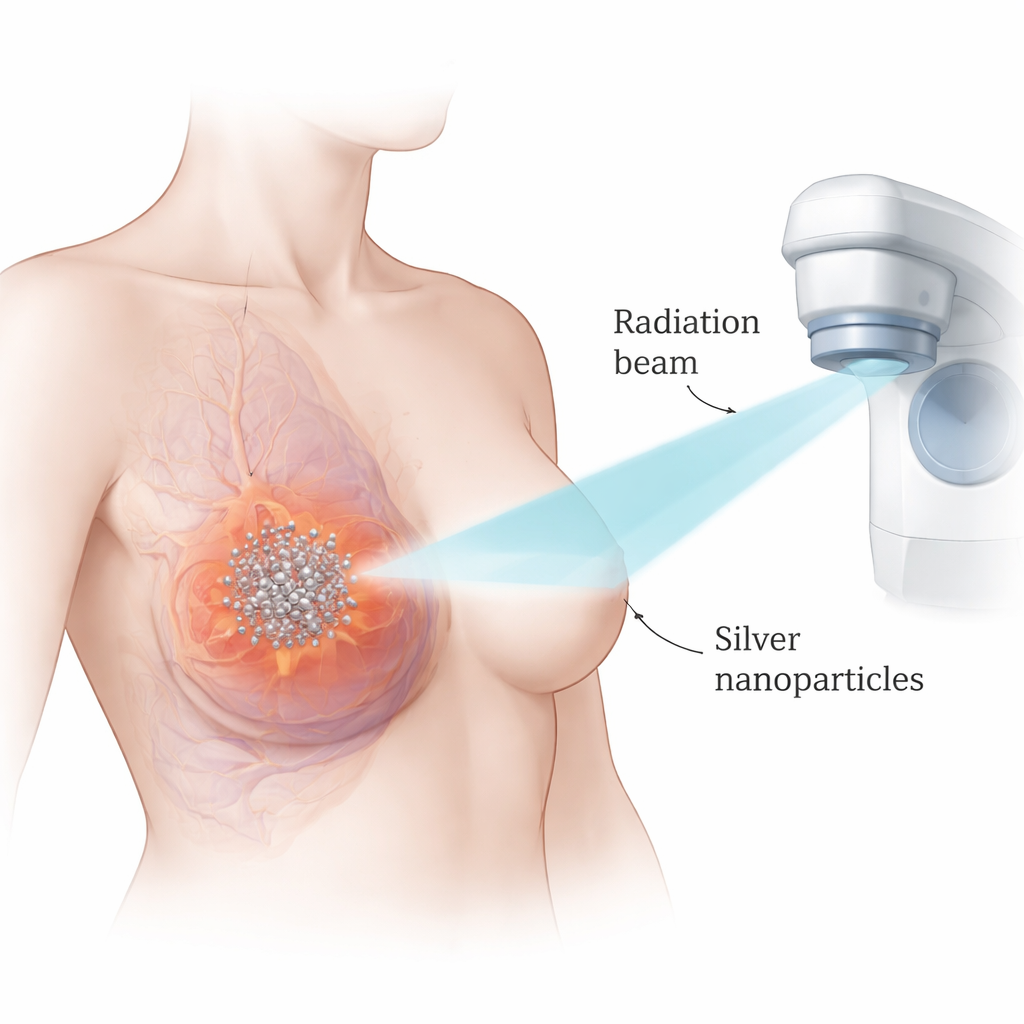
推动癌细胞走向自我毁灭
接下来,科学家们检查了联合治疗是如何杀死细胞的。他们测量了凋亡(一种程序性细胞自杀形式),并追踪了被称为活性氧(ROS)的高反应性分子的积累。众所周知,放射部分通过产生损伤DNA的ROS发挥作用。在两种三阴性乳腺癌细胞系中,银纳米颗粒单独即可提高凋亡和ROS水平,放射单独也能如此——但两者联合使用则使这两项指标显著升高。这意味着更多的癌细胞被推入有序的自毁程序,而不是停留在有损伤但可能导致复发或耐药的状态中。
切断血供并减缓扩散
肿瘤依赖血管输送氧气和营养,侵袭性癌症甚至能模仿血管自身。团队关注了两个参与肿瘤血管构建和稳定的关键分子开关,称为VEGFR2和Tie2。在两种细胞系中,银纳米颗粒降低了这些基因的活性,且与放疗联合后抑制作用更显著。他们还检测了两种酶MMP-2和MMP-9,这些酶帮助癌细胞分解周围组织并迁移。在其中一种细胞模型中,放射和银纳米颗粒均降低了这些酶的水平,而联合治疗效果最强。当科学家观察癌细胞在培养皿中向人工“刮痕”迁移,以及在共培养体系中形成类血管管状结构的能力时,联合治疗最明显地减慢了迁移和管状形成。
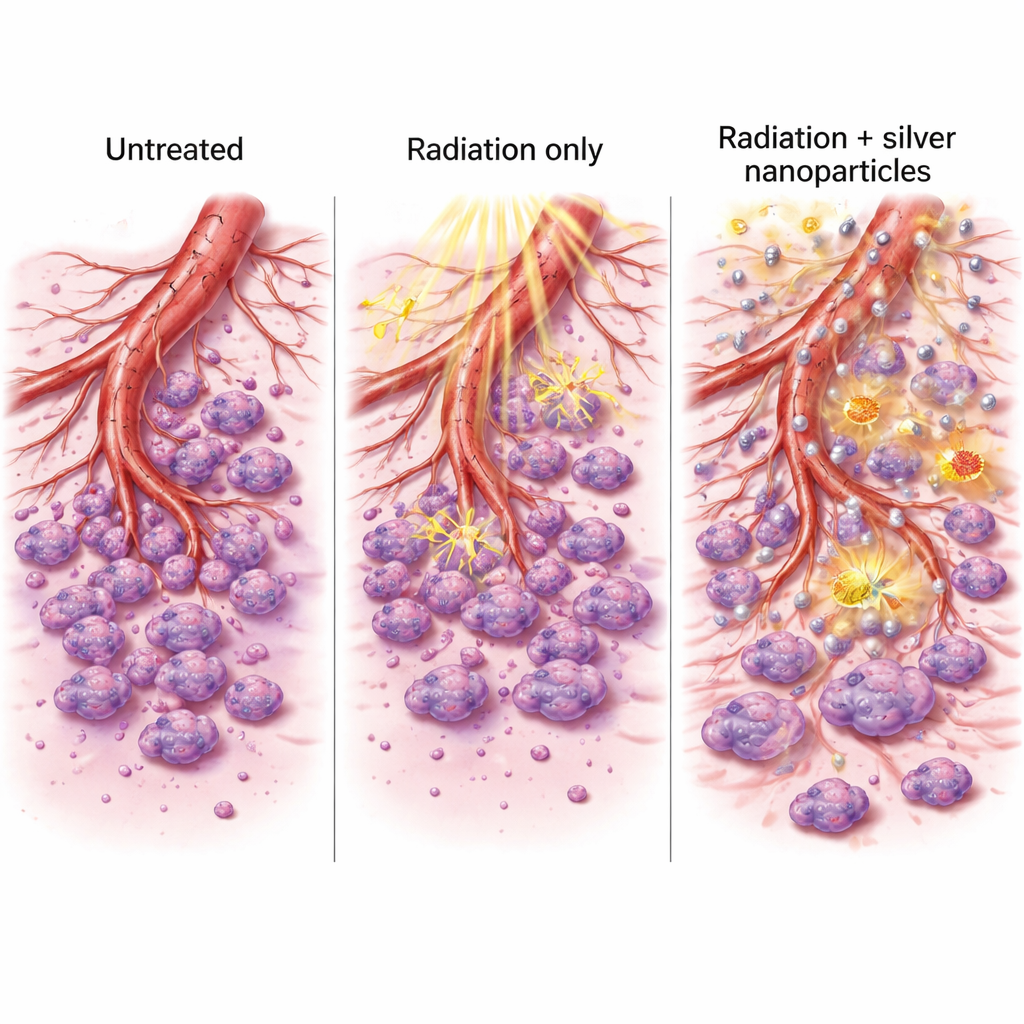
这些变化为何重要
通过下调促进新血管生长的基因和帮助细胞侵袭的酶,银+放射的组合不仅仅是杀死癌细胞。它还破坏了肿瘤扩张和转移所依赖的支持系统。经处理的细胞在实验皿中愈合创口的能力下降,组织成类分支网络(类似早期血管)的能力也减弱。结合凋亡和ROS产生的大幅增强,这些效应提示了双重益处:对肿瘤的直接打击更强,同时削弱了其未来生长和转移的手段。
这对病人可能意味着什么
目前这些结果来自体外培养的癌细胞,而非病人样本或临床试验。尽管如此,它们描绘了一个令人鼓舞的前景。银纳米颗粒表现为放射增敏剂,使标准放疗对三阴性乳腺癌细胞更具效力。与此同时,它们似乎抑制了肿瘤建立血供和侵袭邻近组织的能力。如果未来的动物实验和临床研究确认这些颗粒能被安全且选择性地递送至肿瘤,它们可能帮助医生在使用更低放射剂量的同时获得更好疗效,为对抗这一最具挑战性的乳腺癌类型提供新途径。
引用: Montazersaheb, S., Farahzadi, R., Mansouri, E. et al. Radiosensitizing effects of silver nanoparticles targeting angiogenesis and matrix metalloproteinase signaling in triple negative breast cancer cell lines. Sci Rep 16, 6820 (2026). https://doi.org/10.1038/s41598-026-35662-8
关键词: 三阴性乳腺癌, 银纳米颗粒, 放射治疗, 血管生成, 转移