Clear Sky Science · zh
基于铂类化疗药通过苦味受体在体外的化学感受反应揭示苦味紊乱的新机制
为什么癌症药物会突然让所有东西尝起来很糟
癌症患者常报告在化疗开始后不久食物会变得异常苦或带有金属味。这不仅毁了用餐体验:还会降低食欲、引起体重下降,并在患者最需要力量的时候削弱生活质量。这项研究提出了一个看似简单但具有重大实际意义的问题:常见的铂类化疗药物究竟如何干扰我们的味觉?是否能在不削弱治疗效果的前提下安全地减弱这种影响?
口腔与肠道中“苦味传感器”的隐秘作用
我们的舌头和消化道分布着苦味受体,用来警示可能有害的物质。这些被称为TAS2R的感受器不仅存在于味蕾,还出现在胃等细胞中。研究人员使用了一种人源胃细胞系(HGT-1),它在体外可充当苦味检测器:当苦味受体被激活时,细胞会排出更多质子(酸),可通过一种称为细胞内质子指数的读数变化来测量。通过将这些细胞暴露于两种广泛使用的铂类抗癌药——卡铂和顺铂,团队可以在不让人直接尝有毒化合物的情况下,安全地探查这些药物在人体细胞层面上“多苦”。 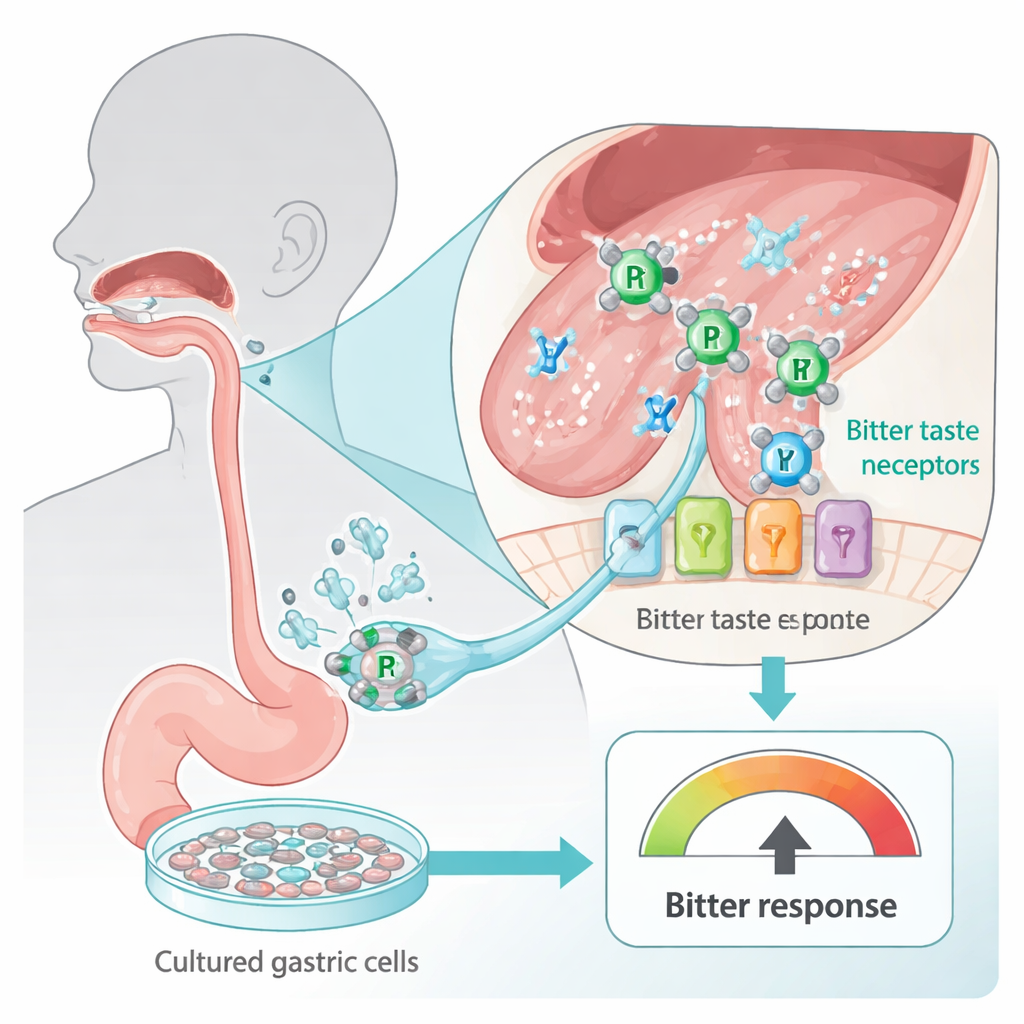
对细胞来说尝起来苦的化疗药物
当胃细胞以临床相关浓度处理卡铂和顺铂时,两种药物都引发了明显的、剂量依赖的类似苦味反应:剂量越高,细胞反应越强。然而,考虑到它们常用的治疗剂量比(约1:4),顺铂产生的反应比卡铂更强烈,这表明顺铂可能在患者的苦味问题中贡献更大。在基因水平上,暴露于这些药物改变了细胞中多个苦味受体基因的活性,这表明铂类药物并非仅作用于单一的“苦味开关”,而是广泛重塑苦味感知系统。其中,TAS2R4和TAS2R5表现出既高度活跃又受到处理强烈影响的特征。
关闭苦味信号并测试一种天然苦味阻断剂
为确定哪些受体最重要,团队选择性地使特定苦味受体失活。敲除TAS2R4或下调TAS2R5均能降低对卡铂和顺铂的类似苦味响应,证实这些受体帮助感知药物。随后,科学家测试了一种有前景的对策:homoeriodictyol的钠盐(Na-HED),这是一种最初从北美植物Herba Santa中分离出的黄烷酮,已知能掩盖其他化合物的苦味。当Na-HED与铂类药物同时加入时,它显著减弱了细胞的苦味反应——对卡铂和顺铂均约降低四分之三左右——且Na-HED本身对细胞无害。这表明Na-HED可以直接作用于苦味受体,钝化化疗药物触发的信号。
苦味感知与药物进入交汇的时刻
除了说明为什么铂类化疗可能尝起来苦之外,研究还揭示了一个出人意料的转折:相同的苦味受体似乎也影响这些药物进入细胞的多少。研究人员使用高灵敏度质谱测量处理后细胞内的铂含量。缺乏某些受体(如TAS2R4或TAS2R43)的细胞比正常细胞积累了更多铂,提示完好的受体有助于限制这些有毒物质的细胞摄取或滞留。Na-HED未改变卡铂的摄取,但确实减少了进入细胞的顺铂量,并在溶液中显示出与顺铂的直接分子互作。这暗示苦味掩盖化合物在某些情况下也可能调节药物对局部组织(如味觉细胞或唾液腺)的影响强度。 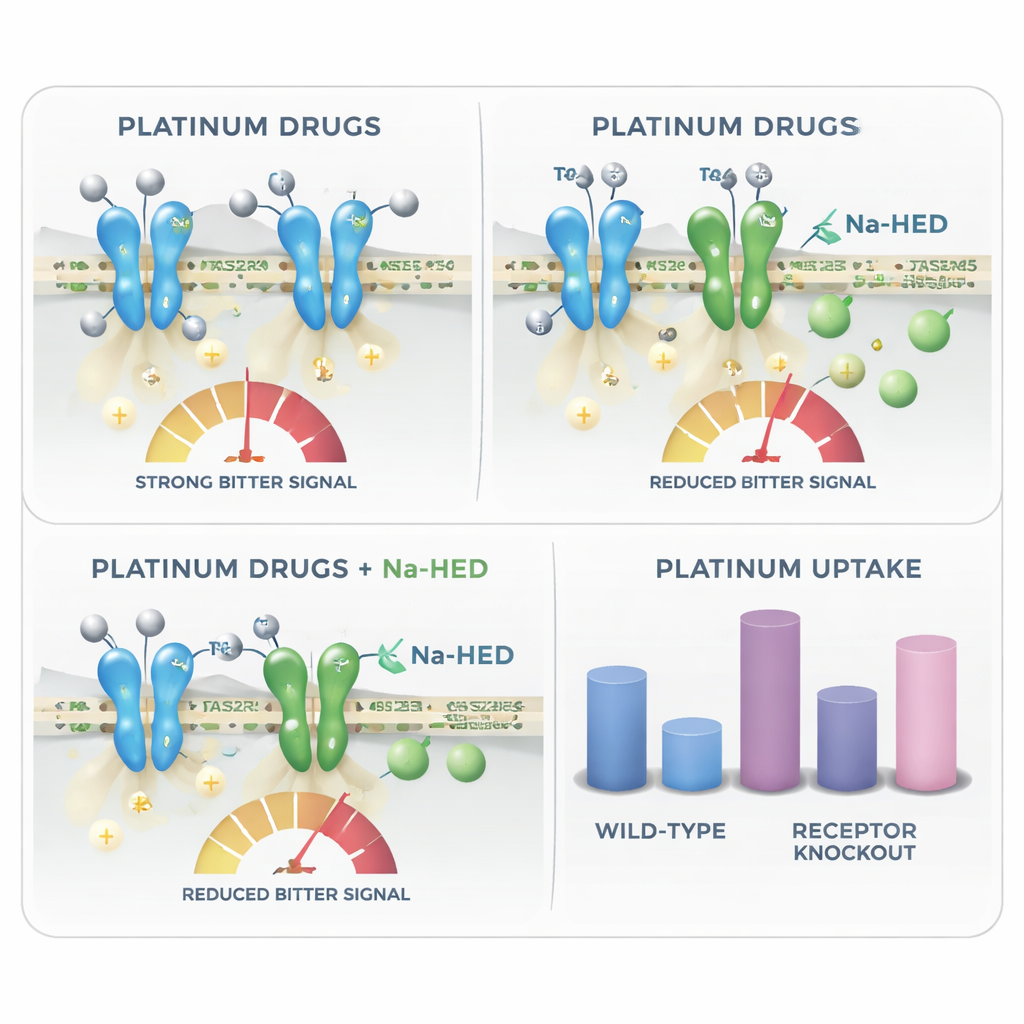
迈向化疗期间更温和的味觉体验
对患者而言,主要结论是带来希望的:铂类化疗似乎通过直接激活不仅存在于舌头上也存在于类肠细胞中的苦味受体,从而诱发苦味问题。顺铂在这方面表现尤为强烈。研究表明,在可控的细胞体系中Na-HED可以显著抑制这一苦味信号,且可能还会限制顺铂在局部的摄取。尽管这些发现需要在人体中得到验证,但它们指向未来可行的“漱口并吐出”口腔处理方案,含Na-HED的制剂可能在不干扰药物在全身抗癌作用的前提下,缓和刺鼻的苦味和金属感。
引用: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
关键词: 化疗导致的味觉变化, 苦味受体, 顺铂与卡铂, 苦味掩盖化合物, 癌症患者营养