Clear Sky Science · zh
使用密度泛函理论计算 Ac3+ 与 Bi3+ 与混合螯合剂 3p-C-DEPA 在靶向α治疗中的配位
这项研究对癌症治疗的重要性
现代癌症医学越来越依赖能逐个肿瘤细胞定位的放射性药物。一种名为靶向α治疗的强效方法使用能量极高的粒子,能够以惊人的精确度杀死单个癌细胞。但为安全递送这些粒子,放射性金属必须被锁在一个微小的分子“笼”中,以防其游离到健康组织中。本研究探索了一种新的笼状分子3p‑C‑DEPA,旨在束缚像镭系‑225和铋‑213等特别具有挑战性的金属,并提出问题:它能否比当前常用的螯合剂DOTA更牢固地结合这些金属?
安全地锁住放射性金属
放射性金属如镭(actinium)、铋和镥被用于癌症的诊断和治疗。然而,这些带正电的金属离子单独存在时会在体内自由相互作用,可能损害健康器官。因此化学家将它们连接到“螯合剂”上——环状分子包裹金属并将其固定。被广泛采用的金标准螯合剂DOTA已用于若干获批药物,但它在处理诸如镭系‑225等体积更大、电荷更分散的离子时存在困难。这些金属可能随着时间从笼中脱出,引发长期安全性问题并限制靶向α治疗的应用范围。
为更大原子打造的混合笼
新型螯合剂3p‑C‑DEPA结合了两种既有设计的特征:DOTA的刚性环状骨架和另一种螯合剂DTPA的更灵活、开放的结构。这种混合结构使3p‑C‑DEPA拥有十个强结合“手”(氮和氧原子),而DOTA只有八个,并且具有更宽敞的空腔,更能容纳大型金属离子。早期的实验室工作表明3p‑C‑DEPA能在温和条件下快速标记抗体,并在血清中稳定地保持基于铋的放射性核素。本研究迈出下一步,使用量子级别的计算系统地比较3p‑C‑DEPA和DOTA对镥‑177、铋‑213和镭系‑225的结合能力。
窥视分子间的“握手”
由于直接处理短寿命α发射体具有困难,研究者转向密度泛函理论(DFT),这是一种强大的计算方法,可估算分子中电子的排布以及原子间的相互吸引强度。他们在水环境中对每个金属离子建模,然后建模其与DOTA或3p‑C‑DEPA形成的配合物,并计算金属从水相进入螯合剂笼时自由能的变化。该能量变化可转换为“稳定常数”:数值越高,螯合剂对金属的束缚越紧密。研究使用了两种不同的DFT方法和两种溶剂化模型,以模拟更真实的溶液条件,并检验趋势是稳健的,而非单一计算设置的伪像。
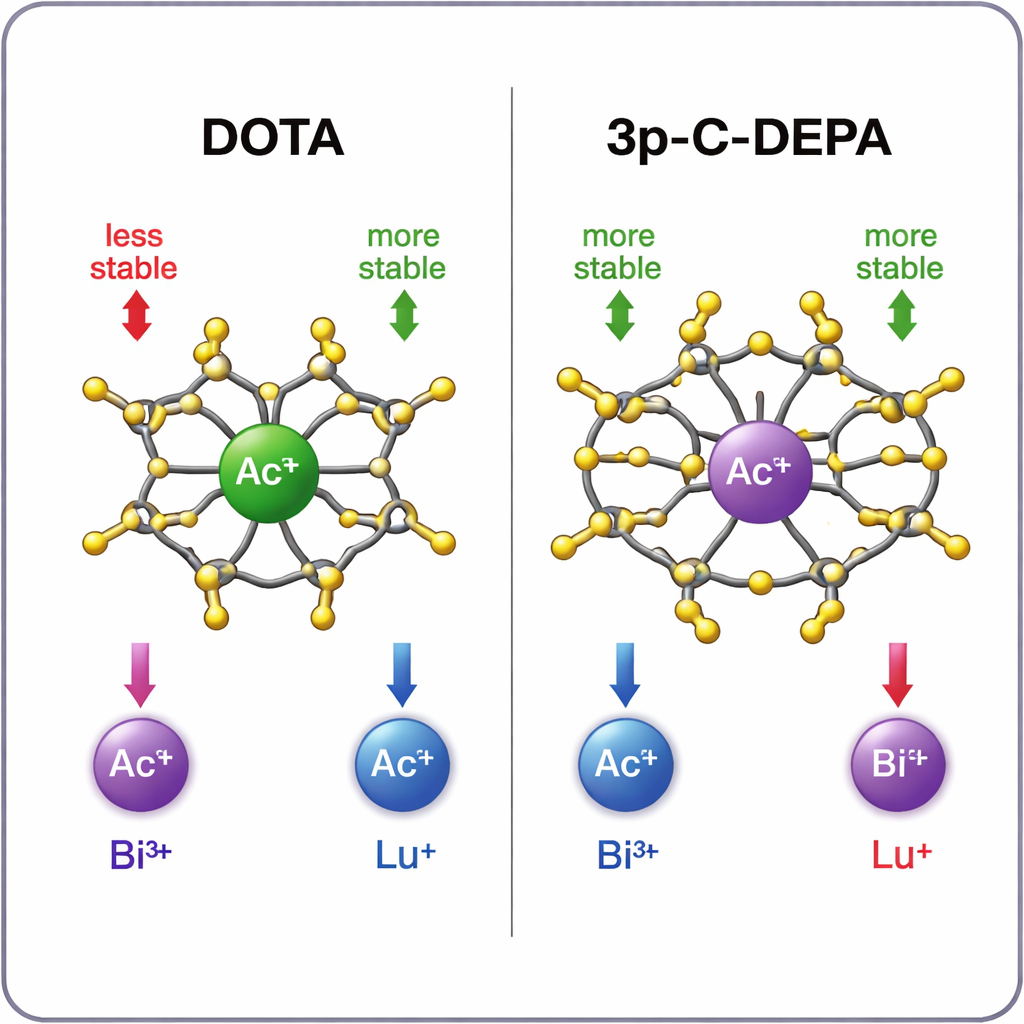
哪个笼子最适合哪种金属?
模拟结果显示出清晰的模式。对于体积较大的镭系离子,3p‑C‑DEPA比DOTA形成明显更稳定的配合物,这归功于其更大的空腔和更多的氧供体可以牢牢抓住金属。铋‑213也能很好地被3p‑C‑DEPA容纳,既受益于其尺寸,也受益于其电子接受特性,这与螯合剂的电子供体基团相匹配。相反,较小的镥‑177更适合DOTA更紧凑、八臂的环境。在3p‑C‑DEPA中,多余的供体基团在小离子周围产生拥挤,导致排斥相互作用,这似乎减慢了标记速度并略微削弱了最终配合物。计算得出的稳定性趋势与现有的实验数据和放射标记产率吻合良好,从而为理论预测提供了可信度。
这对未来癌症疗法的意义
通俗地说,该研究表明DOTA并非万能笼子:它对像镥这样较小的金属非常有效,但对于体积更大的α发射体如镭系‑225则并非最佳。相比之下,3p‑C‑DEPA更像为这些大离子量身打造的托架,在更温和的条件下更紧密地抓住它们,更适合用于抗体等敏感的靶向分子。虽然仍需进一步的实验和临床研究,但这些计算结果将3p‑C‑DEPA指向一种有前景的骨架,有望用于更安全、更有效的靶向α治疗——可能扩大对高效癌症疗法的可及性,使其在毁灭肿瘤的同时尽量避免损伤周围健康组织。
引用: Ramdhani, D., Watabe, H., Ahenkorah, S. et al. DFT calculation of Ac3+ and Bi3+ complexation with hybrid chelator 3p-C-DEPA for targeted alpha therapy. Sci Rep 16, 6587 (2026). https://doi.org/10.1038/s41598-026-35633-z
关键词: 靶向α治疗, 放射性药物, 螯合剂设计, 镭系-225, 密度泛函理论