Clear Sky Science · zh
携带早老素-1 突变的人源 iPSC 衍生神经元在压力下出现线粒体功能障碍和 Ca2+ 失调,且通过一种非 MCU-1 依赖机制产生
这对阿尔茨海默病为何重要
阿尔茨海默病常被描述为大脑中粘性的蛋白斑块,但在记忆衰退之前很久,神经细胞内的微小“发电厂”——线粒体——以及对钙离子的处理可能已经出现问题。本研究利用来自携带一个知名家族性阿尔茨海默突变的人的皮肤细胞培养而成的人类神经元,提出一个简单但关键的问题:能量产生与钙平衡究竟在多早、以何种方式开始失衡?
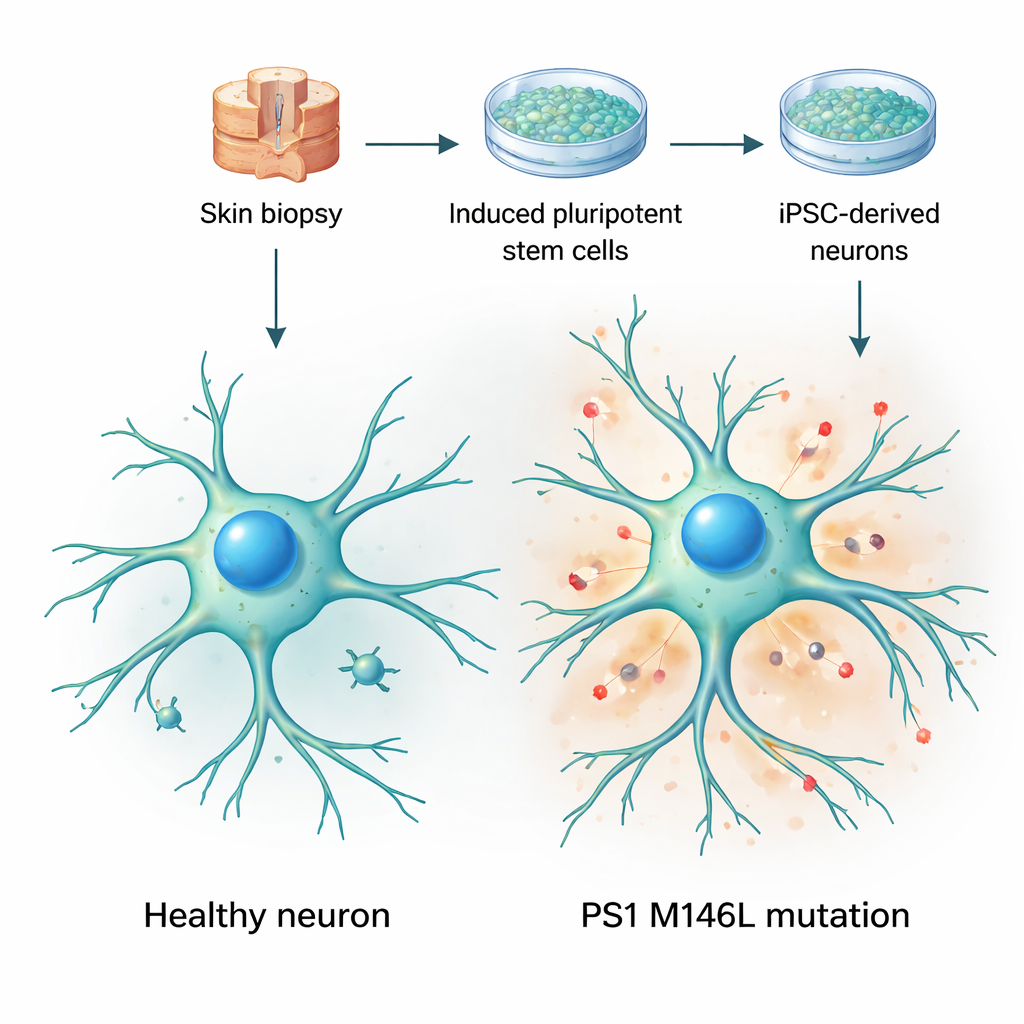
将皮肤细胞变成活体大脑模型
研究者从两位女性的皮肤活检开始:一位健康志愿者和一位无症状但携带称为 M146L 的早老素‑1 突变的携带者,该突变在一个阿根廷的早发家族性阿尔茨海默病例中流行。他们将皮肤细胞重编程为诱导多能干细胞——能够分化为几乎任何组织的细胞——然后诱导其分化为神经元。在培养数周后,这些细胞获得了典型的神经元形态,伸展出长而分枝的突起,并表达常见的神经元标志物。重要的是,对照组和突变组细胞的成熟速度相似,且总体上外观健康,这使团队能够关注细微的功能变化,而不是明显的细胞丧失或损伤。
电信号与受压下的钙
神经细胞依赖对钙的严格控制,钙是一种带电原子,作为许多细胞过程的快速开关。研究团队使用荧光染料追踪在用钾电刺激或用信号分子激活时细胞内钙水平的变化。在简单的去极化刺激下,携带 M146L 突变的神经元显示出比对照神经元更弱的钙升高,提示维持通常驱动钙进入的电和离子梯度方面存在问题。然而,当研究者引发更具应激性的情形——促使内质网内的钙泄漏时,差异变得更明显。对此类压力,突变神经元的线粒体摄取的钙明显少于对照细胞,表明其缓冲危险性钙激增的能力降低。
能量使用与钙平衡解耦
为了解这种改变的钙处理如何影响细胞代谢,研究者测量了神经元消耗的氧气量——这是线粒体活性的直接代理。令人意外的是,携带 M146L 突变的神经元呼吸更剧烈:其基础与最大氧耗率以及与 ATP 生成相关的耗氧量均高于对照细胞。然而,耗氧与 ATP 生成耦合的效率似乎相近,且线粒体数量或关键产 ATP 酶并未增加。相反,突变神经元的线粒体更长、更呈管状,且融合蛋白缝合蛋白‑1(mitofusin‑1)水平更高,这一模式常见于长期低水平应激下的细胞。这些过度活跃、延长的线粒体也产生了更多的活性氧——如果不能被适当控制,这些不稳定分子会损害蛋白质和 DNA。
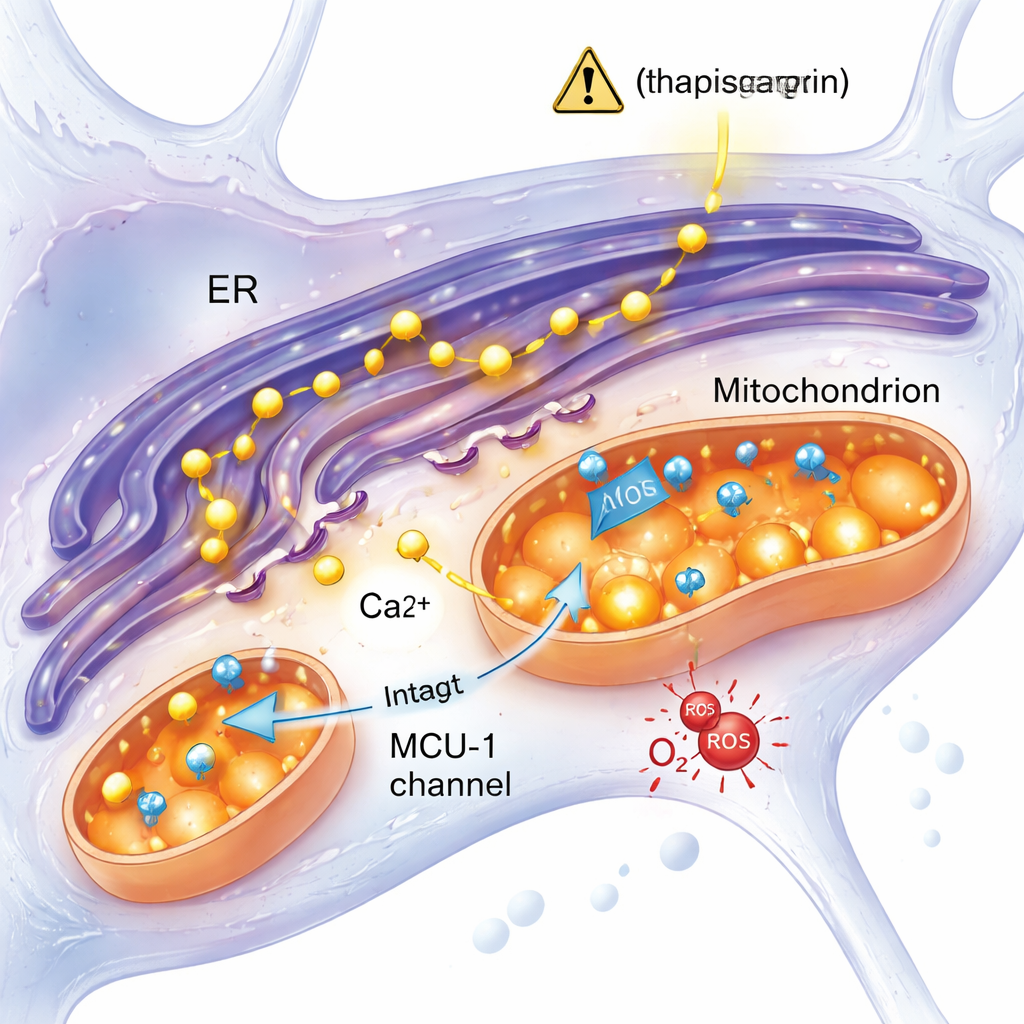
一种独立于关键钙通道的应激反应
阿尔茨海默研究中的一个主要设想是,来自内质网的过量钙通过一种称为线粒体钙一体化转运体(MCU‑1)的通道涌入线粒体,导致过载并驱动功能障碍。本研究直接检验了这一观点。当团队用特异性抑制剂阻断 MCU‑1 时,对照组和突变组神经元的线粒体钙摄取均显著减少,证实该通道在两组中均可工作。此外,当通过涉及 IP3 受体的更生理性的通路触发钙释放时,突变和对照细胞的反应相似。这些结果并不支持 MCU‑1 通道本身损坏的解释,而是提示内质网与线粒体之间的物理和功能接触,或它们相互作用的其他方面,在突变神经元中发生了改变。
对理解和治疗疾病的意义
综合来看,研究结果描绘出携带 PS1 M146L 阿尔茨海默突变的人源神经元:在静息时看起来正常,但在应激下反应异常。它们的线粒体在内源储钙突然释放时无法摄取足够的钙,然而却更“发热”——消耗更多氧气并产生更多活性氧,仿佛处于一种代价高昂的补偿状态。由于这些变化出现在临床症状出现之前的活体人源神经元中,这项工作支持了这样一种观点:钙信号扰动和早期线粒体过度工作是阿尔茨海默病的上游事件,而不仅仅是末期的副产物。对非专业读者而言,关键讯息是:维持钙信号与线粒体能量产生之间的平衡,可能与靶向更广为人知的淀粉样斑块一样,对预防疾病至关重要。
引用: Wilson, C., Galeano, P., Remedi, M.M. et al. Mitochondrial dysfunction and Ca2+ dysregulation in human iPSC-derived neurons carrying presenilin-1 mutation arise under stress via an MCU-1-independent mechanism. Sci Rep 16, 6002 (2026). https://doi.org/10.1038/s41598-026-35597-0
关键词: 阿尔茨海默病, 线粒体, 钙信号, 早老素-1 突变, iPSC 衍生神经元