Clear Sky Science · zh
基于结构与计算支持的2,5-二取代-1,3,4-噁二唑类似物作为有效LOX、脲酶和α-葡萄糖苷酶抑制剂的开发
应对常见疾病的新化学工具
许多日常健康问题——从溃疡和肾结石到糖尿病和慢性炎症——都源于体内某些酶活性过高。本研究探索了一类新设计的小分子,它们像微小的刹车一样作用于三种此类酶。通过调节分子结构并在实验室与计算机上测试,研究人员旨在为未来更有效、更安全的药物奠定基础。 
这些酶为何重要
团队聚焦于三种在健康中扮演截然不同但同样重要角色的酶靶点。脲酶有助于分解尿素;当其在某些细菌或组织中过度活跃时,可能促成胃和泌尿道溃疡、肾结石,甚至导致血压升高。α-葡萄糖苷酶位于肠道细胞表面,将复杂碳水化合物切分为葡萄糖;抑制它是控制2型糖尿病血糖的成熟策略。脂氧合酶(LOX)将脂类转化为驱动炎症、哮喘及某些与癌症相关过程的信号分子。因此,能够在不损害其他系统的情况下降低这些酶活性的药物备受追捧。
构建候选分子库
为寻找此类药物,研究人员构建了一系列基于1,3,4-噁二唑环系并连接哌啶单元的15种相关化合物。该化学骨架已出现在多种现代药物中,且已知能良好地与生物靶点相互作用。团队在该核心上改变了“装饰”——例如甲基、乙基、甲氧基、苄基与环己基等小基团,在不同位置进行取代,构建了标记为7a到7o的小型候选库。他们使用红外和核磁共振等标准分析手段确认每个结构,确保所合成的化合物与设计一致。
测试分子对酶的抑制效果
随后对每种化合物进行了纯化的LOX、脲酶和α-葡萄糖苷酶抑制测试,以评估它们减缓酶活性的能力。有若干化合物表现突出。在抑制α-葡萄糖苷酶方面,化合物7a和7n尤其有效,在低微摩尔浓度下实现了高抑制率,实验室测试中优于标准糖尿病药物阿卡波糖。对于LOX,7a、7h和7n显示出非常强的活性,在某些情况下优于天然参考抑制剂槲皮素。在脲酶测定中,7a,尤其是7l,与标准抑制剂硫脲不相上下或略有超越,表明它们未来可能成为抗溃疡或抗结石治疗的先导分子。 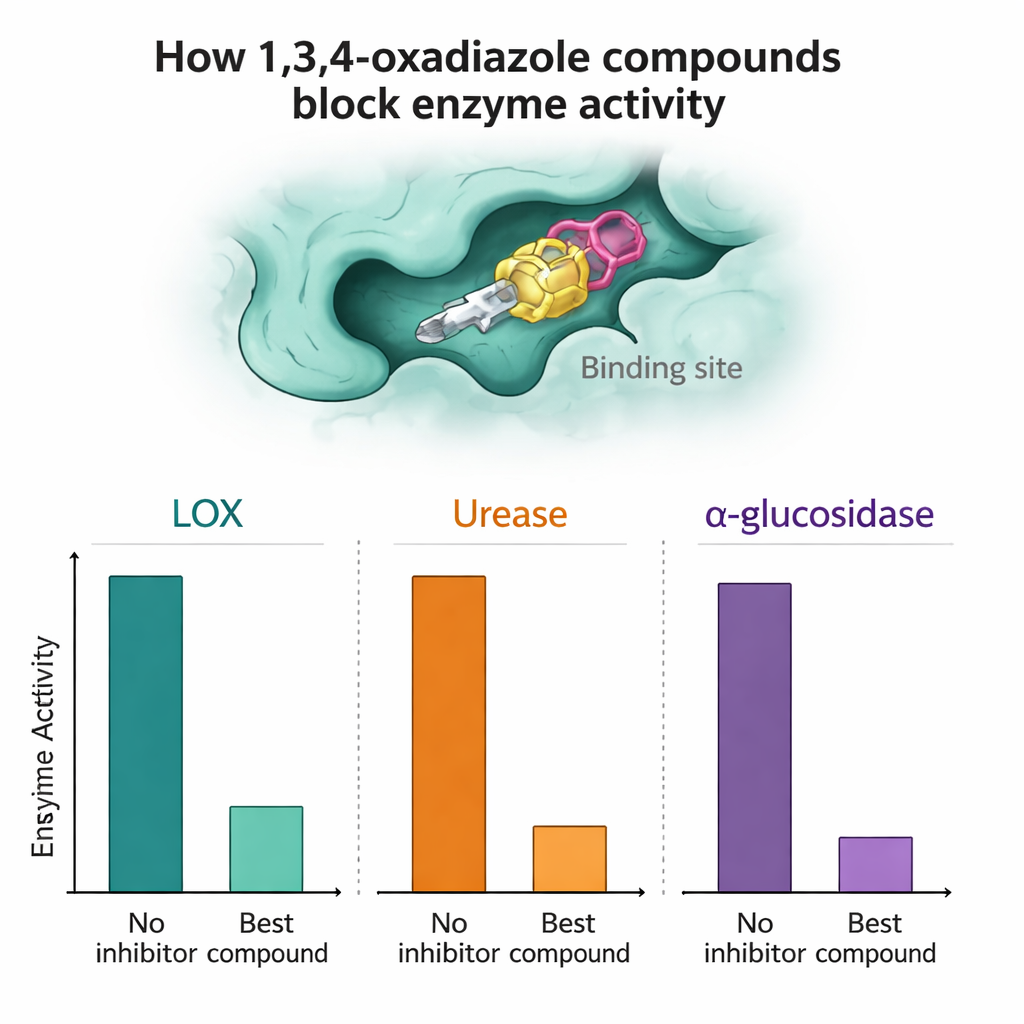
将结构与性能关联
由于7a–7o之间的差异仅是围绕核心环系的小改动,研究人员得以绘制出简单的构效关系。例如,在连接环的某些“邻位”位置引入小的富碳基团,通常能增强阻断α-葡萄糖苷酶或LOX的能力。其它取代基,如某些放置不利的甲氧基或酯基,往往削弱活性。为了解原因,团队采用了计算模拟。量子化学计算显示所有分子在热力学上稳定且具有足够柔性以适应酶的结合口袋。对接研究——将每个分子虚拟置入酶的三维模型中——揭示出最活跃的化合物通过氢键和疏水(类油)相互作用在活性位点关键位置形成更紧密的接触,而较弱的候选物则较松散地结合或错过了关键接触点。
对未来药物开发的意义
通俗来说,该研究识别出若干能够很好地吻合三种疾病相关“锁”的有前景“钥匙”,并开始在原子水平上解释为何某些钥匙转动得更顺畅。这些分子尚未准备好成为药物——它们仍需安全性测试、体内行为优化以及动物与人体试验。但这项工作表明,1,3,4-噁二唑–哌啶框架是针对糖尿病、炎症性疾病和与脲酶相关疾病的有前景起点。精确的实验测量与详尽的计算建模相结合,为将这些候选分子打磨成更精确、更有效的药物提供了路线图。
引用: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
关键词: 酶抑制剂, 药物发现, 噁二唑化合物, 糖尿病与炎症, 脲酶与脂氧合酶