Clear Sky Science · zh
SHP2 通过调控 STAT3/TET3/HOXB2 信号通路促进骨肉瘤进展
这项骨癌研究为何重要
骨肉瘤是儿童和青少年中最常见的原发性骨癌,尽管现代化疗和手术技术不断进步,晚期或复发患者的生存率在几十年间几乎没有明显改善。本研究深入解析了骨肉瘤细胞的内部信号网络,以找出哪些分子充当帮助肿瘤生长、转移和耐药的“主开关”。通过发现以蛋白质 SHP2 为中心的一条关键控制通路,研究指向了未来可能使骨肉瘤治疗更有效、更精准的新型药物靶点。
沿着肿瘤基因活动找线索
研究人员首先将骨肉瘤视为一个数据问题来处理。他们挖掘了公开的基因表达数据集,将肿瘤样本与正常骨组织比较,然后用统计工具识别在癌症中持续上调或下调的基因。数百个基因存在差异,且其中许多聚集在驱动细胞生长、生存与迁移的已知癌症通路中。在这些基因中,一个蛋白质——SHP2——突出成为与多种其他分子紧密相关的枢纽:信号因子 STAT3、DNA 修饰酶 TET3 和发育调控因子 HOXB2。这提示这些分子可能构成一条相互联结的链,推动骨肉瘤细胞表现出侵袭性行为。 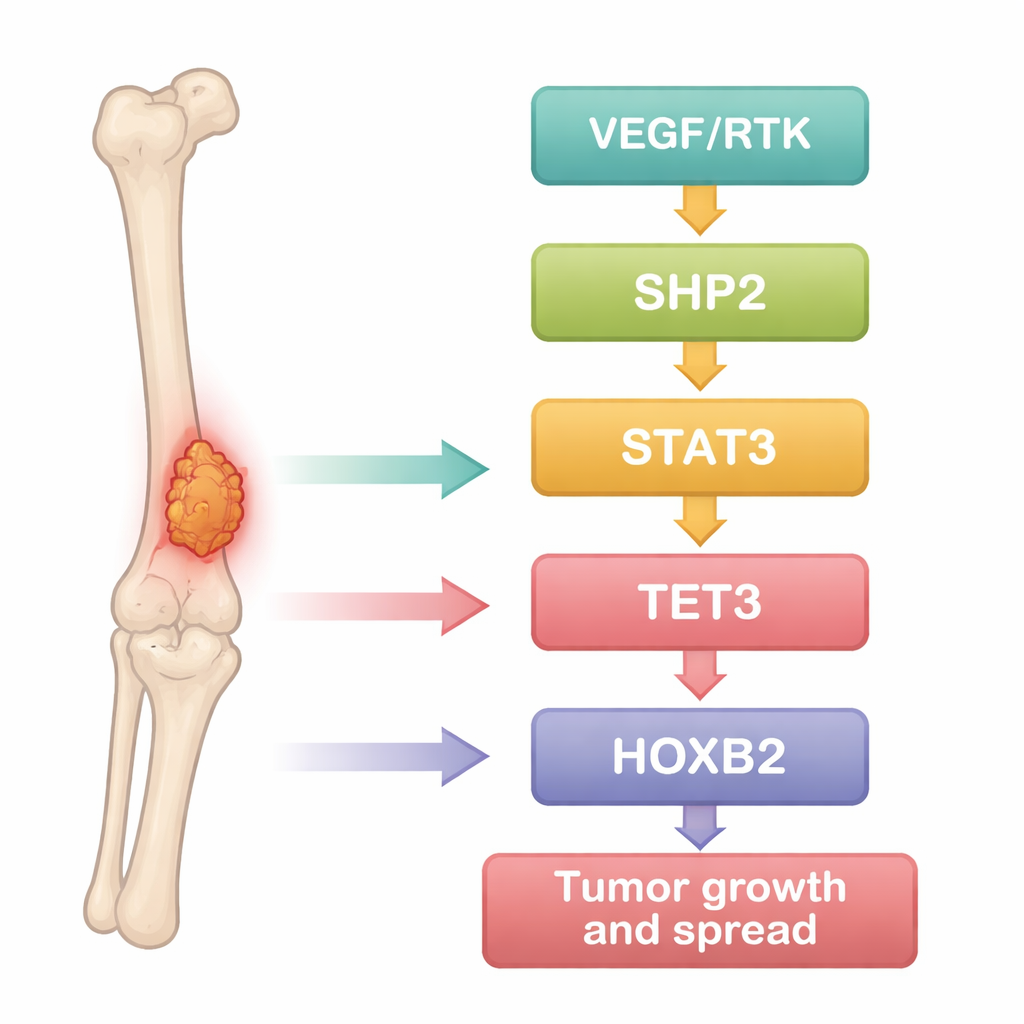
在癌细胞中检验 SHP2 的作用
为了超越相关性,研究团队对人类骨肉瘤细胞系(143B 和 MG63)进行了工程改造,使其降低或增强 SHP2 表达。敲低 SHP2 后,细胞的增殖能力、表面迁移和穿膜侵袭显著下降。STAT3、TET3 和 HOXB2 蛋白的水平,以及与癌症相关的标志物如 c-Myc、NANOG 和 NUSAP1 也随之降低。当重新激活 STAT3 或过表达 HOXB2 时,许多这些效应被逆转,表明 SHP2 位于一条上游链条,最终影响控制细胞分裂、干细胞样特性和细胞分裂机制的基因。
构建逐步的癌症通路模型
将实验结果拼接在一起,作者提出了一个分步模型。在肿瘤微环境中,高水平的血管内皮生长因子(VEGF)刺激细胞表面的受体酪氨酸激酶(RTKs)。这些受体随后在细胞内激活 SHP2。活化的 SHP2 启动 STAT3——一个转录因子——其转入细胞核并促进 TET3 的表达增加。TET3 随后编辑 DNA 上的化学修饰,具体是从 HOXB2 基因区域去除甲基。该去甲基化过程类似于解除刹车,使 HOXB2 得到更强表达。HOXB2 是一个通常在发育中起导向作用的基因,如今增强了 c-Myc、NANOG 和 NUSAP1 的活性,这些基因共同驱动肿瘤细胞持续生长、强化侵袭行为并支持与转移相关的特征。
从培养皿到活体动物
为了验证这一路径在完整肿瘤中的重要性,科学家们将改造过的骨肉瘤细胞皮下接种到小鼠体内。过表达 SHP2 的细胞形成的肿瘤比对照肿瘤更大、更重。当在这些 SHP2 丰富的细胞中沉默 TET3 时,肿瘤生长放缓且 HOXB2 水平下降,即便 SHP2 和 STAT3 仍然处于活性状态。重新引入 HOXB2 又恢复了肿瘤的活力。整体来看,肿瘤组织中蛋白水平的测量与早期细胞培养结果相呼应,强化了 SHP2、STAT3、TET3 与 HOXB2 构成连接轴,推动骨肉瘤向更恶性表型发展的观点。 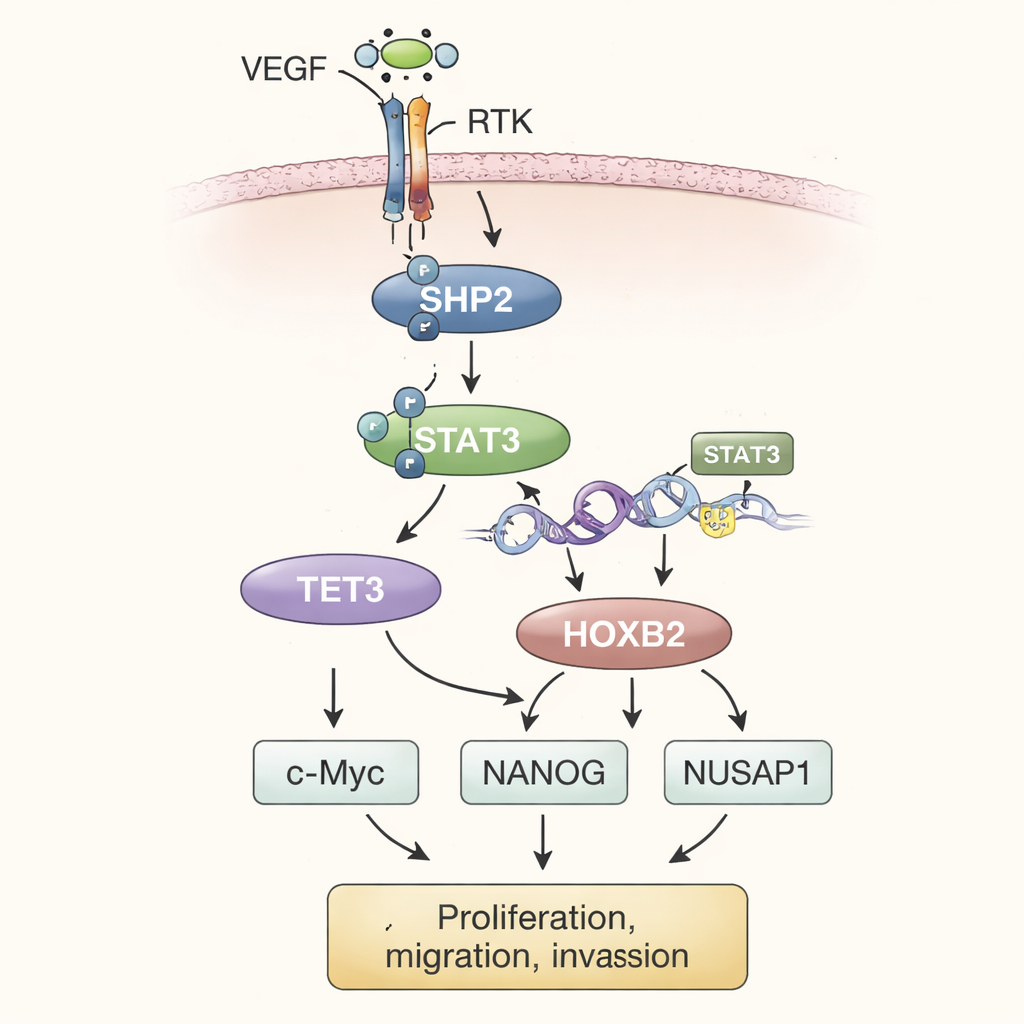
对未来治疗的意义
对非专业读者来说,关键结论是:研究者绘制出了一条清晰的信号链——从 VEGF 及其表面受体,经由 SHP2 和 STAT3,到 TET3、HOXB2 及若干强效促生长基因——这条链有助于解释骨肉瘤为何能快速生长并早期转移。由于 SHP2 和 STAT3 是可以通过小分子药物原则上被抑制的酶,而 TET3 与 HOXB2 标示了同一路径的后续步骤,该通路提供了多个未来疗法可以干预的节点。尽管本研究在细胞系和小鼠模型中完成,但它为药物开发者提供了一张详细地图,便于设计旨在关闭肿瘤中央控制开关的组合疗法,而不仅仅是攻击肿瘤的末端效应。
引用: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
关键词: 骨肉瘤, SHP2, STAT3 通路, 肿瘤信号, 靶向治疗