Clear Sky Science · zh
使用靶向ROS的放射性示踪剂通过无创PET成像检测LPS诱导的骨骼肌氧化应激
为何肌肉受压重要
随着年龄增长、感染斗争或长期卧床,肌肉会收缩并变弱。许多这种隐性损伤在肌肉体积明显变化之前就已开始,其驱动因素是称为活性氧(ROS)的不稳定分子。本研究探讨了一种通过PET医学成像“看见”肌肉内这种不可见化学应激的新方法,可能让医生在肌肉丧失变得难以逆转之前及早发现问题。 
更近距离地观察不可见的肌肉应激
骨骼肌萎缩是肌肉质量和力量逐渐丧失的过程,可因衰老、重病、不活动或化疗等治疗而发生。传统上,医生依赖活组织检查、MRI或CT等工具评估肌肉健康。这些方法能显示尺寸和结构的变化,但无法呈现启动损伤的早期化学信号。其中最早且最重要的信号之一是氧化应激——即ROS过载扰乱细胞的化学平衡并激活分解肌肉蛋白的通路。能够在活体肌肉中直接测量这种应激,有助于识别高风险人群并追踪旨在保护肌肉的治疗是否有效。
能标记有害分子的示踪剂
研究者将注意力集中在一种名为[18F]ROStrace的专用PET成像示踪剂上,它设计用于定位超氧,这是一种主要类型的ROS。在确认该示踪剂可可靠制备并在数小时内保持稳定后,研究人员在体外培养的肌肉细胞中测试了它对氧化应激的响应。暴露于可触发炎症和ROS的细菌毒素LPS的小鼠肌肉细胞(C2C12肌管)随着时间累积了比未处理细胞更多的[18F]ROStrace。当用抗氧化药物保护细胞时,示踪剂摄取减少;当用另一种化合物提高ROS时,摄取增加。这些模式表明,示踪剂信号随ROS水平增减而变化,而不是与细胞形态或代谢的普遍改变一致。 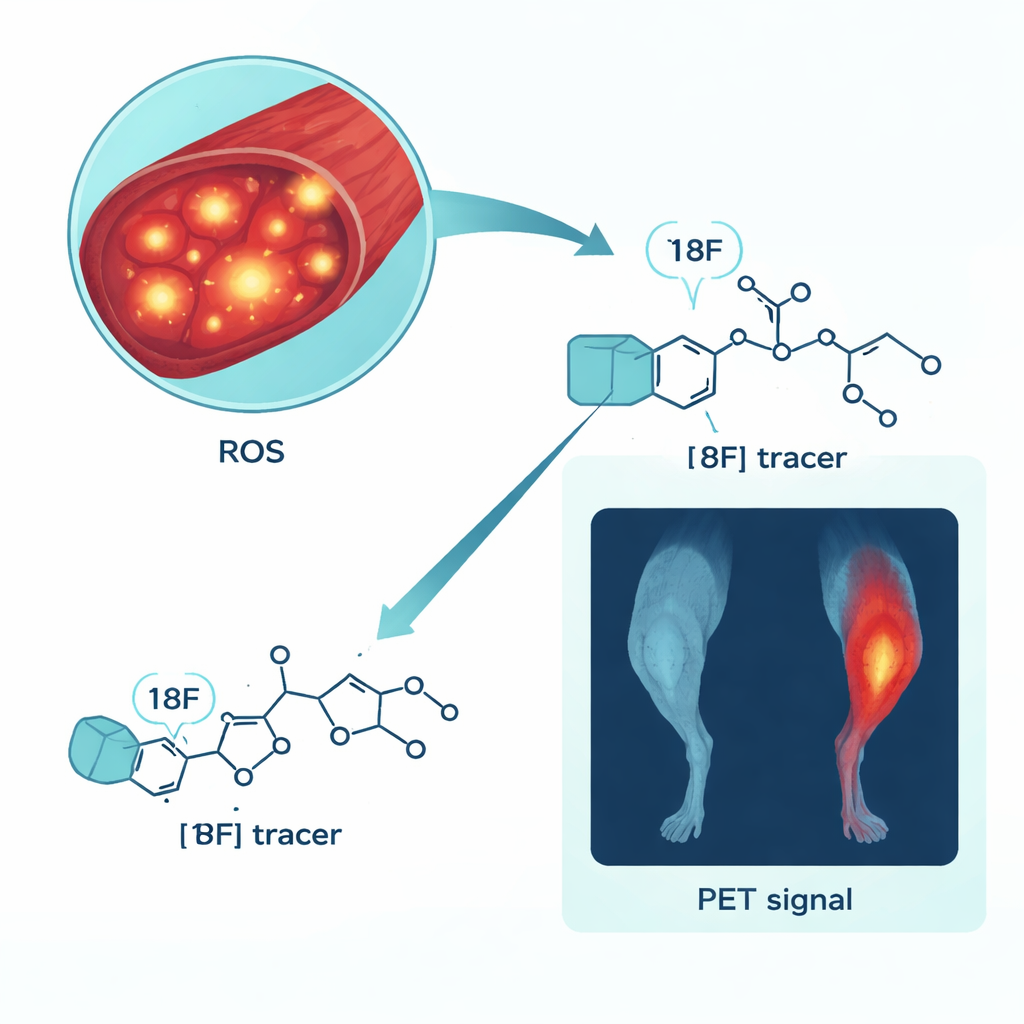
从培养皿到活体肌肉
接着,研究团队在小鼠上测试[18F]ROStrace是否能揭示真实肌肉组织中的氧化应激。研究者给小鼠注射LPS以诱发全身炎症状态,造成肌肉早期消耗的迹象。约一天后使用PET/CT对动物进行扫描,测量后肢肌肉中的示踪剂摄取。与健康对照小鼠相比,LPS处理组在这些肌肉中的PET信号大约翻倍,表明氧化负担明显更高。时间过程扫描显示肌肉中示踪剂水平在注射后约一小时左右达到稳定平台期,为未来研究和潜在临床转化定义了一个实用的成像窗口。
亮信号背后的生物学线索
为了证实PET图像确实反映的是有害化学过程而非血流或其他非特异性效应,研究人员使用多种标准实验室方法分析了相同的肌肉组织。在显微镜下,LPS处理的肌肉和培养的肌管显得更薄,单个肌纤维的横截面积更小——这些特征与萎缩早期阶段一致。线粒体作为细胞的能量工厂,显示膜电位下降,这是在氧化应激下内部平衡受扰动的标志。驱动肌肉分解的关键基因MuRF-1和Atrogin-1在LPS处理的细胞和组织中明显升高。最后,使用与[18F]ROStrace化学性质密切相关的荧光染料染色证实,在呈现更强PET信号的肌肉中,无论是在细胞培养还是在活体小鼠中,ROS水平确实更高。
这对患者可能意味着什么
总体来看,研究结果表明[18F]ROStrace PET可以无创地标出骨骼肌中氧化应激的热点,且信号强度与其他早期肌肉损伤特征相一致。对普通患者而言,这一方法有朝一日可能提供在明显消耗发生前检测肌肉应激的手段,监测新药或运动方案在抑制有害化学反应方面的效果,并更好地理解从败血症相关无力到年龄相关虚弱的各种状况。尽管需要进一步的长期和人体研究,这一靶向ROS的成像工具为理解肌肉何时以及如何开始失能、以及如何更早介入,打开了一扇新的窗口。
引用: Park, J.Y., Park, S.M., Lee, T.S. et al. Noninvasive PET imaging of LPS-induced oxidative stress in skeletal muscle using a ROS-targeting radiotracer. Sci Rep 16, 4917 (2026). https://doi.org/10.1038/s41598-026-35489-3
关键词: 肌肉萎缩, 氧化应激, PET成像, 活性氧(ROS), [18F]ROStrace