Clear Sky Science · zh
对患者样本的全局RNA表达分析发现可用于腹膜、卵巢和深部子宫内膜异位症的潜在诊断生物标志物
为何这种疾病关系到日常生活
子宫内膜异位症估计影响全球约1.9亿女性,常引起严重的盆腔疼痛、疲劳和生育问题。然而许多人在得到明确诊断前往往要等待近十年,诊断通常只能通过手术确诊。本研究提出了一个简单但重要的问题:我们是否可以改用读取身体的分子“指纹”来更早检测子宫内膜异位症,甚至区分其不同类型,未来通过一种简便检测实现?
同一疾病的不同面貌
当类似子宫内膜的组织出现在不应存在的部位时,就会发生子宫内膜异位症,例如在卵巢、腹膜(腹腔薄膜)或盆腔器官深处生长。这些部位定义了三种主要亚型:卵巢型、腹膜型和深部型。每种亚型可引起不同的疼痛模式、生育问题和器官损伤。目前,医生依赖症状、影像学检查,并且常常通过腹腔镜——一种在麻醉下的手术——来确诊并判断是哪种亚型。若能以无创方式区分这些类型,将可让许多女性免受多年不确定和手术之苦。
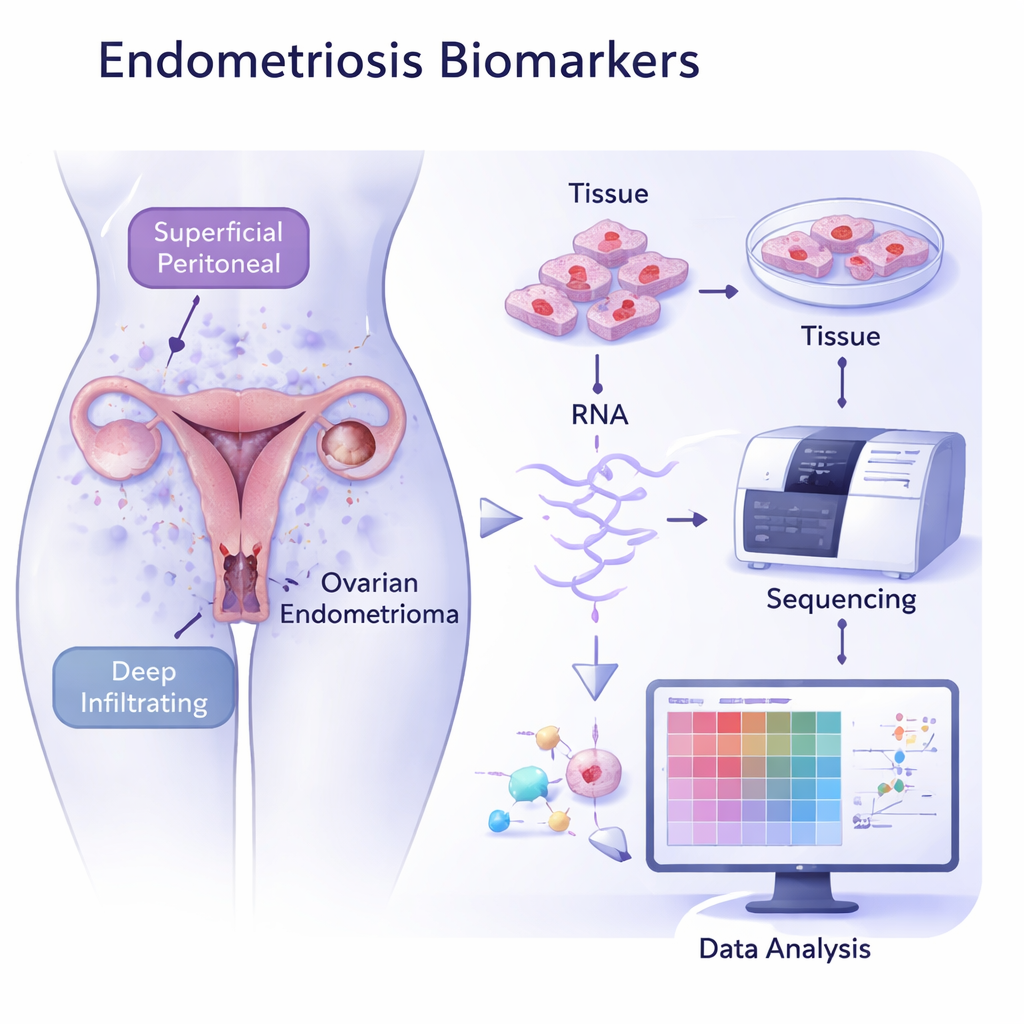
读取病变组织的RNA“条码”
研究者收集了来自26名子宫内膜异位症患者(涵盖所有三种亚型)以及15名无该病的女性的组织样本。随后他们使用RNA测序,这种方法可测量哪些基因被开启或关闭,从而构建这些组织内部活动的全景图。将病变组织与健康子宫内膜比较时,样本出现明显分群,显示出不同的基因活动模式。卵巢病灶形成了一个紧密的群体,而腹膜和深部病灶则归为另一组,这支持了即使具有某些共同特征,这些亚型也沿着不同生物学路径发展的观点。
共同的瘢痕形成与炎症通路
在三种亚型中,研究团队都发现了与构建和重塑组织支架(细胞外基质)相关基因的活性升高、典型瘢痕的细胞收缩性增强以及强烈的炎症信号。这些变化与临床所见相吻合:僵硬、纤维化的病灶会引起疼痛和粘连。研究还检测到病灶内改变的免疫景观。所谓的M2巨噬细胞——一种与伤口愈合和纤维化相关的免疫细胞——尤其丰富,而负责清除异常细胞的自然杀伤(NK)细胞显著减少。这种失衡可能有助于异位组织在不适当位置存活和扩散。
亚型特异的分子线索
除了这些共同模式外,每种亚型都有其独特的分子特征。在深部和腹膜型子宫内膜异位症中,与磷酸二酯酶信号相关的基因——这些通路已与其他纤维化疾病相关联——明显上调。在卵巢型中,与免疫呈递和激素产生相关的基因突出,提示卵巢提供了不同的生化环境。研究者还探讨了非编码RNA,这些分子虽不编码蛋白但能调控基因活性。他们鉴定出若干在总体上或特定亚型中显著增加的非编码RNA,提示了新的调控因子和可能可在血液或其他体液中检测到的生物标志物候选。
有前景的蛋白质标志物用于未来检测
从大量改变的基因中,研究团队聚焦于那些产生分泌蛋白的基因——这类蛋白是未来血液检测的理想候选。他们选择了三种蛋白进行进一步研究:PLA2G2A、ANGPTL7 和 PLA2G5。使用ELISA(一种测量蛋白水平的实验室方法),他们发现PLA2G2A在三种子宫内膜异位症类型中均升高,尤以卵巢病灶为甚。ANGPTL7主要在深部和腹膜病灶中升高,而PLA2G5仅在深部子宫内膜异位症中升高。合在一起,这些蛋白构成了一个潜在的检测组合,不仅可指示子宫内膜异位症的存在,还可提示病灶的可能位置。
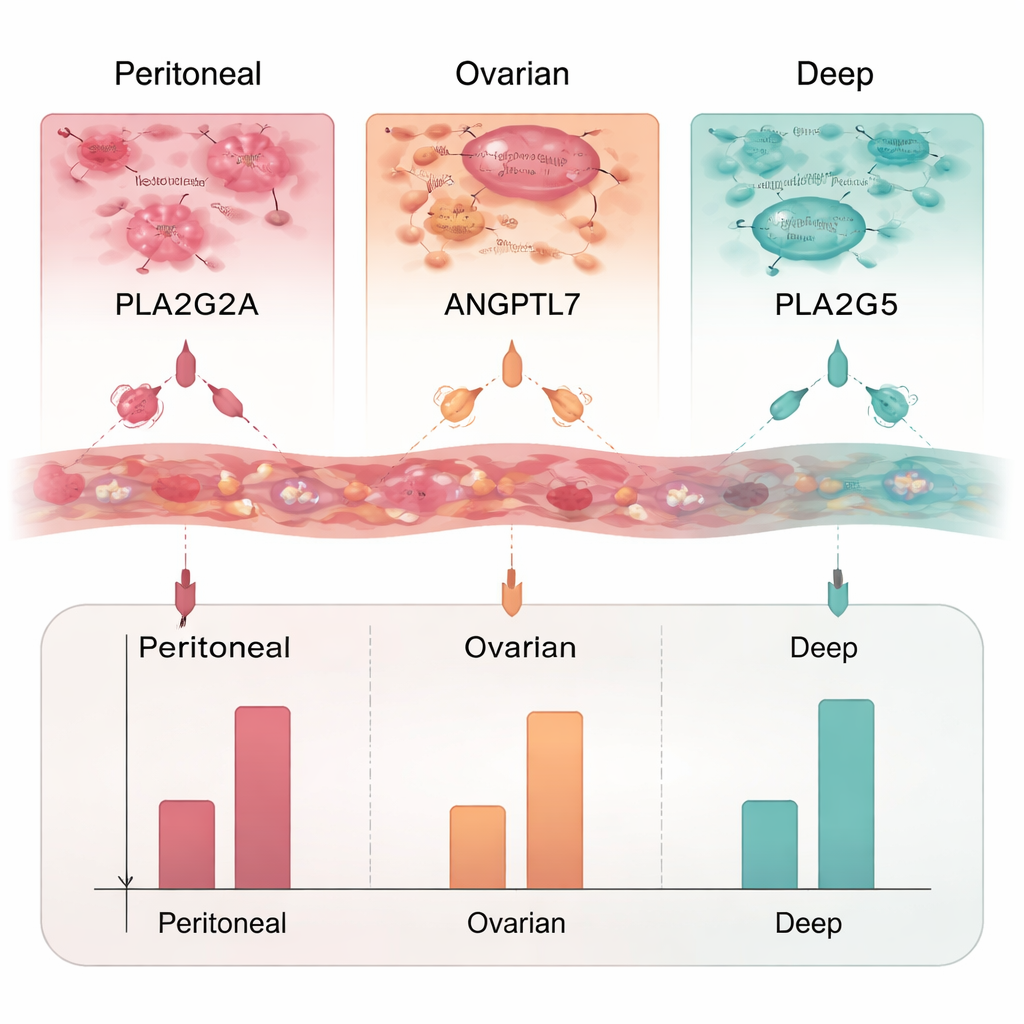
这对患者意味着什么
这项研究尚未带来现成的血液检测,但奠定了重要基础。通过绘制成千上万基因和免疫细胞在不同子宫内膜异位症亚型中的行为模式,研究确定了可被非侵入性测量的特定蛋白——PLA2G2A、ANGPTL7 和 PLA2G5。如果在更大、独立的患者群体中得到验证,这类标志物的组合可能缩短漫长的诊断过程,减少仅为确诊而进行的手术,并且能根据女性所患的具体亚型实现更有针对性的治疗。
引用: Lisá, Z., Fanta, M., Kokavec, J. et al. Global RNA expression analysis of patient samples identified potential diagnostic biomarkers specific for peritoneal, ovarian and deep endometriosis. Sci Rep 16, 5070 (2026). https://doi.org/10.1038/s41598-026-35467-9
关键词: 子宫内膜异位症, 生物标志物, RNA测序, 免疫细胞, 女性健康