Clear Sky Science · zh
在裂殖酵母中通过发光互补检测蛋白质–蛋白质相互作用的全球筛查系统的开发
照亮蛋白质隐秘的生命
我们的每一次心跳、思考和呼吸都依赖于细胞内蛋白质的协作。这些微小的伙伴关系——称为蛋白质–蛋白质相互作用——控制着从基因表达到细胞应对压力的方方面面。然而,许多此类相互作用短暂或脆弱,现有工具难以探测到。本文介绍了一种在简单模式生物裂殖酵母中构建的全新高灵敏度“光学”筛查系统,可一次性揭示成千上万条隐藏的蛋白质连接。
为何蛋白质的伙伴关系难以察觉
蛋白质很少单独工作。它们会在不同时刻与不同的伙伴结合,有时仅维持片刻,其行为还会被化学修饰或在细胞内的位置所影响。传统研究这些相互作用的方法,要么将蛋白质从其天然环境中抽离,要么依赖某些遗传学技巧,这些方法无法捕获所有配对。因此,现有的细胞相互作用图谱不完整。作者旨在通过创建一个更灵活、更灵敏的系统来改进这一图谱,使之能在活细胞中几乎遍历裂殖酵母的每种蛋白质。
把接触变成光
该方法的核心是一个可发光的分裂酶。一部分称为LgBiT,连接到研究者想要研究的“诱饵”蛋白;另一部分SmBiT,分别连接到多个可能的“猎物”伙伴,每个酵母菌株携带一种猎物。单独时,这两段酶很少相互结合。但当诱饵和猎物在细胞内结合时,两段酶会复合,重组为能在化学底物存在下发光的完整酶。通过测量每种酵母菌株产生的光强,团队便能判断哪些蛋白在细胞内真实相遇以及它们相互作用的强度。为了避免标签阻碍蛋白正常功能而遗漏伙伴,诱饵蛋白被制成两种版本,LgBiT分别连接在蛋白的任一末端,大大提高至少有一种构型可行的几率。 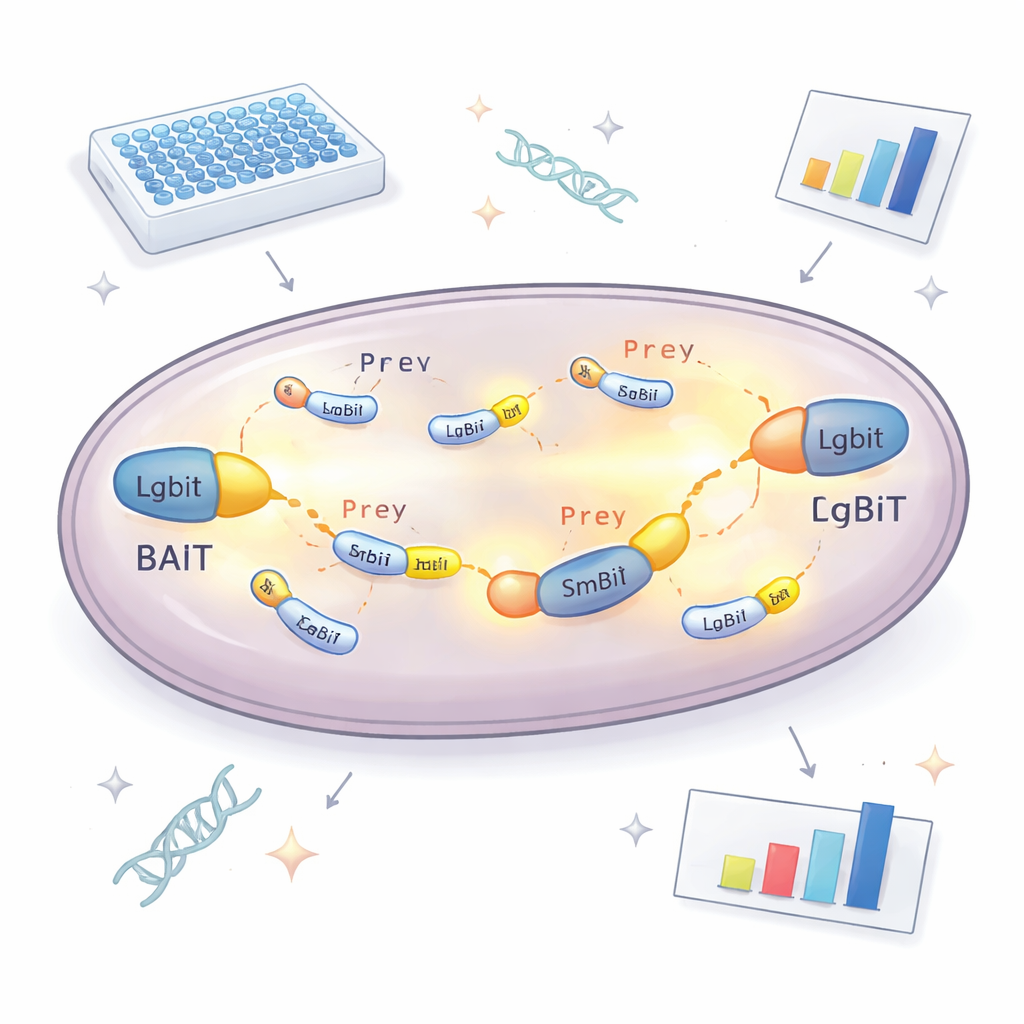
构建酵母文库与菌株系统
构建该平台不仅需要巧妙的酶设计。研究者还必须以可控的单拷贝方式将数千个猎物蛋白引入酵母。他们设计了一种特殊的猎物DNA载体,可插入酵母基因组的特定位点,并携带红色荧光标记。红色信号的亮度反映了插入拷贝数,便于团队轻松挑选出恰好单拷贝的菌落,这对可靠比较至关重要。他们还创建了专门的诱饵载体,将LgBiT置于诱饵蛋白的前端或末端,并使用柔性连接肽分隔,以便蛋白仍能折叠并正常运动。随后精心设计的酵母菌株被构建为同时携带两个诱饵构建体和一个猎物构建体,利用营养标记确保只有正确组合的细胞能够存活。
将系统付诸检验
为了检验其设计是否真正提高了检测能力,科学家们首先检查了具有已知伙伴的蛋白。他们证实信号强度在很大程度上取决于发光标签的连接位置:某些相互作用仅在LgBiT位于诱饵的一端时才出现,而在另一端则看不到。两种版本同时表达可以提升光信号,证明双诱饵策略使得弱相互作用或对构型敏感的相互作用更容易被捕获。该系统还检测到涉及膜结合蛋白的接触——这类蛋白对传统酵母双杂交方法向来极为棘手。基于这些验证,团队将规模扩大到全基因组筛查,选取一个与转录相关的蛋白Tfs1作为诱饵。在筛查超过4,600个猎物蛋白时,他们找到了31个强候选者,包含若干已知伙伴和许多新发现,其中一些位于细胞核外的区域,如线粒体和细胞表面。 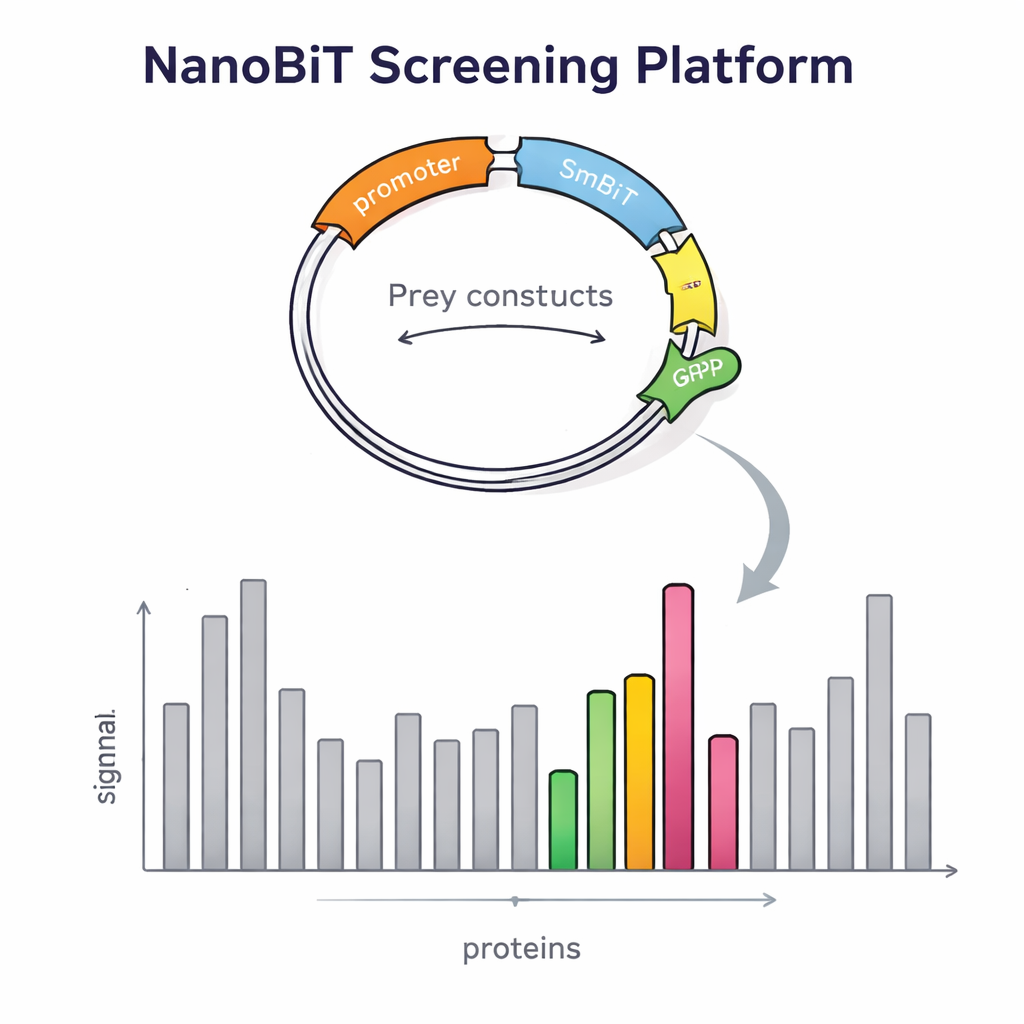
这对生物学与药物发现意味着什么
对于非专业读者,核心信息是作者在酵母细胞内构建了一个更灵敏的“相互作用雷达”。通过将短暂的蛋白握手转换为可测量的光闪,并巧妙安排遗传学使三种带标签的蛋白能同时表达,他们的系统既揭示了已知的也揭示了以前看不见的蛋白伙伴。尽管还需要用其它技术对每一项新配对进行进一步验证,这一平台弥补了我们细胞网络图谱中的重要空白。由于这些菌株也被设计为对小分子更敏感,同一套系统可调整用于筛选能够破坏有害蛋白伙伴关系或稳定有益伙伴关系的药物,为基础生物学研究和早期药物发现提供了一个强大的新工具。
引用: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
关键词: 蛋白质相互作用, 裂殖酵母, 发光检测, 高通量筛查, 药物发现工具