Clear Sky Science · zh
顺序使用铂类药物与PARP抑制剂可增强PD1免疫治疗在小鼠Brca2突变胰腺癌中的疗效
这项研究对患者有何重要意义
胰腺癌是最致命的癌症之一,即便医生知道肿瘤存在可利用的弱点——例如BRCA2基因突变——现有治疗通常也难以长期控制疾病。该研究使用更为现实的小鼠模型来回答一个许多患者与肿瘤科医生面临的实用问题:在强效化疗和PARP抑制剂之后,加入现代免疫治疗能否显著延长生存期,且肿瘤为何常常复发?
带有遗传弱点的难治癌症
胰腺导管腺癌极难治疗,五年生存率仍然只有个位数。少数患者携带遗传或肿瘤特异性的BRCA2缺陷,该基因参与断裂DNA的修复。这类肿瘤对损伤DNA的药物(如铂类化疗)以及进一步削弱癌细胞DNA修复能力的PARP抑制剂特别敏感。当前晚期BRCA突变胰腺癌的标准治疗是数月的铂类化疗,随后以PARP抑制剂维持治疗。然而在关键的POLO临床试验中,这一策略并未延长总生存期,凸显了理解耐药机制并设计更好维持方案的必要性。
构建更逼真的小鼠模型
许多现有实验模型去除了包围真实患者肿瘤的免疫与基质成分。为了解决这一问题,作者构建了在完全功能性免疫系统背景下形成BRCA2缺失胰腺肿瘤的小鼠。从这些自发性肿瘤中分离出可植入到基因匹配小鼠体内的克隆细胞系。这些Brca2突变肿瘤在形态与行为上非常像人类胰腺癌:纤维化严重,T细胞被大量排斥,并显示高度自发性DNA损伤。关键是,这些肿瘤对常用的铂类联合方案(吉西他滨加顺铂)高度敏感,而单独使用PARP抑制剂在动物体内仅表现出温和且短暂的疗效,尽管对同一细胞系的体外活性很强。 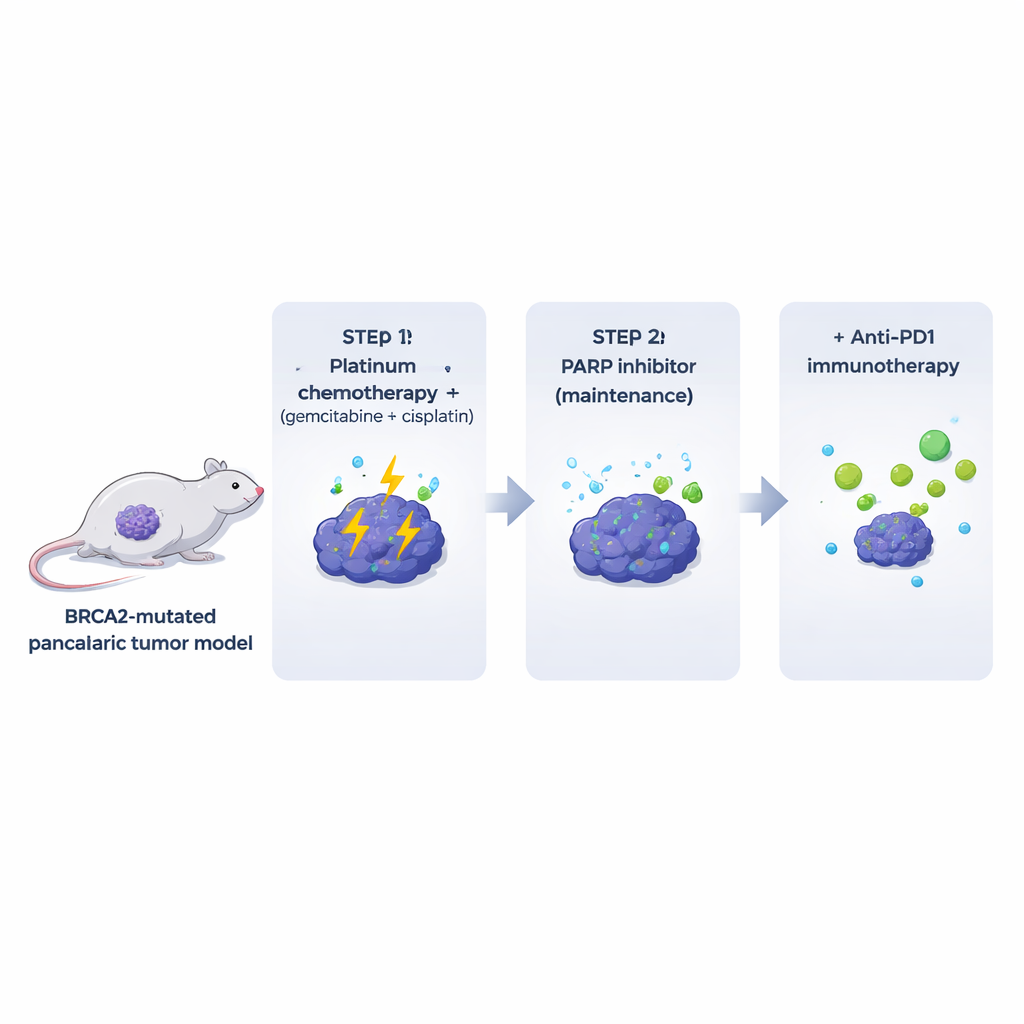
化疗重塑肿瘤微环境
团队接着探查铂类化疗后肿瘤内部发生了什么。治疗十天后,肿瘤虽然缩小但未被清除。基因表达分析显示向免疫相关活动的显著转变:与T细胞激活和适应性免疫有关的通路被激活。被治疗的肿瘤中发现更多T细胞,且许多T细胞带有衰竭标志——表明它们已被激活但功能正在丧失。在患者中,携带BRCA或相关PALB2突变的胰腺癌在术前接受铂类化疗后,也观察到类似的T细胞浸润增加。同时,肿瘤细胞提高了PD-L1的表达,PD-L1是一种能通过结合PD-1受体关闭T细胞的表面蛋白,提示肿瘤在对抗这一新出现的免疫压力。
为何单用PARP不足——以及耐药从何而来
模拟临床治疗,研究者先给予小鼠吉西他滨和顺铂的初疗程,随后以PARP抑制剂奥拉帕利作为维持治疗。这一序列相比单独化疗改进了肿瘤控制和生存,证实既往化疗能使肿瘤对PARP抑制更敏感。然而,没有小鼠被治愈:在PARP维持下肿瘤最终仍出现再生。耐药肿瘤呈现更分化的外观,且发育调控因子CDX2表达显著升高。这提示在该模型中,耐药不只是通过修复原始DNA修复缺陷而产生,而可能伴随肿瘤细胞身份的转变。CDX2或可作为患者中耐药出现的潜在生物标志物。
用正确的序列解锁免疫治疗
免疫检查点药物如抗PD1抗体已经改变了若干癌种的治疗,但胰腺癌总体上仍然不敏感。与此一致,抗PD1(无论是否联合另一种检查点药物抗CTLA4)在初治的BRCA2突变肿瘤中均未见获益,且仅简单地把抗PD1加入PARP抑制也效果有限。情形在采用完整序列时发生变化:先进行铂类化疗,然后在维持阶段同时使用PARP抑制剂和抗PD1。在这种情况下,肿瘤缩小更明显,小鼠的生存优于仅化疗加PARP抑制或单独抗PD1。将抗CTLA4加入PARP维持并未产生类似益处,提示化疗所诱导的肿瘤微环境特别有利于对PD-1阻断产生反应。 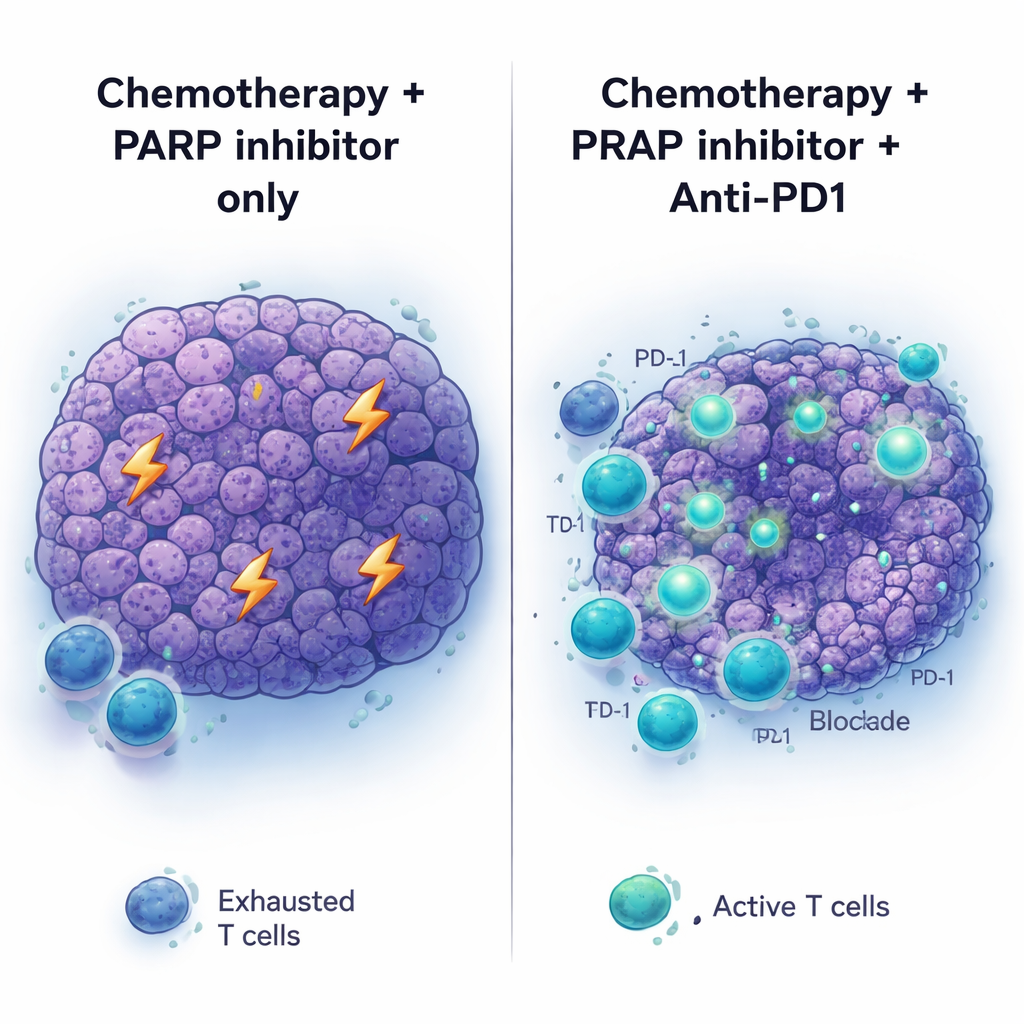
这对未来治疗可能意味着什么
综上所述,该研究表明对于BRCA突变的胰腺癌,疗法的顺序与组合极为重要。强烈的损伤DNA化疗不仅直接攻击肿瘤细胞,还能激发免疫反应,即便该反应最初被衰竭和PD-L1防御所抑制。PARP抑制剂可延长这种益处,但单独使用难以根治,且可能推动肿瘤朝向CDX2高表达的耐药状态。通过在铂类化疗之后,于PARP维持期叠加抗PD1免疫治疗,或可将这一短暂被激活但衰竭的免疫状态转化为更有效且持久的抗肿瘤反应。正在进行的将PARP抑制剂与免疫治疗联合用于BRCA相关胰腺癌的临床试验,将是检验这一精心时序策略能否转化为更长和更好患者生命的关键途径。
引用: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
关键词: 胰腺癌, BRCA2突变, 铂类化疗, PARP抑制剂, PD-1免疫治疗