Clear Sky Science · zh
槲皮素通过抑制活性氧生成、p38 MAPK 磷酸化和 NF-κB 激活减轻高糖诱导的 ARPE-19 细胞 VEGFA 表达
一种常见植物色素为何与视力相关
糖尿病性眼病是导致视力丧失的主要原因之一,但大多数治疗仅针对问题的一部分:视网膜中形成的脆弱、易渗漏的血管。本研究考察了槲皮素——一种存在于苹果、洋葱、浆果和茶中的天然化合物——是否能够在损伤变得严重之前平抑眼后部受压的细胞。通过研究槲皮素在暴露于高糖环境的视网膜细胞中的作用,研究者提出了一个简单但意义重大的问题:饮食中已有的某种物质是否能帮助保护糖尿病患者的视力?
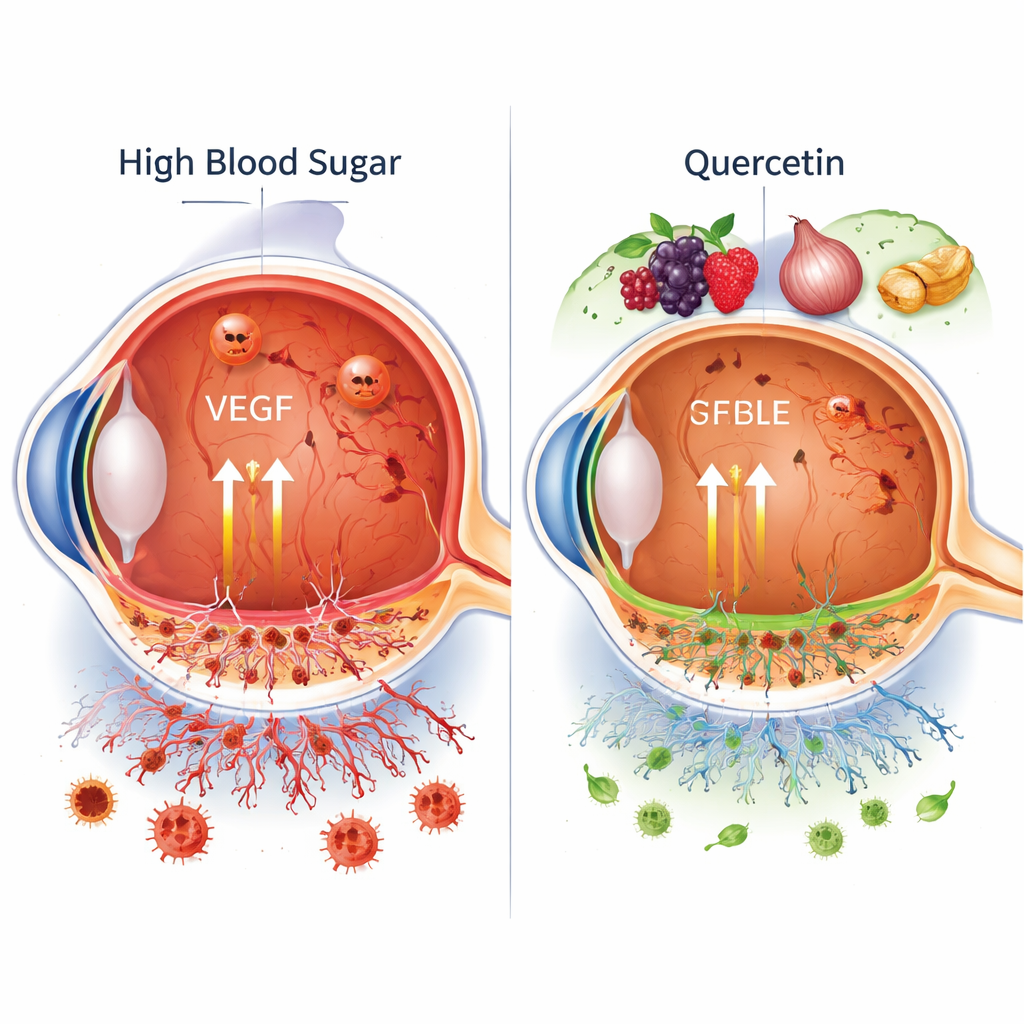
高血糖如何损害眼后部
在糖尿病中,多年高血糖逐步损伤为感光组织提供营养的细小血管。一个关键的祸首是称为 VEGF 的信号分子,它促使新血管生长并使现有血管更易渗漏。在视网膜中,这可能导致肿胀、出血,最终引发中心视力丧失。视网膜色素上皮层像花园下面的肥沃土壤一样支持视网膜,该层细胞在高糖刺激下会释放更多 VEGF。高糖还会增加不稳定的反应性分子(即氧化应激),并在这些细胞内开启炎性开关,进一步提高 VEGF 产生并加重糖尿病视网膜病变。
测试槲皮素的安全性及对有害信号的影响
研究者首先检查了槲皮素本身对体外培养的视网膜色素上皮细胞是否有害。在适度剂量下,细胞数日内保持健康,但非常高的剂量开始降低细胞存活率。随后他们选择了两个无毒浓度,将细胞暴露于高糖环境,有无槲皮素两组对照。在单独高糖条件下,VEGF 在基因和蛋白水平上均显著上升。当加入槲皮素时,VEGF 的这种激增被明显抑制,与作为比较的已知抗氧化药物效果相近。这意味着槲皮素能够降低导致视网膜血管渗漏的主要驱动因素之一,而不会杀死产生该因子的细胞。
平息氧化和炎性级联反应
为了解槲皮素如何实现这一点,团队测量了细胞内的氧化应激及特定信号通路。高糖增加了活性氧物质,这是氧化损伤的标志。槲皮素显著减少了这些有害分子,表现与抗氧化对照一致。研究者还追踪了两条响应应激的分子通路:一条涉及名为 p38 的蛋白,另一条由 NF-κB 复合体控制,后者是炎症的主要开关。高糖强烈激活了 p38 并促使 NF-κB 进入细胞核,在那里它会开启像 VEGF 这样的基因。槲皮素选择性抑制了 p38 的活性,并通过维持其抑制子 IκBα 来阻止 NF-κB 完全进入细胞核,有效地降低了炎性基因程序的活性,而相关通路 ERK 大体保持不受影响。
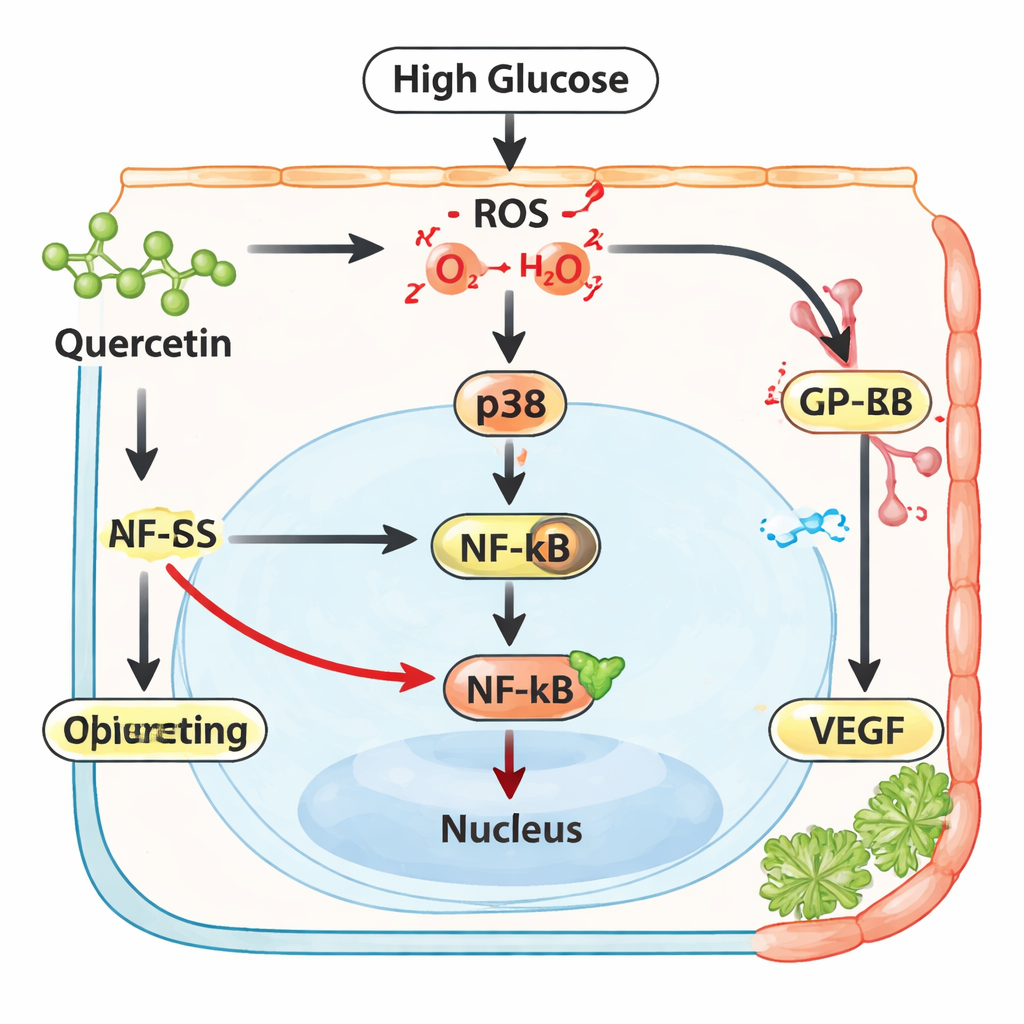
从细胞信号到血管渗漏再到回归
研究还通过使用小鼠原代视网膜色素细胞和一种间接的血管渗漏测试,将研究推进到更接近真实组织的层面。在小鼠细胞中,高糖再次促使 VEGF 升高,槲皮素使其回落至接近正常水平。随后团队收集了在人类视网膜色素细胞高糖培养下的“培养基”,并将其倒在一层人类血管内皮细胞上。穿过这层血管细胞的液体渗漏增加,模仿了糖尿病眼中视网膜屏障的破坏。当色素上皮细胞在处理过槲皮素或抗氧化剂后,所诱发的渗漏显著下降,表明改变色素细胞分泌物——尤其是 VEGF——可以帮助维持血管的完整性。
这对糖尿病患者可能意味着什么
综合来看,这项工作支持了一个简单但有力的观点:槲皮素既具抗氧化又具抗炎特性,能够打断高血糖促使视网膜细胞过度产生 VEGF 并削弱血管的连锁反应。这并不意味着食用富含槲皮素的食物或服用补充剂可以替代当前直接阻断 VEGF 的眼内注射;膳食中可获得的剂量与实验室中的用量不同,且该化合物不易被吸收或递送到眼部。但这些发现暗示槲皮素或经改良的制剂,未来可能作为一种辅助疗法,帮助降低糖尿病眼部的基础应激和炎症,减轻治疗负担并放缓导致视力丧失的进程。
引用: Liu, PK., Chi, YC., Chang, YC. et al. Quercetin attenuates high glucose-induced VEGFA expression in ARPE-19 cells by inhibiting ROS generation, p38 MAPK phosphorylation, and NF-κB activation. Sci Rep 16, 4987 (2026). https://doi.org/10.1038/s41598-026-35409-5
关键词: 糖尿病视网膜病变, 槲皮素, 氧化应激, VEGF, 视网膜色素上皮