Clear Sky Science · zh
靶向 NLRP3 炎症小体通过增强自噬缓解慢性疼痛与抑郁共病
为什么疼痛和情绪常常相伴而来
许多长期承受神经性疼痛的人同时也在与抑郁作斗争。这种双重负担可能将患者困在恶性循环中:疼痛使情绪恶化,低落的情绪又放大疼痛感,两者同时治疗十分困难。本文背后的研究提出了一个令人期待的问题:如果科学家们瞄准大脑中的一个关键炎症开关,能否同时缓解慢性疼痛和抑郁,而非分别治疗?
位于疼痛与情绪交汇处的大脑区域
研究者把注意力集中在前扣带皮质(ACC),这是大脑深处的一个区域,参与塑造我们对疼痛的感受、决策以及情绪处理。慢性疼痛或抑郁患者的大脑成像常显示该区域的变化。在小鼠中,损伤信号从体内沿脊髓向上传递,并经其他大脑枢纽到达 ACC,影响疼痛的不适感及其在精神生活中的主导程度。由于 ACC 也参与情绪控制,它成为解释为什么慢性疼痛与抑郁常常共存的自然候选部位。
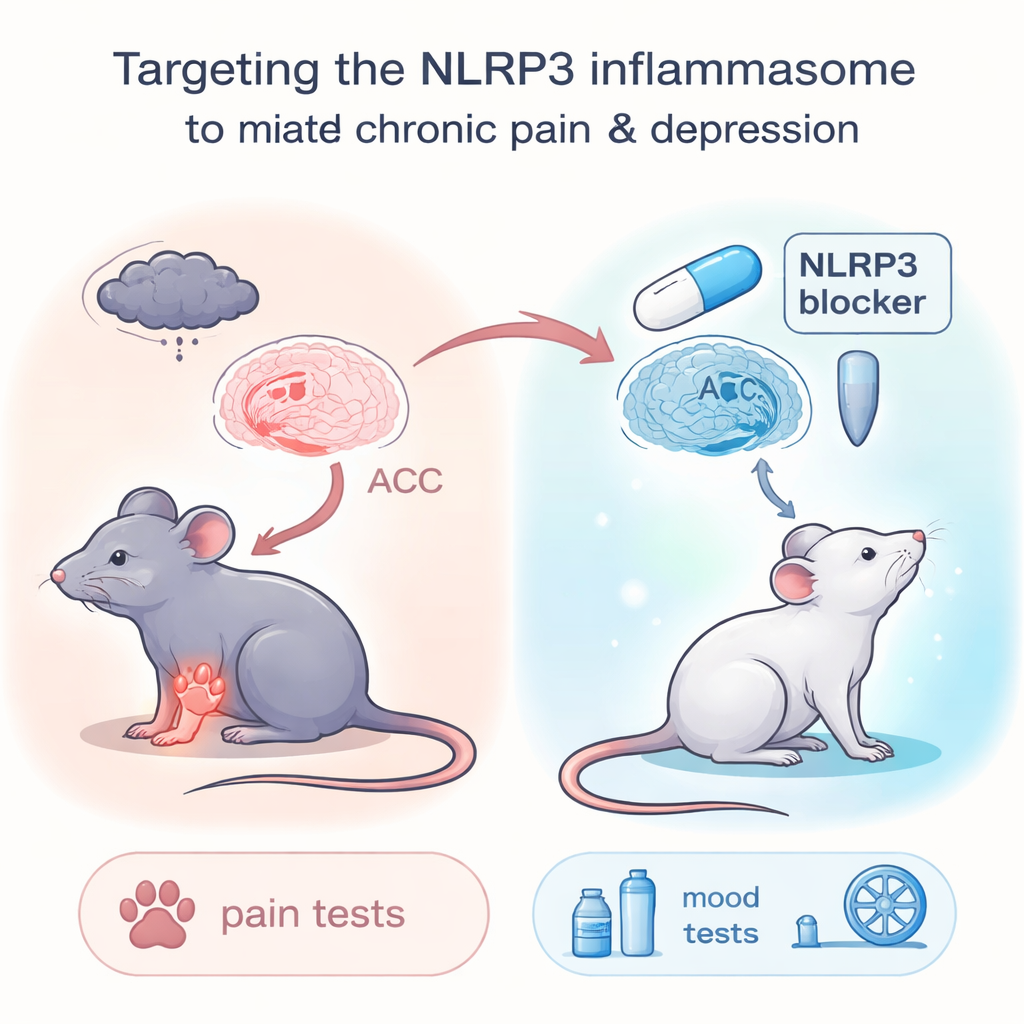
调低一种炎症报警器
本研究的核心是一个称为 NLRP3 炎症小体的蛋白“机器”,它像内部的火警报警器,感知危险和损伤。一旦被激活,它就会触发炎性物质的释放,扰乱脑细胞并改变行为。研究团队使用了一种成熟的小鼠模型称为“保留神经损伤”(spared nerve injury),以模拟源于神经损伤的神经性疼痛。术后六周,这些小鼠表现出明显的痛苦迹象:对触碰与热刺激迅速收回爪子、活动减少、在应激测试中更早放弃、对加糖水失去兴趣——这些都是疼痛和类抑郁行为的标志。
一种药物和一种基因策略检验新治疗思路
为验证 NLRP3 是否驱动这些问题,科学家采用了两种策略。一种是将名为 MCC950 的化合物直接注入脑脊液腔,让它能到达包括 ACC 在内的多个脑区。MCC950 已知能特异性阻断 NLRP3。第二种方法是使用基因工程小鼠,使其缺失 Nlrp3 基因。无论哪种方式,阻断 NLRP3 都带来了显著变化:接受处理或基因编辑的小鼠对触觉和热刺激的敏感性下降、活动更自如、在焦虑动物通常回避的开放空间停留时间更长,并在简单的记忆测试中表现更好。重要的是,所用剂量的药物并未显示对动物肝脏或肾脏造成明显损害。
清理细胞内部的“垃圾”
研究还探讨了一种细胞清洁机制——自噬,细胞通过它回收老旧成分并清除可能有害的物质。在表现出疼痛与抑郁样行为的小鼠中,ACC 的脑细胞呈现出应激和炎症迹象,同时自噬标志物降低。当用 MCC950 阻断 NLRP3 或通过基因编辑去除它时,炎症迹象下降,神经元状况更健康,自噬标志物上升。在培养皿中生长的支持性脑细胞(辅佐细胞)中也观察到类似效应:药物处理或基因缺失在刺激后均增强了回收清理机制并减少炎性信号。
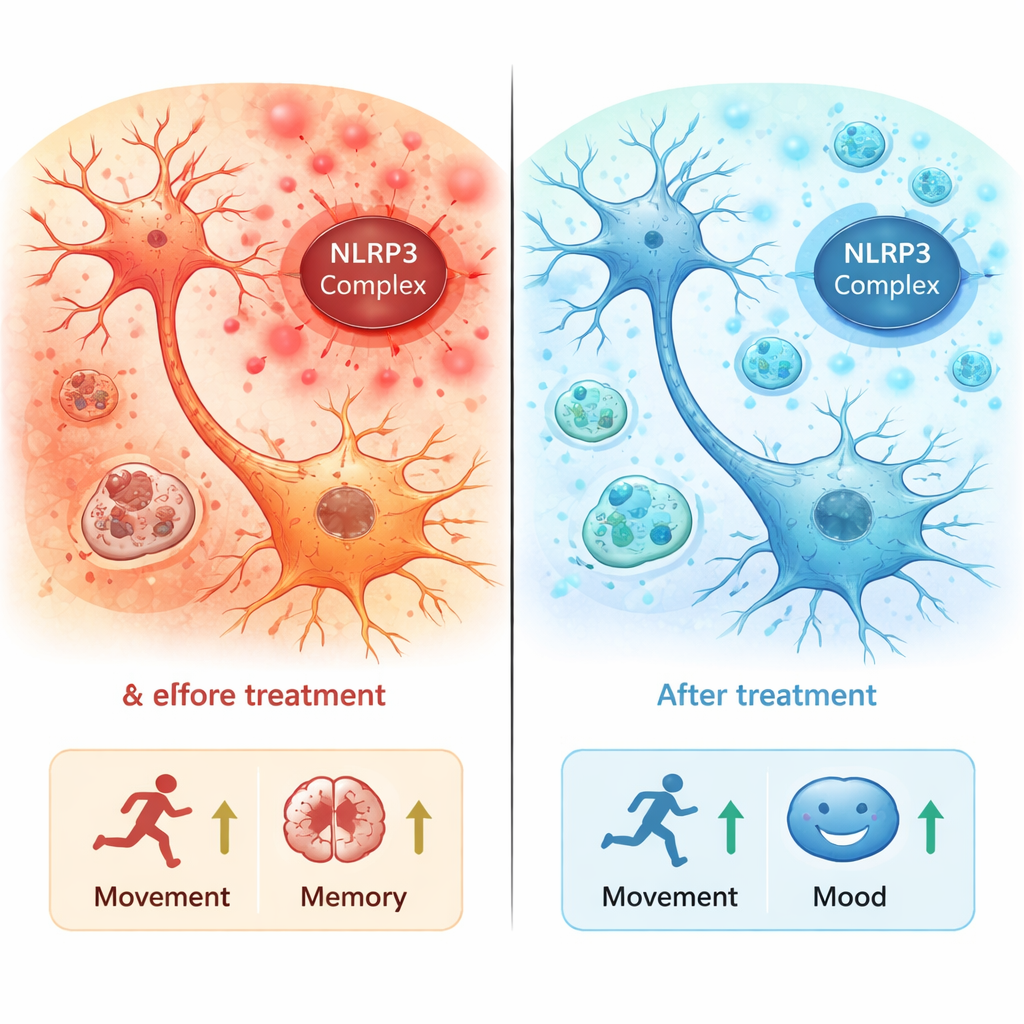
这对疼痛患者意味着什么
综合来看,这些发现表明当神经损伤在 ACC 激活 NLRP3 炎症小体时,炎症上升、细胞内部清洁受阻,这一组合有助于推动慢性疼痛和类抑郁行为的出现。在小鼠中,阻断 NLRP3 可恢复自噬、平抑炎症并缓解两类症状。尽管 MCC950 本身仍需谨慎的安全性测试,且该研究处于临床前阶段,但这项工作强调了 NLRP3 及细胞回收系统作为未来可能同时应对疼痛与抑郁的有希望治疗靶点。
引用: Zhang, P., Liu, H., Zhou, J. et al. Targeting the NLRP3 inflammasome alleviates the comorbidity of chronic pain and depression via enhancing the autophagy. Sci Rep 16, 4932 (2026). https://doi.org/10.1038/s41598-026-35400-0
关键词: 慢性疼痛, 抑郁, 脑炎症, 自噬, NLRP3