Clear Sky Science · zh
通过与ATP13A2表达抑制相关的线粒体功能障碍扰乱细胞内铁稳态
为何细胞内的铁很重要
帕金森病最为人熟知的是震颤和运动僵硬,但在受影响的脑细胞内部还有另一场戏在上演:铁,这种必需金属,开始在不该积聚的地方堆积起来。本研究提出了一个简单但重要的问题:这种铁的积聚如何发生,它会如何损害神经细胞内的微小“发电厂”和“回收站”?通过回答这个问题,工作为解释为何帕金森及相关疾病中特定脑区发生退化提供了线索,并指向超越多巴胺替代的新型治疗方向。
关注一种罕见的遗传线索
研究人员聚焦于一种罕见的遗传性帕金森病,称为PARK9,由ATP13A2基因缺陷引起。该基因编码一种位于溶酶体——细胞的垃圾处理和回收室——内的蛋白。携带ATP13A2突变的人也可能出现脑内铁沉积的症状。这个关联使ATP13A2成为研究铁平衡如何失常的理想切入点。研究团队使用一种过表达帕金森相关蛋白α‑突触核蛋白的人类类神经元细胞系,利用小RNA片段下调ATP13A2,随后追踪铁、能量产生和细胞健康的变化。
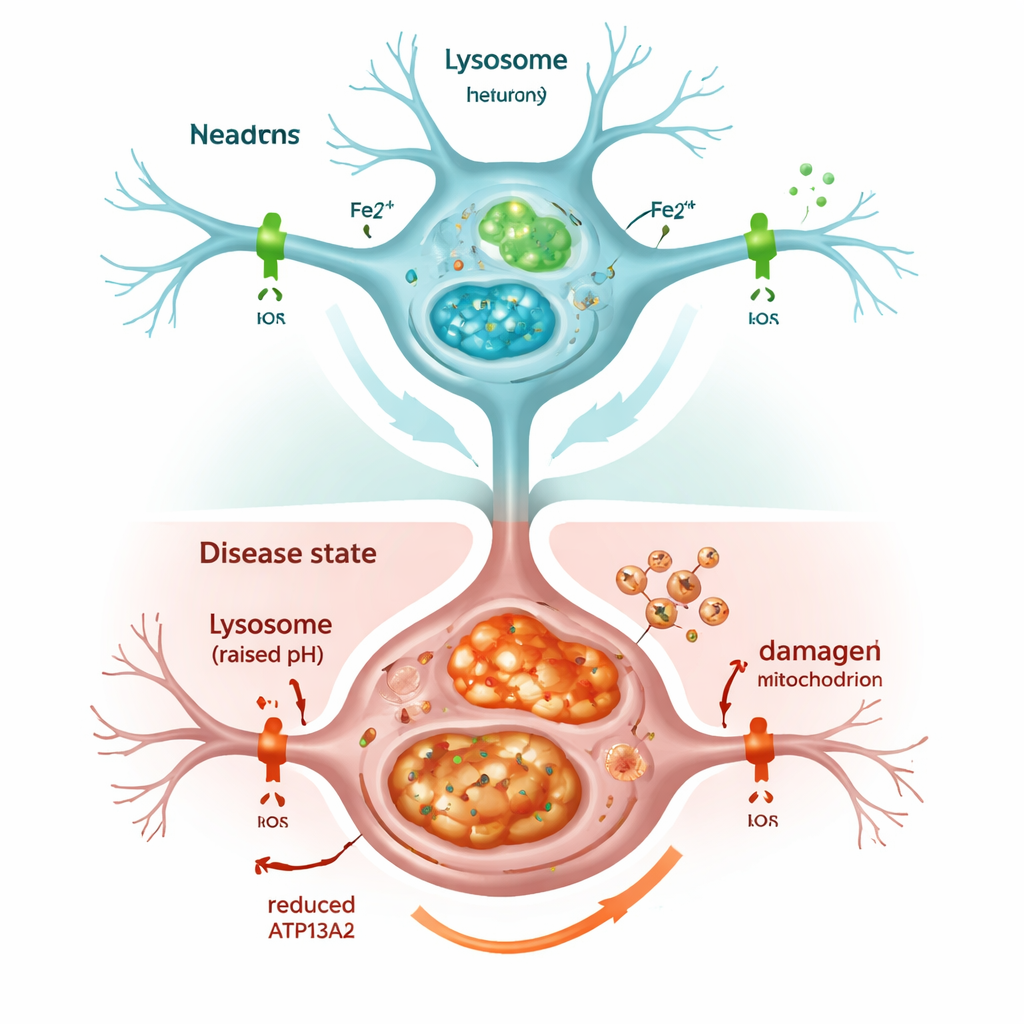
当细胞的回收系统停滞
关闭ATP13A2很快削弱了溶酶体功能。它们的内部酸性——对分解不需要的物质至关重要——下降,细胞的清理过程(被称为自噬)的标志物反而积累而未被清除。结果,α‑突触核蛋白堆积,与帕金森病大脑中观察到的情况相呼应。细胞总体铁含量增加,尤其是化学活性更强的二价铁(Fe2+)在溶酶体和线粒体中均增多。细胞通过合成更多的铁储存蛋白铁蛋白来应对,但这不足以阻止问题:过载的线粒体产生过量反应性氧物质,细胞存活率下降。用一种与临床上使用的相似的铁结合药物处理细胞,减少了氧化应激并部分挽救了细胞活力,强调了过量铁本身是损伤的关键驱动因素。
铁感知器不再“听见”金属信号
通常,细胞有一套反馈系统来察觉铁水平上升,并通过降低铁的输入来回应。一种叫IRP2的蛋白通过线粒体提供的血红素依赖性信号部分感知铁,然后调节细胞表面携铁蛋白的生成。在缺乏ATP13A2的细胞中,这一防护机制失效。即便铁已升高,负责将铁带入细胞的转运蛋白仍维持在高水平。IRP2蛋白量几乎没有变化,向外补充额外铁也未触发其正常的降解。研究团队将这一故障追溯到线粒体:受损的线粒体呼吸效率降低,表现出错误质量控制(线粒体自噬)迹象,并且关键是失去了合成血红素的能力——血红素是帮助IRP2感知铁的含铁分子。血红素不足时,IRP2无法接收到“铁过多”的信号,从而允许持续的铁流入。
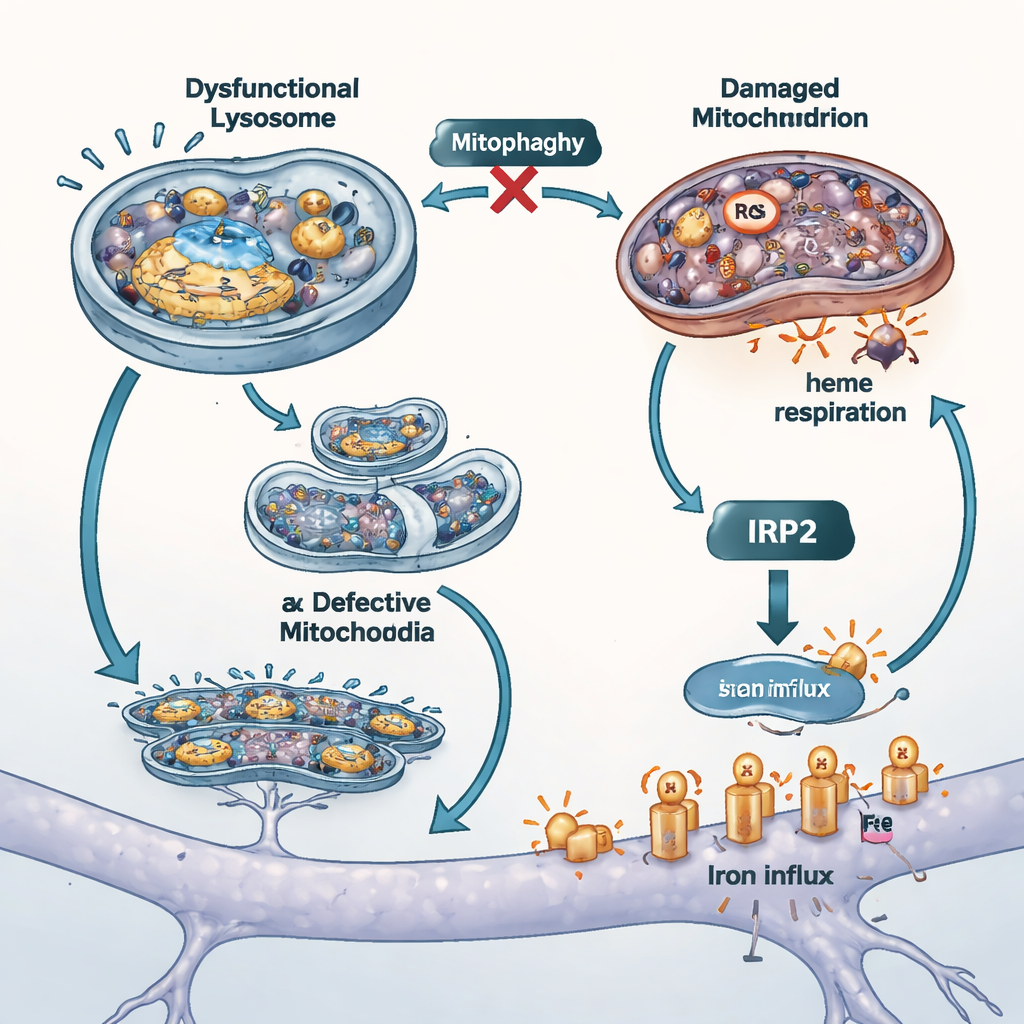
堵住铁的水龙头并在其他模型中验证
为探测这种失控铁进入在细胞损伤中所占的比例,科学家阻断了两条主要的铁摄取路径。他们使用不含铁的转铁蛋白来与其中一类转运体竞争,并用一种小药物抑制另一种名为DMT1的转运蛋白的活性。两种操作都降低了细胞内的总铁和游离铁,减少了线粒体氧化应激,并改善了存活率,表明细胞表面的铁通道在ATP13A2丧失时是放大损伤的重要因素。研究人员还在缺失另一帕金森相关基因PINK1的细胞中重复了关键实验,PINK1已知会损害线粒体自噬。这些细胞显示出相同的铁积聚和血红素合成减弱的组合,支持了这样一个观点:线粒体质量控制与铁平衡在疾病的不同形式中紧密相连。
这对帕金森病和未来治疗意味着什么
简言之,该研究描述了一个恶性循环。当ATP13A2被抑制时,溶酶体无法清除受损组分,包括故障的线粒体。这些被削弱的线粒体随后产生更少的能量和更少的血红素,削弱了细胞的铁感知系统。铁继续通过表面转运蛋白涌入,聚集在脆弱的细胞区室中,并促进进一步损伤线粒体的有毒反应。随着时间推移,这一循环可能有助于解释为何某些神经元在帕金森病及相关的脑内铁沉积疾病中发生死亡。研究结果提示,未来的治疗不仅可能试图移除过量铁,还应恢复正常的溶酶体功能、线粒体质量控制和血红素生成——从根源上解决问题,而不仅仅是事后清理金属。
引用: Murakami, T., Ohuchi, K., Kiuchi, M. et al. Disruption of intracellular iron homeostasis through mitochondrial dysfunction associated with suppression of ATP 13A2 expression. Sci Rep 16, 5007 (2026). https://doi.org/10.1038/s41598-026-35368-x
关键词: 帕金森病, 脑铁, 线粒体, 溶酶体, 血红素合成