Clear Sky Science · zh
SPHK1在免疫-代谢交界处的新兴角色:泛癌整合分析
这个隐藏的癌症开关为何重要
癌症不再被简单视为一团失控增殖的细胞。肿瘤还会重塑能量利用方式并改变对免疫系统的隐匿策略。本研究聚焦于单一酶——SPHK1,证据显示它恰好位于这两类过程的交汇点。通过分析来自33种不同癌症类型的数据,作者提出SPHK1可能像一个“主调光开关”,既帮助肿瘤更快生长,又抑制抗癌免疫反应。理解这个开关可能为多种癌症(而非单一癌种)的诊断与治疗打开新路径。
许多癌症中的共同线索
研究者没有孤立研究单一肿瘤类型,而是进行了泛癌分析,利用大型公共肿瘤与正常组织数据集。他们测量了33种癌症中SPHK1的表达,并将其与邻近健康组织比较。在十几种癌症中——包括头颈癌、胃癌、肝癌、肺癌、肾癌、膀胱癌和结肠癌——肿瘤组织中的SPHK1水平均明显升高。仅有一种癌症显示出较低水平。团队还检测了来自头颈部、胃和肝癌患者的临床样本,证实在RNA和蛋白水平上SPHK1在肿瘤组织中均持续更高。当他们在体外培养的癌细胞系中降低SPHK1水平时,这些细胞的生长变慢,提示肿瘤可能对该酶存在依赖性。
从生长驱动因子到预后警示
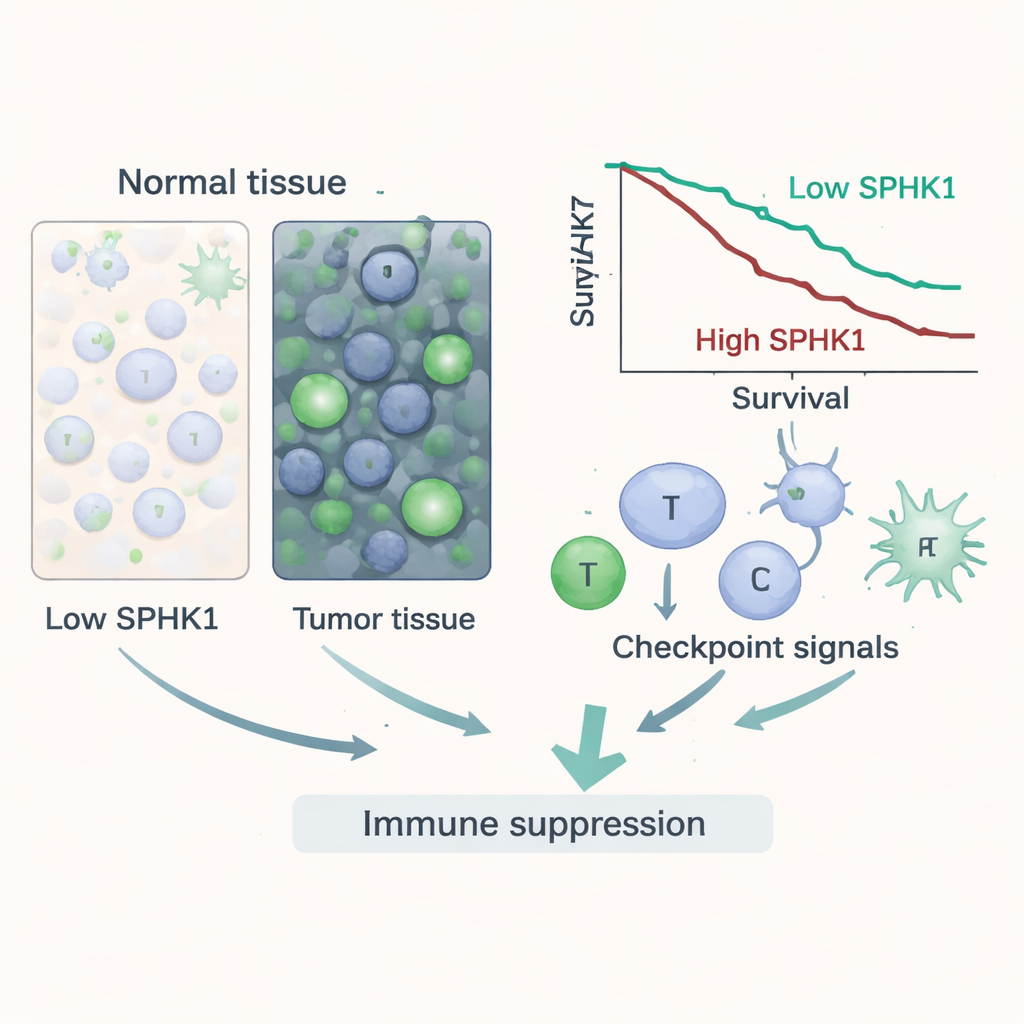
除了单纯的过度表达外,SPHK1还包含有关于患者结局的重要信息。利用数千名患者的生存数据,作者发现较高的SPHK1常与多种癌症中更短的总体生存期和更快的疾病进展相关,如肾癌、肝癌、肺癌及某些脑瘤。即便在调整了年龄、肿瘤分期和分级后,SPHK1在多种癌症中仍是一个独立的风险因素。在评估一个标志物区分肿瘤与正常组织能力的诊断测试中,SPHK1在若干肿瘤中表现良好,尤其是胆管癌及头颈癌、胃癌和甲状腺癌。综上,这些发现将SPHK1定位为既促进生长又可作为识别高危疾病的潜在生物标志物。
肿瘤“燃料”与免疫逃逸如何相互关联
SPHK1调控细胞内两种脂类分子之间的平衡,使信号偏向有利于生存与炎症的一方。研究表明,当SPHK1升高时,肿瘤不仅生长更好,还重塑微环境以抵御免疫细胞。在许多癌症中,SPHK1水平与肿瘤突变负荷和微卫星不稳定性等基因混乱特征相关,而这些特征常与肿瘤对免疫疗法的反应有关。更显著的是,富含SPHK1的肿瘤往往含有处于对杀伤效应较弱状态的免疫细胞群体,同时显示出多种知名的免疫“刹车”分子的活性上调,包括若干导致T细胞衰竭的检查点分子。SPHK1还与招募抑制性免疫细胞的化学信号以及如TGF-β等进一步抑制免疫攻击的因子相关,表明该酶有助于在肿瘤周围建立免疫抑制的堡垒。
为更聪明的联合疗法提供线索
由于SPHK1位于癌症代谢与免疫控制的接口,它可能影响肿瘤对药物的反应。通过将SPHK1水平与来自大型细胞系面板的药物敏感性数据关联,作者发现SPHK1较高的肿瘤对某些特定药物(包括一些靶向药物和化疗药)表现出更高或更低的敏感性。这一模式并非单向,强调SPHK1的效应依赖于具体背景和所用治疗类型。尽管如此,结果提示测量SPHK1可能有助于指导最佳治疗选择,并且阻断SPHK1或其产生信号的药物,可能与现有的免疫检查点抑制剂联合使用,以克服某些患者的耐药性。
这对未来癌症治疗意味着什么
总体而言,该研究认为SPHK1不仅仅是一个简单的癌基因;它充当了一个“代谢-免疫检查点”,将肿瘤的能量供应方式与其抵御免疫攻击的能力连接起来。对非专业读者而言,这意味着一种单一酶既帮助癌症踩下油门,又削弱免疫系统的刹车。通过靶向SPHK1,未来的治疗或许能够同时减缓肿瘤生长并重新激活免疫细胞,从而在多种癌症中实现更有效、个体化的免疫治疗策略。
引用: Wang, L., Zhong, G., Luo, H. et al. The emerging role of SPHK1 at the immune-metabolic interface: a pan-cancer integrative analysis. Sci Rep 16, 5528 (2026). https://doi.org/10.1038/s41598-026-35350-7
关键词: 癌症代谢, 肿瘤免疫逃逸, SPHK1, 泛癌分析, 免疫疗法